Дилатация нпв что это
Дилатационная кардиомиопатия
Не полагайтесь на самоисцеление, если вас беспокоит недомогание, ангинозные боли, головокружения, нарушения дыхательной функции. Врачи «Клиники АВС» вас осмотрят, соберут анамнез и назначат диагностику для уточнения диагноза ДКМП. Исходя из результатов обследования, разработают индивидуальную схему лечения. Чем раньше вы обратитесь к специалистам, тем выше шансы восстановить кардиальную деятельность и предотвратить развитие необратимых последствий.
Механизм развития патологии
Под воздействием определенных факторов снижается количество функционирующих кардиомиоцитов. Это приводит к растягиванию камер сердца, ухудшению насосной функции сердечной мышцы.
В процессе развития патологии в кардиальных структурах наблюдается скопление крови, — она полностью не выбрасывается из-за растяжения стенок и снижения сократительной способности сердца. Возникают застойные процессы, что в дальнейшем провоцируют тромбоэмболический синдром. Сердце увеличивается в размерах, слой функционирующих клеток становится тоньше и мышечная ткань растягивается, снижается сердечный выброс. Это отражается на функционировании всех систем организма. Развивается сердечная недостаточность, ишемия, дистрофия тканей и другие осложнения. Без лечения патология заканчивается внезапным летальным исходом.
Заметьте, что с момента развития первых клинических проявлений до необратимых последствий проходит 5-15 лет.
Причины расширения камер
Дилатационная кардиомиопатия это многофакторное заболевание. Считается, что повлиять на развитие данной патологии может отягощенная наследственность. Примерно в 25 % случаев болезнь является следствием генетических отклонений или врожденных пороков сердца (первичная кардиомиопатия дилатационная).
Вторичная дилатационная кардиомиопатия развивается на фоне других патологий: приобретенные пороки сердца (спровоцированные вредными привычками, перенесенными заболеваниями) сосудистые болезни, токсическое воздействие (медикаменты, наркотики, алкоголь), расстройства метаболизма (вследствие голодания, анорексии, плохого питания), аутоиммунные патологии, инфекционные поражения организма.
Симптомы
Кардиомиопатия дилатационная развивается медленно, симптоматика может не беспокоить годами. Реже патология манифестирует подостро, например, после перенесенных инфекций. Патогномоничными симптомами заболевания являются сердечная недостаточность, аритмия, нарушение проводимости, закупорка сосудов тромбами.
Нарушение работы левого желудочка провоцирует одышку при небольшой нагрузке, усталость из-за повышенного диастолического давления в нем и пониженного сердечного выброса. Дисфункция правого желудочка становится причиной отечности тканей и набухания шейных вен.
Также клиника включает:
Диагностика
Из-за отсутствия специфических клинических проявлений, которые бы четко охарактеризовали данное заболевание, диагностика затруднена. В связи с этим специалисты «Клиники АВС» проводят комплексное и тщательное обследование, чтобы дифференцировать заболевание от других патологий.
Чтобы поставить ДКМП диагноз (дилатационная кардиомиопатия), врачам могут понадобиться результаты следующих исследований:
Лечение
Если патология является вторичной, то требуется этиотропное лечение, т. е. устранение первопричины заболевания. Также терапия должна быть направлена на остановку прогрессирования патологического процесса. Необходима коррекция проявлений сердечной недостаточности, аритмии, повышенной свертываемости крови.
Лечение дилатационной кардиомиопатии зачастую консервативное и включает:
Шансы и осложнения
Прогноз дилатационной кардиомиопатии зависит от своевременности диагностики и адекватности терапии. При выявлении патологии на ранней стадии шансы на продолжительную полноценную жизнь высокие. Если же игнорировать выраженные проявления болезни, то прогноз неблагоприятный. Без медицинской помощи риск летального исхода в ближайшие пару лет возрастает до 70 %.
Чтобы не допустить развития осложнений (кардиогенный шок, инфаркт, полиорганная недостаточность, инсульт, эмболия тромбами), обращайтесь в «Клинику АВС» при малейших подозрениях на заболевания сердца. Вы попадете в руки настоящих профессионалов, которые в кратчайшие сроки проведут необходимое обследование, поставят верный диагноз дилатационная кардиомиопатия и разработают индивидуальную схему лечения.
Синдром нижней полой вены
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Иногда, во время беременности и не только, диагностируют синдром нижней полой вены. Называть данный синдром заболеванием не совсем корректно: скорее, это нарушение адаптации организма к увеличению матки или другим изменениям венозного кровообращения.
В большинстве случаев синдром обнаруживается у женщин с многоплодием, многоводием, крупным плодом, при беременности, сочетающейся с сосудистой гипотонией, а также при опухолях и нарушениях свертываемости крови.
Код по МКБ-10
Причины синдрома нижней полой вены
Изначальная причина синдрома до сих пор окончательно не установлена. Тем не менее, доказано, что провоцирующими факторами могут стать:
Кроме периода вынашивания ребенка, значительно реже синдром нижней полой вены может развиваться при эхинококкозе, опухолевых процессах в брюшной полости. Пациентам с подобными патологиями необходимо быть особенно бдительными относительно своего здоровья.

Патогенез
Патогенез синдрома специфичен, но зависит от особенностей конкретного организма. Чаще всего наблюдается нарушение проходимости основания нижней полой вены, что зачастую может сочетаться с формированием тромба на пораженном участке сосуда.

Симптомы синдрома нижней полой вены
Симптомы данного синдрома зависят от степени пережатия или закупорки просвета нижней полой вены. Наиболее выраженные признаки наблюдаются при максимальной закупорке сосуда в сочетании с ухудшением проходимости вен печени и почек.
Первые признаки синдрома, на которые следует обратить внимание – это ощущения «ползания мурашек» в ногах, с последующим онемением.
Далее болезнь развивается в зависимости от локализации закупорки нижней полой вены.
Кроме этого, может повышаться кровяное давление, появиться слабость и ощущение тревожности, усилиться сердцебиение.
Синдром верхней и нижней полой вены
Появляется синдром верхней и нижней полой вены из-за расстройства кровообращения в верхней полой вене.
Физиологически через верхнюю полую вену течет венозная кровь из верхней части туловища. Нормальный кровоток может быть нарушен опухолевыми процессами, аневризмой, увеличенными лимфатическими узлами, тромбами.
Обычно подобный синдром развивается постепенно. Больной может отмечать у себя периодические головные боли, нарушения сна, кровотечения из носа или горла, ухудшение зрения, трудности с засыпанием в лежачем положении. Со временем у больного появляются отеки, посинение и выделение вен верхней части тела. Одновременно выявляются и симптомы основной патологии, которая изначально спровоцировала непроходимость.
Лечение синдрома верхней и нижней полых вен назначается в зависимости от степени закупорки и её локализации. Консервативная терапия предусматривает прием фибринолитических, антикоагулирующих и дезагрегантных препаратов.
Осложнения и последствия
Синдром нижней полой вены у беременных не всегда приводит к каким-либо негативным последствиям. Дело в том, что у большего количества пациенток отток венозной крови с нижней части тела происходит посредством непарной и позвоночной вены, поэтому синдром нижней полой вены может не сопровождаться нарушением кровообращения.
Опасность представляет ситуация, при которой развивается коллаптоидное состояние. Обычно это происходит во время операции «кесарева сечения» и учитывается врачами.
При значительном придавливании маткой нижней полой вены ухудшается кровообращение непосредственно в матке и почках. Вследствие этого страдает состояние будущего ребенка, а также нарушается клубочковая фильтрация у женщины. Перечисленные процессы могут послужить причинами преждевременной отслойки плаценты, формирования тромбов и варикозного расширения вен.

Диагностика синдрома нижней полой вены
Лабораторные методы: общие анализы крови и мочи, биохимия крови, оценка свертываемости крови.

Что нужно обследовать?
Как обследовать?
Дифференциальная диагностика
Дифференциальная диагностика направлена на исключение экстравазального сдавливания нижней полой вены опухолевым или воспалительным процессом. При этом важно определить наличие или отсутствие опухоли по результатам УЗИ, КТ или флебографии.

К кому обратиться?
Лечение синдрома нижней полой вены
На данный момент не разработано четкой схемы лечения синдрома нижней полой вены. В большинстве ситуаций применяют консервативную терапию с обязательным назначением препаратов, влияющих на сворачиваемость крови, как прямого, так и непрямого воздействия.
При назначении лекарства следует учитывать продолжительность заболевания, которую при данном синдроме определить практически не представляется возможным. Известно, что наибольший эффект противотромботические средства оказывают лишь на начальных этапах формирования закупорки.
Немаловажное значение имеет также поддержание нормальной работы почек и печени.
Применяют до и после оперативного вмешательства, чаще по 0,3 мл инъекционно п/к.
Кровотечения, подкожные гематомы, кровоизлияния.
Препарат не применяют внутримышечно.
Чаще всего принимают перорально, от 2 до 10 мг в сутки.
Кровоточивость, кровоизлияния, анемия, дерматиты, головная боль.
Во время терапевтического курса следует контролировать степень свертываемости крови.
Средство для инфузионной терапии. Доза препарата подбирается только индивидуально.
Кровоточивость десен, гематомы, покраснения кожи, внутренние кровотечения.
Назначают осторожно при заболеваниях печени и почек, а также в пожилом возрасте.
Вводят внутривенно капельно, от 10 до 1000 мл в сутки.
Рвота, зуд кожи, болезненность в пояснице.
Во время лечения обязательно контролируют почечную функцию.
Принимают по 75 мг трижды в сутки.
Учащенное сердцебиение, диспепсия, тромбоцитопения, шум в ушах, ощущение слабости.
Не рекомендуется принимать одновременно с кофеин содержащими напитками.
Основные витамины, которые способствуют укреплению венозных стенок – это токоферол и аскорбиновая кислота. Пища, богатая этими витаминами, снижает вероятность формирования тромбов и закупорки нижней полой вены.
Токоферол (в. E) присутствует в бобах, злаках, печени, брокколи, а также в растительных маслах.
Аскорбиновая кислота в достаточном количестве находится в ягодах, винограде, киви и цитрусах.
Кроме этого, желательно употреблять пищу, богатую каротином, рутином, а также такими микроэлементами, как медь, железо и цинк. Для этого необходимо чаще готовить блюда из капусты, орехов, красных фруктов и овощей, мяса.
Из фармацевтических препаратов особенно рекомендуются Аевит и Аскорутин, которые назначают по 1 таблетке или капсуле дважды в сутки, в течение 3-4 недель. При беременности необходимо подбирать витаминный препарат только под контролем врача.
Физиотерапевтическое лечение при синдроме нижней полой вены применяется крайне редко. Возможно назначение лечебной физкультуры, мануальной терапии (согласно показаниям).
Гомеопатия уже много лет занимается лечением заболеваний такого рода, как синдром нижней полой вены. Врачи гомеопаты в данном случае советуют применять средства, укрепляющие сосудистые стенки, регулирующие кровообращение и улучшающие свойства крови. Тактика лечения обычно определяется в зависимости от болезни или состояния, которые могли спровоцировать закупорку вены.
В последнее время интерес представляют следующие гомеопатические препараты:
Кроме этого, могут быть назначены препараты, приготовленные на основе свертывающих факторов: тромбина, фибриногена, фибрина и пр. В перспективе рекомендуется применять средства Aorta suis Ingeel, Arteria suis Injeel, Vena suis Ingeel, которые изготовлены из тромботического материала.
Оперативное лечение назначают при тромбозе нижней полой вены:
Операции не рекомендуются, если у пациента имеется декомпенсация сердечной деятельности, свежий инсульт сосудов головного мозга.
Народное лечение
По согласованию с врачом можно использовать следующие народные рецепты:
Лечение травами часто включает в себя и сложные многокомпонентные рецепты:

УЗИ нижней полой вены (норма и патология)
УЗИ нижней полой вены. Анатомия
Прежде чем разобрать характеристики УЗИ, рассмотрим анатомические особенность нижней полой вены (НПВ). Нижняя полая вена образована слиянием общих подвздошных вен на уровне 5-го поясничного отдела позвонка и идет справа краниально от средней линии. Она проходит через диафрагму на уровне 8-го грудного позвонка и входит в правое предсердие. У зародыша имеется сложное венозное расположение венозных пазух, которые образуются во время эмбриогенеза, и несколько из них способствуют формированию нижней полой вены. Это означает что есть много вариантов анатомии НПВ, которые можно будет видеть на УЗИ. Наиболее распространенным вариантом является то, что общие подвздошные вены продолжаются краниально как парные «полые вены» с пересечением левого компонента для соединения с правой стороной на уровне левой почечной вены. Много другие изменения были также зарегистрированы. Такие состояния легко и больше оцениваются с помощью контрастного КТ, чем при ультразвуковом сканировании, но может вызвать некоторую путаницу, если они видны во время УЗИ и не распознаются.
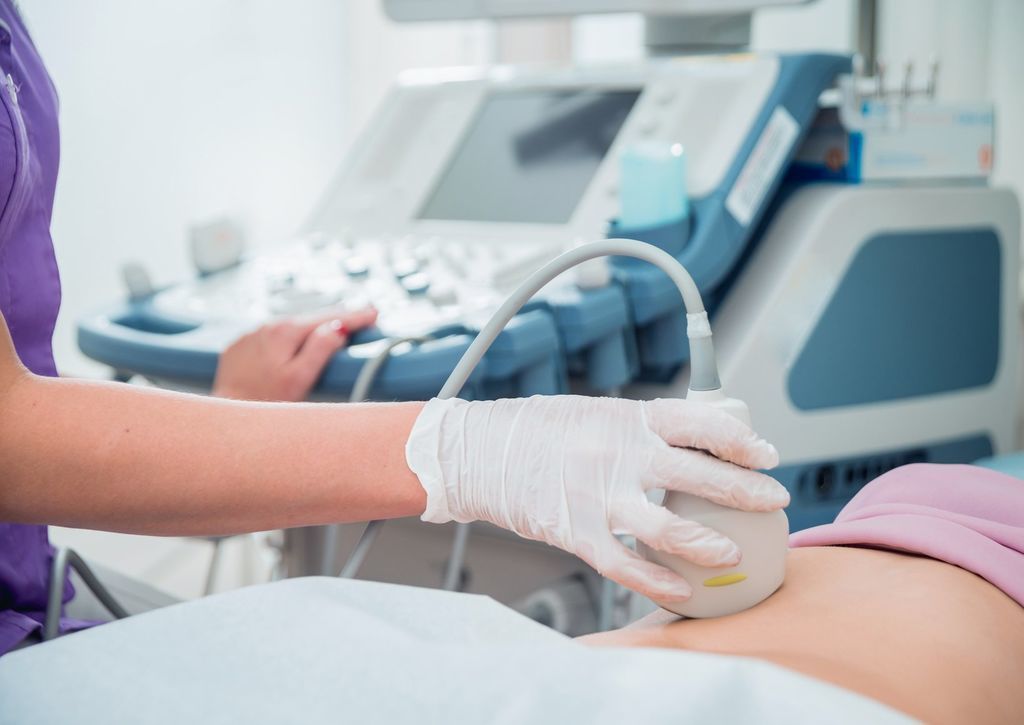
ТЕХНИКА УЛЬТРАЗВУКОВОГО ИССЛЕДОВАНИЯ НПВ
Нижнюю полую вену исследуют с использованием УЗИ методик, описанных нами ранее для брюшной аорты. Однако в положении на спине сосуд может быть узким и в переднезадней плоскости его трудно определить. Поперечное сканирование с цветным допплером и использованием аорты в качестве ориентира может позволить определить локализацию вены в этих обстоятельствах. Другой прием, с поднятием ног помощником будет увеличивать поток и калибр вены, делая его более заметным. Калибр НПВ будет варьироваться в зависимости от состояния гидратации больного. У хорошо-гидратированного пациента нижняя полая вена на УЗИ будет растянута, в то время как у обезвоженного пациента будет спадаться, тогда ее узкий просвет будет сложнее визуализировать. Избыточное давление датчиком, приложенное для рассеивания газа в кишечнике, также может сжать может НПВ, поэтому необходимо искать баланс для визуализации сегментов сосуда у некоторых сложных пациентов.
НОРМАЛЬНЫЕ И ПАТОЛОГИЧЕСКИЕ ИЗМЕНЕНИЯ НИЖНЕЙ ПОЛОЙ ВЕНЫ НА УЗИ
Поток в нижней полой вене на УЗИ в норме медленный и меняется в зависимости от как дыхание, так и пульсация сердца. На вдохе диафрагма опускается и это приводит к отрицательному давлению в грудной клетке и повышению давления в брюшной полости, поэтому кровь течет из живота к грудному отделу, обратное происходит по истечении срока этой фазы дыхания. На это накладывается более быстрая периодичность в результате сердечной деятельности, что видно особенно в верхней части живота. Известно также, что форма волны в нижней полой вене также зависит от степени гидратация больного. У обезвоженного пациента НПВ будет узкой и ее довольно трудно увидеть, также как и почечные вены, в то время как при перегрузке жидкости нижняя полая вена на УЗИ расширена и сердечная периодичность обнаруживается вниз на подвздошные вены.
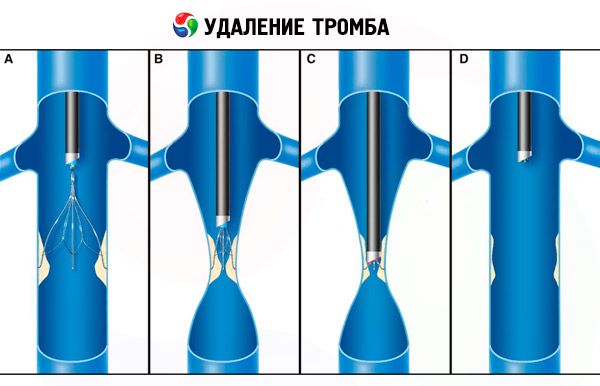
Одним из наиболее распространенных показаний для специфического обследования нижней полой вены является оценка того, распространился ли тромб из тромбоза глубоких вен таза или нижних конечностей в ее просвет. Тромб может заполнить просвет НПВ и даже вызвать расширение этого сосуда. В качестве альтернативы можно увидеть язык тромба, лежащий свободно в просвете, идущий вверх по направлению к правому предсердию.
У некоторых пациентов, которые подвергаются риску легочной эмболии из-за более дистального тромба, вводятся кава-фильтры. Есть несколько типов, но все они вставляются в среднюю или нижнюю область, ниже почечных вен. Выявление металлической эхогенной структуры на УЗИ в нижней полой вене над уровнем почечных вен может указывать на миграцию фильтра. Существует небольшой риск того, что тромб может пройти через фильтр или развиться тромбоз на месте фильтра. Цветной допплер — это быстрый и простой метод подтверждения проходимости НПВ вокруг фильтра и над ним. Металлические стойки фильтра могут быть распознаны в просвете нижней полой вены, и цветной допплер, или энергетический допплер, покажет кровоток за уровнем фильтра.
Опухоли почек и гепатоцеллюлярная карцинома представляют собой две опухоли, которые имеют тенденцию проникать в венозные сосуды, и в результате опухолевый тромб может распространяться в полость из почечной или печеночной вены. Нарушение венозного оттока печени или почек на УЗИ проявляется потерей нормальной сердечной и дыхательной периодичности формы венозной волны, и опухолевый тромб может быть отчетливо виден, когда он распространяется в просвет полости. Некоторые опухоли забрюшинного пространства могут сдавливать или непосредственно вторгаться в нижнюю полую вену, вызывая обструкцию венозного возврата из нижней части живота и ног. Хотя каудальные сегменты нижней полой вены и подвздошных вен обычно остаются открытыми, они часто будут расширяться, венозный кровоток будет вялым или ретроградным, профиль потока будет плоским, и отсутствовать нормальная реакция Вальсальвы. В редких случаях в стенке НПВ могут развиваться внутренние опухоли, обычно мезенхимальные по происхождению, такие как фибросаркомы, лейомиосаркомы, также сообщалось о нахождении липомы на УЗИ.
После трансплантации печени следует оценить просвет НПВ для обеспечения удовлетворительного кровотока. Внешний вид будет зависеть от типа выполняемого анастомоза. В прошлом сегмент донорской НПВ, прикрепленный к новой печени, заменял эквивалентный сегмент нативной нижней поло вены, который был удален с больной печенью. Многие хирурги в настоящее время выполняют технику «контрейлерных перевозок», когда нативная НПВ остается на месте, нижний конец донорского полого сегмента зашивается, а верхний конец анастомозируется с нативной нижней полой веной. Это приводит к появлению послеоперационного периода, который может сбивать с толку, если его не распознать, так как могут появиться две НПВ на УЗИ, связанные с пересаженной печенью. Другие послеоперационные проблемы, которые могут возникнуть в связи с НПВ после трансплантации, включают компрессию, если новая печень относительно большая; искажение нижней полой вены также может произойти, если имеется относительное скручивание кавального канала в результате встраивания донорской печени в новые условия. В долгосрочной перспективе стеноз может развиваться в местах анастомоза. Пересадка печени будет рассматриваться в других постах блога.
Забрюшинные и другие образования брюшной полости могут сдавливать или закупоривать нижнюю полую вену. Ситуация на УЗИ обычно очевидна, особенно с цветным допплером, который показывает, что НПВ входит в образование и сужается или перекрывается отсутствующим потоком. Могут возникнуть врожденные ткани, особенно в верхнем конце НПВ. Это может приводить к различной степени ее сужения, а в некоторых случаях может предрасполагать к тромбозу печеночной вены и синдрому Бадда-Киари.
Свищи, вовлекающие нижнюю полую вену, могут редко встречаться самопроизвольно, часто вторично к аневризме аорты, или они могут быть созданы хирургическим путем, как в случае с портокавальными шунтами. В случае аортокавальных свищей на УЗИ цветовой допплер может показать видимый тканевый отросток с пульсирующим течением в полости выше уровня фистулы; иногда сам фистулу трудно идентифицировать. Хирургические портокавальные шунты обычно представляют собой шунтирующие из стороны в сторону в верхней части живота на уровне, где проксимальная основная воротная вена проходит близко перед полостью. Ткань может быть заметна, и шунт легче идентифицировать, если печень можно использовать как окно до точки анастомоза, а поворот пациента вверх на левую сторону может облегчить визуализацию. Тем не менее, в настоящее время они выполняются редко, их заменяют внутрипеченочные внутрипеченочные портосистемные шунты.
Воротная вена
Поражения воротной вены
Выделяют следующие виды патологий.
Портальная гипертензия. Данное заболевание характеризуется увеличением внутреннего давления в воротной вене. Причинами развития данной патологии могут быть вирусные гепатиты, печеночный цирроз, нарушения обменных процессов, тяжелые сердечные заболевания, тромбы печеночных, селезеночных вен и другие. Симптоматика выражена диспепсией, снижением веса, тяжестью в правом подреберье, общей слабостью.
Тромбоз. Данная тяжелая патология развивается при формировании кровяных сгустков в просвете воротной вены, препятствующих оттоку крови. Основными причинами развития тромбоза являются следующие: воспаление и злокачественные образования органов пищеварения, травмы печени, желчного пузыря, селезенки, аномалии свертываемости крови, цирроз, различные инфекции и другие. Патология проявляется болевыми ощущениями в области живота, тошнотой с последующей рвотой, повышением температуры, диспепсическим синдромом и другими симптомами.
Кавернозная трансформация. Заболевание характеризуется образованием сосудистых полостей (каверном), заполненных кровью, и развивается вследствие генетического порока формирования вен, заключающегося в их значительном сужении, частичном или полном отсутствии. Кавернозная трансформация является врожденной аномалией. Если она не была выявлена в детстве, то обнаруженная в зрелом возрасте указывает на прогрессирующую портальную гипертензию, вызванную гепатитом или циррозом.
Пилефлебит. Эта патология характеризуется гнойным воспалением воротной вены, спровоцированным перитонитом, возникшим после перенесенного острого аппендицита. Симптомами пилефлебита являются: сильный жар, боли в животе с признаками отравления, желтуха, внутреннее кровоизлияние в венозной области пищевода, желудка и другие.
Диагностика и лечение
Диагностические мероприятия включают в себя следующие этапы и методы: осмотр, сбор анамнеза, ультразвуковое обследование, компьютерную и магнитно-резонансную томографию, портографию. Полученные инструментальными обследованиями данные дополняются показателями анализов крови. Лечение зависит от вида и тяжести поражения, сопутствующих симптоматических патологий и других факторов.
Синдром портальной гипертензии
Введение
Кровь, питающая ряд органов брюшной полости, отводится по единому венозному руслу. Эта вена называется (учитывая ее расположение) воротной или портальной веной печени; она имеет множество ответвлений и является наиболее крупной веной в организме человека, достигая в диаметре 8-12 мм. Как и в любом ином магистральном кровеносном сосуде, в воротной вене должно постоянно поддерживаться определенное кровяное давление – здесь оно в норме составляет от 5-7 до 10-12 мм рт. ст. Хроническое превышение этого уровня приводит к общим нарушениям гемо- и гидродинамики брюшной полости, дегенеративным изменениям в тканях и другим тяжелым последствиям, которые в совокупности образуют синдром портальной гипертензии.
По определению, синдром не является самостоятельным заболеванием; это устойчивое, повторяющееся сочетание взаимосвязанных клинических симптомов, которое может формироваться в силу разных причин, но обладает собственными специфическими закономерностями развития и протекания. Это в полной мере касается и синдрома портальной гипертензии.
Причины
Выделяют две основные группы причин развития портальной гипертензии: внепеченочные и внутрипеченочные. На этих же критериях (конкретная локализация блока воротной вены) построены общепринятые ее классификации, обычно включающие под- или предпеченочную форму, внутрипеченочную (с несколькими подтипами), надпеченочную и смешанную.
Согласно доступной медицинской статистике, наиболее распространенной (85-90%) является внутрипеченочная локализация нарушений портально-венозного оттока. В этиологическом плане внутрипеченочная портальная гипертензия чаще всего обусловлена циррозом печени или иным процессом дегенеративного замещения паренхиматозных клеток соединительной тканью.
Предпеченочная форма составляет 10-12% в общем объеме портальной гипертензии и, как правило, развивается вследствие механического давления (например, злокачественной опухолью), врожденных или приобретенных аномалий анатомического строения вены, воспалительного процесса в миокарде, обструктивного тромбоза Бадда-Киари и пр.
Частота надпеченочной (постпеченочной) формы не превышает 3-4%; причинами обычно становятся прорастание опухоли, тромбоз, эндофлебит печеночных вен.
В целом, к перечню этиопатогенетических факторов портальной гипертензии следует добавить все разновидности гепатитов, онкозаболевания, патологию билиарной (желчевыводящей) и сердечнососудистой систем, последствия травм и некоторых хирургических вмешательств, отравления (медикаментами, грибами, соединениями меди и пр.), ожоги. Кроме того, портальная гипертензия нередко развивается на фоне жизнеугрожающих состояний в ходе реанимационных мероприятий.
Симптоматика
Классическая триада симптомов включает варикозное расширение вен пищевода и верхних отделов желудка (в 85% случаев), спленомегалию (селезенка в той или иной степени увеличена практически всегда) и асцит (массивное скопление жидкости в брюшной полости).
Ранние проявления синдрома портальной гипертензии могут быть неспецифическими: признаки диспепсии (абдоминальные боли и тяжесть в животе, тошнота, различные проблемы с дефекацией, метеоризм и т.д.). Кроме того, по мере нарастания выраженности нарушений кровоснабжения печени снижается ее способность к выполнению дезинтоксикационных функций, что отражается и на функционировании мозга, – развивается т.н. печеночная энцефалопатия с присущей ей психоневрологической симптоматикой. При тяжелой печеночной недостаточности наблюдается желтуха. Прямую угрозу жизни несут (и нередко приводят к летальному исходу) внутренние кровотечения из растянутых и истонченных венозных стенок.
Выраженность, стадийность и скорость появления симптомов в значительной мере различаются при разных типах портальной гипертензии. Так, «водянка живота» (асцит) в одних случаях развивается постепенно, в других остро, и т.д.
Диагностика
Диагноз устанавливается путем сопоставления жалоб, анамнестических данных, результатов клинического осмотра и инструментального обследования. В частности, необходимой и обязательной является ФГДС (фиброгастродуоденоскопия), в ходе которой визуализируются вены пищевода и желудка, оценивается их статус и собирается другая клинически значимая информация. Назначают УЗИ в дуплекс-режиме, рентгенографию, по необходимости – дополнительные методы исследования селезенки и гепатобилиарной системы (сканирование печени, спленоманометрия, спленопортография, КТ, МРТ и т.д.).
Лечение
Синдром портальной гипертензии, в целом, весьма проблематичен в терапевтическом плане. Амбулаторное консервативное лечение и курсы поддерживающей терапии могут занимать несколько лет; назначаются «прицельные» гипотензивные средства для снижения давления в воротной, нижней полой и печеночных венах, вазо- и гепатопротекторы. Однако с усугублением ситуации амбулаторное лечение становится все менее эффективным, и пациента приходится госпитализировать, – сроки стационарного лечения варьируют от двух недель до месяца и более.
Масштабы и цели хирургического вмешательства, – если оно целесообразно и необходимо, – определяются особенностями конкретного случая: в различных ситуациях основной задачей может быть восстановление венозной проходимости, коррекция путей отвода крови, удаление из брюшной полости избыточной жидкости при асците, склерозирование расширенных и кровоточащих вен пищевода, и т.д. Однако относительными или абсолютными противопоказаниями к операции могут становиться сопутствующие хронические заболевания, беременность, пожилой возраст, тяжелое общее состояние пациента (обусловленное, например, выраженной печеночной недостаточностью).
Отдаленный прогноз при некоторых формах синдрома портальной гипертензии (внутрипеченочная, надпеченочная) неблагоприятен, особенно при пищеводно-желудочных геморрагиях у больных циррозом печени. В других случаях оперативное вмешательство может значительно улучшить ситуацию. Однако единственным радикальным лечением в настоящее время остается трансплантация печени.