Что такое градиент давления в эхокардиографии
Что такое градиент давления в эхокардиографии
В местах сужения поперечного сечения потока крови возникает перепад давления, который в клинической практике обозначается как «градиент давления». Уменьшающаяся на протяжении сужения энергия давления преобразуется в кинетическую энергию, ускоряющую движение жидкости в области сужения до более высоких скоростей. Поэтому по разнице скоростей (до и в месте сужения) можно сделать вывод о величине падения давления, т.е. о «градиенте давления».
а) Уравнение Бернулли. С физической точки зрения эта взаимосвязь точно описывается (для идеальных, «ньютоновских» жидкостей) математической формулировкой закона сохранения энергии, известной как уравнение Бернулли и представляющей собой частный случай общего уравнения Эйлера или уравнения Навье-Стокса:
б) Упрощения. Для практического использования в повседневной кардиологической практике это общее уравнение можно значительно упростить до квадратичной связи между давлением и скоростью движения жидкости:
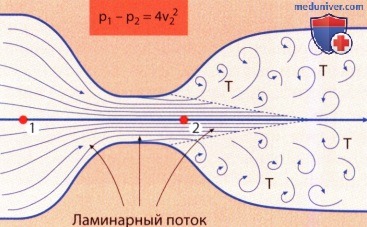
Применение уравнения Бернулли представлено в тексте. Следует обратить внимание на возникновение турбулентностей (Т) непосредственно за местом стеноза.
До стеноза и вплоть до клиновидного ядра потока после стеноза течение жидкости ламинарно, пока не «уничтожается» множеством завихрений.
в) Исключения. Следует помнить, что упрощенное уравнение Бернулли (В) применимо лишь тогда, когда можно пренебречь проксимальной скоростью перед стенозом (1 м/с или меньше). Но, например, в случае одновременной выраженной недостаточности аортального клапана это не так; тогда следует учесть проксимальную скорость и использовать уравнение (А). Кроме того, по физическим причинам (низкие) скорости в области нормальных или лишь слегка стенозированных просветов клапанов нельзя просто пересчитать в градиенты по уравнению (В). В таких случаях в заключении вместо указания на градиент давления предпочтительнее указывать максимальную скорость движения крови.
Описание феномена восстановления давления («pressure recovery») см. в статьях на сайте об аортальном клапане и о клапанных протезах.
Редактор: Искандер Милевски. Дата публикации: 17.12.2019
Архив
Radhakrishnan Ramaraj, Vincent L. Sorrell
Дегенеративный аортальный стеноз (АС) — наиболее распространенная патология клапанов сердца в Европе и Северной Америке. Преимущественно он проявляется в виде кальциноза аортального клапана (АК), который встречается у 2–7% представителей популяции старше 65 лет. Около 80% взрослых пациентов с симптомным АС — мужчины. Поскольку 1–2% общей популяции рождается с двустворчатым АК, к тому же наблюдается старение населения, АС выявляется все чаще и чаще. Предполагается, что к 2020 году в Англии у 3,5 млн. человек будет АС, при этом у 150 тысяч диагностируют тяжелый аортальный стеноз. В данной статье представлены основы диагностики и лечения больных с АС и его последствиями. Большинство действующих рекомендаций основано на результатах рандомизированных контролированных исследований. Представлены также данные обзорных исследований и согласованные рекомендации Американской ассоциации сердца (АНА), Американской коллегии кардиологов (АСС) и Европейского общества кардиологов (ESC), что позволяет более полноценно осветить аспекты, не являющиеся предметом данной публикации.
Причины аортального стеноза
Наиболее распространенная причина АС — кальцификация нормального трехстворчатого аортального клапана (рис. 1). Считается, что кальцифицирующий АС — это дегенеративный процесс, имеющий много общих признаков с заболеваниями коронарных артерий, таких как липидные скопления, воспаление и кальциноз. Изменения структуры двух- или одностворчатого АК обусловливают уязвимость створок к гемодинамической нагрузке. Это приводит к утолщению створок, их кальцификации, повышению ригидности и сужению аортального отверстия.
Аортальный стеноз может также быть вторичным, — т. е. формироваться после ревматического воспаления створок клапанов. Исследователи выявили общие гистологические признаки повреждений при АС и атероматозном поражении коронарных артерий. Удалось также доказать связь между традиционными факторами риска атеросклероза и развитием кальциноза АК. Установлено, что гиперхолестеринемия может индуцировать пролиферацию клеток и экспрессию фенотипа остеобластов, что обусловливает прогрессирующее поражение АК.
Классификация гемодинамической тяжести аортального стеноза
В 2006 году AHA и ACC опубликовали общие рекомендации по оценке степени тяжести АС (табл. 1), в которых выделен АС легкой, средней и тяжелой степени (рис. 2 и 3). Недавно были также опубликованы рекомендации ESC (2007).
| Степень тяжести АС | Площадь АК | Средний градиент давления на АК | Скорость аортального потока | |
|---|---|---|---|---|
| Легкой степени АС | >1,5 см 2 | 2 | 25–40 мм рт. ст. | 3–4 м/с |
| Тяжелой степени АС | 2 | >40 мм рт. ст. | >4 м/с |
Рисунок 1. Трехмерное чреспищеводное эхокардиографическое изображение области на уровне трехстворчатого АК с перспективы корня аорты (визуализация в направлении полости левого желудочка) в момент полного открытия трехстворчатого АК (слева — фаза диастолы, справа — фаза систолы).
Рисунок 2. Допплеровское исследование в импульсном режиме: двухмерная трансторакальная ЭхоКГ (пятикамерное изображение сердца с верхушечного подхода). Пробный объем импульсного допплера расположен проксимальнее стенозированного АК в выносящем тракте левого желудочка. Скорость кровотока в выносящем тракте левого желудочка 1,0 м/с эквивалентна градиенту давления 4 мм рт. ст.
Рисунок 3. Исследование в режиме непрерывного (постоянного) допплера у пациента с тяжелым аортальным стенозом (тот же пациент, что и на рисунке 2). Двухмерная трансторакальная ЭхоКГ (пятикамерное изображение сердца с верхушечного подхода). С помощью постоянного допплера регистрируется максимальная скорость в точке наибольшего сужения стенозированного аортального отверстия. Соотношение скорости кровотока в выносящем тракте левого желудочка (1,0 м/с) и скорости кровотока на уровне суженного клапана (4,5 м/с) меньше 0,25, что свидетельствует о тяжелом аортальном стенозе.
Аортальный стеноз обусловливает систолический градиент давления между выносящим трактом левого желудочка и аортой. Аортальный стеноз необходимо отличать от склероза аортального клапана, при котором утолщение и кальциноз клапана не сопровождаются обструкцией (высоким градиентом давления) (рис. 1). Однако на протяжении 7 лет у 16% пациентов со склерозом аортального клапана наблюдается прогрессирование до АС.
Как диагностировать аортальный стеноз?
Ключевыми элементами диагностики АС являются анамнез и физикальное исследование. Для дальнейшего подбора оптимального лечения важно обращать внимание на такие симптомы, как ощущение нехватки воздуха при нагрузке, стенокардия, головокружение или синкопе. Характерный систолический шум свидетельствует о необходимости более углубленной диагностики. Шум с ранним пиком, как правило, ассоциируется с менее выраженным стенозом клапана, тогда как наличие позднего пика — с более тяжелой степенью стеноза. Объяснением этого служит более длительный период, необходимый для достижения в желудочке давления, которое обеспечит выброс крови с возможностью ее прохождения через стенозированный клапан. Иногда выслушивается шум слабой интенсивности, первичным проявлением при этом может стать сердечная недостаточность неизвестного происхождения. Исчезновение аортального компонента второго тона является специфическим признаком тяжелого АС, хотя и недостаточно чувствительным. У многих пациентов шум АС не выслушивается (или не распознается), особенно при наличии ожирения или обструктивного заболевания легких (при которых шум приглушен) либо дисфункции левого желудочка (когда интенсивность шума существенно снижена).
Естественное течение аортального стеноза
Необходимость поддержания адекватного сердечного выброса на фоне градиента давления, обусловленного аортальным стенозом, приводит к гипертрофии левого желудочка. Увеличение массы миокарда левого желудочка сопровождается повышением потребления им кислорода. При тяжелом АС, даже при отсутствии сужения коронарных артерий, увеличивается нагрузка на левый желудочек и потребность миокарда в артериальной крови для обеспечения работы сердца. Кроме того, при повышенном диастолическом давлении в желудочке происходит непосредственное сдавливание коронарных артерий в период диастолы. Если это давление превышает уровень, необходимый для адекватной перфузии коронарных артерий, могут развиваться ишемия миокарда и стенокардия. В типичных случаях выявляют выраженную диастолическую дисфункцию левого желудочка. В то же время, систолическая дисфункция также не является редкостью. Оба указанных состояния способствуют развитию симптомов застойной сердечной недостаточности.
Средняя выживаемость пациентов с момента возникновения симптомов составляет всего два-три года. На основании данных, полученных при вскрытии, у пациентов, не лечившихся оперативным путем, были установлены следующие средние сроки до наступления смерти после манифестации симптоматики: стенокардия — три года, синкопе — три года, одышка — два года, застойная сердечная недостаточность — полтора-два года. И наоборот, у бессимптомных пациентов, даже при наличии тяжелого АС, прогноз отличный без протезирования АК. При этом продолжительность бессимптомного периода может быть различной. К сожалению, как минимум, 1–2% бессимптомных пациентов умирает внезапно или же у них наблюдается быстрое прогрессирование до клинической симптоматики с последующей внезапной смертью. У пациентов с врожденным или дегенеративным пороком необходимость в протезировании клапана ранее всего возникает при одностворчатом клапане, затем — при двустворчатом и позже всего — при трехстворчатом АК.
Существуют ли методы медикаментозного лечения аортального стеноза?
При появлении симптоматики резко возрастает смертность, поэтому в согласованных стандартах рекомендуется хирургическое лечение. Эффективных средств медикаментозного лечения тяжелого АС не существует, и только некоторые препараты способны облегчить клинические симптомы. У пациентов с признаками застоя в легких полезным может быть осторожное назначение дигоксина или диуретиков либо их комбинации. Недавно завершилось обсервационное, одностороннее слепое исследование с отменой препарата и проведением рандомизации в порядке тестирования. Удалось засвидетельствовать безопасность применения ингибиторов ангиотензин-превращающего фермента (ИАПФ) и краткосрочную эффективность указанных препаратов у пациентов с АС. При наличии АС снижение постнагрузки на фоне ИАПФ частично ослабляется вследствие параллельного увеличения градиента давления на клапане. В то же время, ИАПФ благоприятно влияют на гемодинамические показатели на фоне стресса у большинства пациентов с сопутствующей артериальной гипертензией. В односторонне слепом исследовании, проводившемся в Кливленде, было установлено, что у пациентов с острым отеком легких, систолической дисфункцией левого желудочка и АС инфузия нитропруссида позволяет уменьшить признаки застоя и сгладить клинические проявления. Неблагоприятное влияние на насосную функцию предсердий и частоту сердечных сокращений оказывает мерцательная аритмия; в таком случае полезным является немедленное проведение кардиоверсии. Профилактика эндокардита показана всем пациентам с аортальным стенозом.
Не существует средств медикаментозного лечения, способных предотвратить или отсрочить прогрессирующее поражение створок АК. Ассоциативная связь АС с клиническими признаками атеросклероза позволила сформулировать гипотезу о возможности замедления или предотвращения прогрессирующего поражения створок АК на фоне интенсивной коррекции факторов риска ИБС. Несмотря на появившиеся надежды, в недавних исследованиях с применением статинов были получены неоднородные результаты. В одном из исследований не удалось засвидетельствовать благоприятные эффекты, тогда как в другом применение розувастатина сопровождалось замедлением гемодинамического прогрессирования АС.
Какое лечение является наиболее эффективным?
Аортальный стеноз вызван механической обструкцией, и поэтому требуется механическая коррекция. С момента возникновения симптомов, если не проводится протезирование АК, предполагаемая продолжительность жизни значительно уменьшается. При этом корригированные по возрасту показатели 10-летней выживаемости пациентов с протезом АК приближаются к таковым в общей популяции. Учитывая это, при отсутствии серьезных сопутствующих заболеваний протезирование АК показано практически всем пациентам с симптоматикой тяжелого АС, даже лицам старческого возраста. Баллонная вальвулопластика не рекомендуется взрослым, но может использоваться как мостик к хирургическому лечению при гемодинамической нестабильности с высокой степенью операционного риска или у пациентов с бессимптомным тяжелым АС, нуждающихся в ургентном обширном некардиальном оперативном вмешательстве.
Большинству пациентов старше 40–45 лет перед протезированием АК показана коронарная ангиография с целью исключения сопутствующего атеросклероза коронарных артерий. Если после эхокардиографии все же не удается точно подтвердить диагноз, ангиографическое исследование поможет определить наличие и оценить степень тяжести АС. Приблизительно у 40% пациентов, которым осуществляется протезирование АК, обнаруживаются признаки тяжелого атеросклероза коронарных артерий. В подобных случаях показано одновременное аортокоронарное шунтирование. Чрескожное протезирование АК возможно, но проводится нечасто. Для установления его потенциальной эффективности необходимы последующие исследования. У бессимптомных пациентов с тяжелым АС прогноз отличный без протезирования АК. У пациентов с дисфункцией левого желудочка и тяжелым АС прогноз после протезирования АК является благоприятным, несмотря на снижение фракции выброса до операции. Дисфункция левого желудочка может быть частично связана с повышением постнагрузки. В данном случае после устранения обструкции систолическая функция левого желудочка часто восстанавливается до нормы.
Является ли возраст противопоказанием для протезирования аортального клапана?
Проспективные и обсервационные исследования свидетельствуют, что протезирование АК уменьшает симптоматику и повышает выживаемость больных с тяжелым АС. Возраст не является противопоказанием для хирургического вмешательства. Прогноз подобен таковому у здоровых лиц соответствующего возраста. Риск операции можно рассчитать с помощью доступного онлайн и проверенного калькулятора риска — European System for Cardiac Operative Risk Evaluation (www.euroscore.org). Показания к протезированию АК приведены в рекомендациях АНА/АСС (2006) (табл. 2, рис. 4) и ESC (2007). Для исходной оценки состояния пациентов с подозрением на АС следует провести допплерэхокардиографию. Данный метод исследования показан также больным с ранее установленным диагнозом при появлении симптоматики или изменении физикальных признаков.
Рекомендации ESC (2007) по наблюдению за пациентами с аортальным стенозом:
Рисунок 4. Алгоритм лечения аортального стеноза, основанный на рекомендациях АНА/АСС (2006).
Как спрогнозировать скорость прогрессирования аортального стеноза?
Скорость прогрессирования аортального стеноза у конкретного пациента рассчитать невозможно. Однако АС быстрее прогрессирует при дегенеративном кальцинозе клапана, нежели при врожденном или ревматическом пороке. Результаты ряда исследований позволили предположить, что скорость нарастания гемодинамических нарушений увеличивается у лиц старше 50 лет, при выраженном кальцинозе клапана или сопутствующей ИБС. Имеются предварительные доказательства возможности прогнозирования бессимптомной выживаемости при аортальном стенозе по уровню натрийуретических пептидов в крови. В таблице 3 приведены факторы прогрессирования АС и неблагоприятного исхода у бессимптомных пациентов.





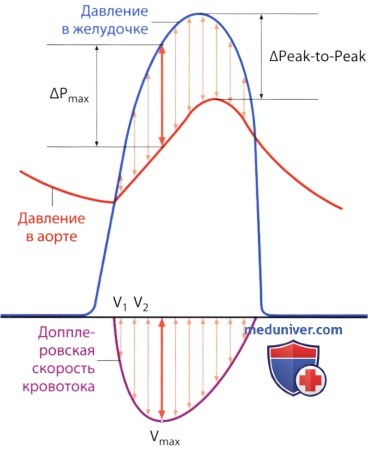 Сравнение кривых межпикового градиента давления (Peak-to-Peak), определяемого при катетеризации полостей сердца, и мгновенного пикового градиента давления (ΔPmax), рассчитываемого по максимальной скорости потока Vmax (допплеровский градиент).
Сравнение кривых межпикового градиента давления (Peak-to-Peak), определяемого при катетеризации полостей сердца, и мгновенного пикового градиента давления (ΔPmax), рассчитываемого по максимальной скорости потока Vmax (допплеровский градиент). 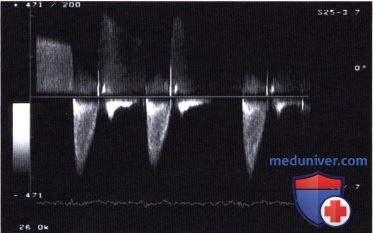 Пример вариабельности градиента давления от сокращения к сокращению при мерцании предсердий.
Пример вариабельности градиента давления от сокращения к сокращению при мерцании предсердий.