Что такое диффузная крупноклеточная в клеточная лимфома
Что такое диффузная крупноклеточная в клеточная лимфома
Диффузная В-клеточная крупноклеточная лимфома относится к агрессивному классу лимфом.
«В-клеточная», потому что состоит из заболевших В-клеток, а В-клетки (В-лимфоциты) – это клетки-следователи, они ищут и передают сообщения о клетках-чужаках другим членам иммунитета. Опорными пунктами иммунной системы являются лимфатические узлы, которые имеют свое строение и разделены на области. Каждая область лимфатического узла выполняет определенную работу. При диффузной В-крупноклеточной лимфоме строение лимфатического узла нарушено, опухолевые клетки находятся во всех областях, то есть диффузно, поэтому и лимфома называется «диффузной».
Одиночные лимфомные опухоли могут появляться в любой точке тела, хотя чаще при этой болезни увеличиваются лимфатические узлы группами на шее, подмышками, в паху и в других местах. Увеличенные узлы можно прощупать руками или найти с помощью рентгена и ультразвука (УЗИ). У больного могут появляться такие признаки болезни, которые называются «В-симптомы»: он быстро худеет, у него поднимается температура и появляется сильная потливость вечером и ночью. Диффузная В-клеточная крупноклеточная лимфома может возникнуть сама или ее могут вызвать другие лимфомы, которые развиваются в организме больного медленно, так называемые индолентные, вялотекущие лимфомы.
Существуют разные виды диффузной В-крупноклеточной лимфомы:
Диффузная В-клеточная крупноклеточная лимфома быстро нарастает, прогрессирует, но в целом хорошо поддается лечению.
Диагноз
Чтобы поставить правильный диагноз, обязательно берут кусочек опухоли или увеличенного лимфатического узла для морфологического и иммуногистохимического исследования. Только после такого сложного комплексного анализа можно быть уверенным в диагнозе и провести эффективное лечение.
Для того чтобы точно узнать, есть ли увеличенные лимфатические узлы и каково их количество в тех частях тела, которые нельзя увидеть при внешнем осмотре, необходимо сделать компьютерную томографию грудной клетки, брюшной полости и малого таза. Стадию болезни устанавливают по системе «Ann-Arbor», которая показывает, какие органы и лимфатические узлы затронуты болезнью.
Для того чтобы точно узнать, есть ли увеличенные лимфатические узлы и каково их количество в тех частях тела, которые нельзя увидеть при внешнем осмотре, необходимо сделать компьютерную томографию грудной клетки, брюшной полости и малого таза. Стадию болезни устанавливают по системе «Ann-Arbor», которая показывает, какие органы и лимфатические узлы затронуты болезнью.
Лечение
Обычную диффузную В-крупноклеточную лимфому чаще всего начинают лечить по общепринятой схеме «СНОР», с добавлением лекарства «ритуксимаб». Как правило, проводят 6 курсов, но возможны варианты как по длительности, так и по выбору схемы лечения в зависимости от состояния здоровья пациента и особенностей болезни. Более редкие виды диффузной В-крупноклеточой лимфомы имеют свои особенности лечения. Между курсами, для оценки их эффективности, может потребоваться контрольная компьютерная томография. Если первое лечение не помогает, то терапией «второй линии» является высокодозная химиотерапия с поддержкой собственными стволовыми клетками.
Применение современных схем лечения позволяет полностью излечить около 75% пациентов.
Диффузная В-крупноклеточная лимфома
Диффузная В-крупноклеточная лимфома (ДБККЛ) — самый распространенный вариант злокачественного заболевания крови у взрослых.
Причины развития ДБККЛ
Причины развития заболевания на сегодняшний день неизвестны. ДБККЛ может возникнуть первично, как самостоятельное заболевание, или трансформироваться из хронического лимфолейкоза/лимфомы из малых лимфоцитов, фолликулярной лимфомы, лимфомы из клеток маргинальной зоны.
В норме в костном мозге из стволовых клеток-предшественников образуются незрелые В-лимфоциты, которые выходят в кровь, устремляются в лимфатические узлы, миндалины, селезенку, лимфатические образования тонкой кишки, где происходит их дальнейшее созревание, деление, дифференцировка, приобретается способность продуцировать антитела. При ДБККЛ вышеперечисленные процессы нарушаются вследствие спонтанной мутации гена, который контролирует жизненный цикл В-лимфоцитов. В результате образуется злокачественная опухоль.
Симптомы
К возможным симптомам заболевания относятся:
Диагностика
Диагностика ДБККЛ включает:
Лечение диффузной В-крупноклеточной лимфомы
Золотым стандартом терапии ДБККЛ, согласно международным и отечественным рекомендациям, является химиотерапия по схеме R-CHOP и R-miniCHOP для людей >80 лет. Схема включает следующие препараты: ритуксимаб, преднизолон, циклофосфан, доксорубицин, винкристин. В некоторых случаях могут использоваться другие схемы химиотерапии (например R-DA-EPOCH), а также лучевая терапия в дополнение к лекарственному лечению. Решение принимает лечащий врач совместно с пациентом и его близкими, исходя из индивидуальных особенностей пациента и его заболевания.
После 2–3 курсов проводится контрольное обследование, которое включает физикальный осмотр, оценку результатов анализов крови, компьютерную томографию или ПЭТ/КТ, исследование костного мозга при наличии данных за его поражение в дебюте заболевания.
При своевременном выявлении и лечении заболевания прогноз обнадеживает: у 80 % пациентов сохраняется ремиссия через 5 лет после завершения лечения. Считается, что через 5 лет вероятность развития рецидива значительно снижается.
Факторы неблагоприятного прогноза на момент установления диагноза:
70 % успеха лечения полностью зависят от компетентности старшего и среднего медицинского персонала, но 30 % успеха — это поддержка близких, продуктивный контакт, взаимное доверие и понимание между врачом и пациентом, соблюдение рекомендаций, своевременное посещение доктора.
Что такое диффузная крупноклеточная в клеточная лимфома
Диффузная В-клеточная крупноклеточная лимфома относится к агрессивному классу лимфом.
«В-клеточная», потому что состоит из заболевших В-клеток, а В-клетки (В-лимфоциты) – это клетки-следователи, они ищут и передают сообщения о клетках-чужаках другим членам иммунитета. Опорными пунктами иммунной системы являются лимфатические узлы, которые имеют свое строение и разделены на области. Каждая область лимфатического узла выполняет определенную работу. При диффузной В-крупноклеточной лимфоме строение лимфатического узла нарушено, опухолевые клетки находятся во всех областях, то есть диффузно, поэтому и лимфома называется «диффузной».
Одиночные лимфомные опухоли могут появляться в любой точке тела, хотя чаще при этой болезни увеличиваются лимфатические узлы группами на шее, подмышками, в паху и в других местах. Увеличенные узлы можно прощупать руками или найти с помощью рентгена и ультразвука (УЗИ). У больного могут появляться такие признаки болезни, которые называются «В-симптомы»: он быстро худеет, у него поднимается температура и появляется сильная потливость вечером и ночью. Диффузная В-клеточная крупноклеточная лимфома может возникнуть сама или ее могут вызвать другие лимфомы, которые развиваются в организме больного медленно, так называемые индолентные, вялотекущие лимфомы.
Существуют разные виды диффузной В-крупноклеточной лимфомы:
Диффузная В-клеточная крупноклеточная лимфома быстро нарастает, прогрессирует, но в целом хорошо поддается лечению.
Диагноз
Чтобы поставить правильный диагноз, обязательно берут кусочек опухоли или увеличенного лимфатического узла для морфологического и иммуногистохимического исследования. Только после такого сложного комплексного анализа можно быть уверенным в диагнозе и провести эффективное лечение.
Для того чтобы точно узнать, есть ли увеличенные лимфатические узлы и каково их количество в тех частях тела, которые нельзя увидеть при внешнем осмотре, необходимо сделать компьютерную томографию грудной клетки, брюшной полости и малого таза. Стадию болезни устанавливают по системе «Ann-Arbor», которая показывает, какие органы и лимфатические узлы затронуты болезнью.
Для того чтобы точно узнать, есть ли увеличенные лимфатические узлы и каково их количество в тех частях тела, которые нельзя увидеть при внешнем осмотре, необходимо сделать компьютерную томографию грудной клетки, брюшной полости и малого таза. Стадию болезни устанавливают по системе «Ann-Arbor», которая показывает, какие органы и лимфатические узлы затронуты болезнью.
Лечение
Обычную диффузную В-крупноклеточную лимфому чаще всего начинают лечить по общепринятой схеме «СНОР», с добавлением лекарства «ритуксимаб». Как правило, проводят 6 курсов, но возможны варианты как по длительности, так и по выбору схемы лечения в зависимости от состояния здоровья пациента и особенностей болезни. Более редкие виды диффузной В-крупноклеточой лимфомы имеют свои особенности лечения. Между курсами, для оценки их эффективности, может потребоваться контрольная компьютерная томография. Если первое лечение не помогает, то терапией «второй линии» является высокодозная химиотерапия с поддержкой собственными стволовыми клетками.
Применение современных схем лечения позволяет полностью излечить около 75% пациентов.
Диффузная В-крупноклеточная лимфома у взрослых. Клинические рекомендации.
Диффузная В-крупноклеточная лимфома у взрослых
Оглавление
Ключевые слова
клинические рекомендации 2016 г
Список сокращений
ДВКЛ – диффузная В-крупноклеточная лимфома
МРТ – магнитно-резонансная томография
УЗИ – ультразвуковое исследование
ЛТ – лучевая терапия
ВДХТ с аутоТГСК – высокодозная химиотерапия с последующей трасплантацией аутологичных гемопоэтических стволовых клеток.
ЦНС – центральная нервная система
ПЭТ – позитронно-эмиссионная томография
Термины и определения
Первичная медиастинальная В-крупноклеточная лимфома (ПМВКЛ) относится к первичным экстранодальным опухолям и происходит из В-клеток мозгового слоя вилочковой железы.
Диффузная В-крупноклеточная лимфома (ДВКЛ) является гетерогенной группой лимфатических опухолей с различными клиническими, морфологическими, иммунофенотипическими, цитогенетическими проявлениями и с разным ответом на терапию. Субстратом опухоли являются крупные В-лимфоидные клетки с выраженным атипизмом и полиморфизмом, с размером ядра в два и более раз превышающим размер ядра малого лимфоцита. Опухолевые клетки в большинстве случаев располагаются диффузно, но могут быть и разбросанными среди зрелых В-лимфоцитов, иногда на фоне Т-клеточного окружения, или формировать очаговые скопления 2.
Нодальная ДВКЛ – заболевание с первичным и преимущественным поражением лимфоузлов
Экстранодальная ДВКЛ – заболевание с первичным поражением любого органа, кроме лимфоузлов
1. Краткая информация
1.1 Определение
ДВКЛ является гетерогенной группой лимфатических опухолей с различными клиническими, морфологическими, иммунофенотипическими, цитогенетическими проявлениями и с разным ответом на терапию. Субстратом опухоли являются крупные В-лимфоидные клетки с выраженным атипизмом и полиморфизмом, с размером ядра в два и более раз превышающим размер ядра малого лимфоцита. Опухолевые клетки в большинстве случаев располагаются диффузно, но могут быть и разбросанными среди зрелых В-лимфоцитов, иногда на фоне Т-клеточного окружения, или формировать очаговые скопления.
1.2 Этиология и патогенез.
Патогенез ДВКЛ плохо изучен. Разнообразие клинических и морфологических проявлений ДВКЛ, иммунофенотипа позволяет предположить, что ДВКЛ является не единой нозологической формой, а группой лимфатических опухолей, имеющих близкий, но неодинаковый патогенез.
Это доказывают и молекулярно-цитогенетические исследования последних лет, позволившие выделить несколько вариантов ДВКЛ в зависимости от уровня дифференцировки опухолевых клеток, типов нарушения клеточных процессов, хромосомных аномалий [4].
В патогенезе ДВКЛ, вероятно, имеют значения многие гены, регулирующие события в зародышевых центрах, но изученным механизмом является перестройка гена Bcl-6, которая вызвана неправильным переключением класса иммуноглобулинов В-клеток в зародышевом центре. Ген Bcl-6 расположен в локусе 3q27 и экспрессируется исключительно В-клетками зародышевого центра.
В физиологических условиях ген Bcl-6 связывается с определенными регулирующими последовательностями ДНК, влияет на транскрипцию других генов, участвующих в В-клеточной активации и терминальной дифференцировке лимфоцитов. При перестройке локуса 3q27 происходит блок дальнейшей дифференцировки В-клеток в плазматические клетки, что приводит к бесконтрольной пролиферации В-клеток зародышевого центра.
1.3 Эпидемиология.
Диффузная В-крупноклеточная лимфома относится к наиболее распространенным вариантам лимфопролиферативных заболеваний взрослых (30-50% от всех неходжкинских лимфом). В возрасте до 18 лет частота этого варианта агрессивной В-клеточной опухоли не превышает 8-10%. Заболеваемость ДВКЛ составляет в среднем 4-5 на 100 000 населения в год. Риск развития опухоли увеличивается с возрастом и значительно выше у людей с серопозитивностью на вирус гепатита С, при наличии вируса иммунодефицита человека (ВИЧ), при аутоиммунных заболеваниях. Мужчины и женщины болеют ДВКЛ с приблизительно равной частотой [2].
1.4 Кодирование по МКБ 10 :
Что такое диффузная крупноклеточная в клеточная лимфома
Диффузная В-крупноклеточная лимфома (KILL): центробластная, иммунобластная; WF: диффузная крупноклеточная, крупноклеточная иммунобластная, плазмоцитоидная]
К диффузным крупноклеточным В-клеточным лимфомам относят крупноклеточные (бластные) лимфомы с весьма широким спектром клеточного состава опухолевой ткани.
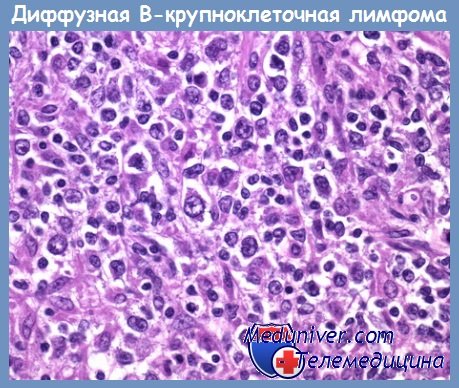
При преобладании в опухолевом инфильтрате крупных центрофолликулярных клеток — центробластов опухоль получила название центробластной лимфомы. Центробласт — крупная (в 3—4 раза превышающая по размеру малый лимфоцит) клетка с овально-округлым светлым ядром и 2—3 ядрышками, локализующимися у ядерной мембраны. Цитоплазма опухолевого центробласта разной степени пиронинофилии и базофилии.
Иммунобласт — бласттрансформированная клетка В-клеточной линии лимфопоэза. Для него характерно округлое пузырьковидное ядро с крупным центрально расположенным ядрышком. Ободок цитоплазмы широкий, обычно интенсивно пиронинофильный (базофильный). При иммунобластной лимфоме могут наблюдаться морфологические признаки плазмоцитарной дифференцировки.
При явном преобладании в опухолевой ткани центробластов или иммунобластов поставить диагноз несложно. В большинстве случаев даже разграничение лимфом на центробластные и иммунобласт-ные не так просто, так как в опухолевом инфильтрате могут присутствовать как одни, так и другие клетки.
Положение усугубляется тем, что при этой категории лимфом опухолевая ткань может иметь чрезвычайно «пестрый» клеточный состав за счет присутствия в инфильтрате того или иного количества клеток типа центробластоидных, занимающих по структуре промежуточное положение между центробластом и центроцитом, клеток с многодольчатыми ядрами (из трех и более долек), а также мелких лимфоидных клеток и гистиоцитов.
Встречаются случаи, когда в качестве реактивного компонента представлены Т-клетки, причем количество последних может быть весьма значительным (до 90 % от клеточного состава). Такая форма лимфомы получила название богатой Т-клетками В-крупноклеточной лимфомы. Помимо мелких, с неправильной формой ядер Т-клеток, встречаются гистиоциты, эозинофилы; в опухолевой ткани много сосудов, поэтому возникает необходимость дифференциальной диагностики с периферической Т-клеточной лимфомой.
Гистологическими дифференциальнодиагностическими критериями надо считать отсутствие переходных форм от мелких клеток к крупным бластным, а также преимущественно округло-овальную форму ядер последних (центробласт, иммунобласт), что, как правило, не свойственно Т-клеточным лимфомам.
В качестве отдельного подтипа крупноклеточной В-клеточной лимфомы выделяют вариант с первичной локализацией опухоли в средостении — медиастинальную (тимичсскую) В-крупноклеточную лимфому. Основанием для такого выделения послужили особенности клинической картины: заболевают молодые люди, чаще женщины, опухоль локальная (I— II стадия), часто пораждается тимус, рецидивы преимущественно экстранодальные.
Кроме того, необходимо учитывать морфологический субстрат. Последний характеризуется чрезвычайным клеточным полиморфизмом опухолевой ткани, связанным прежде всего с различной конфигурацией ядер опухолевых клеток, присутствием многоядерных форм. Цитоплазма опухолевых клеток обычно светлая, в опухолевой ткани могут встречаться тонкие коллагеновые волокна, окружающие группы клеток.
Первичная лимфома серозных оболочек (primary effusion lymphoma) — подтип диффузной крупноклеточной В-клеточной лимфомы выделен благодаря клиническому своеобразию, обусловленному локализацией опухолевого субстрата. Последний поражает серозные оболочки, не формируя узловатых масс. Болеют почти исключительно молодые мужчины, большинство из них ВИЧ-инфицированные.
Заболевание сопровождается выпотом в плевре, перикарде, асцитом. Серозные оболочки могут быть инфильтрированы как относительно мономорфными клетками типа иммунобластов, так и полиморфными крупными бластами с большим содержанием дву- и многоядерных форм.
Иммунофенотип диффузной В-крупноклеточной лимфомы: CD19+, CD20+, CD22+, CD79a+ (возможна потеря экспрессии одного или более панВ-маркеров), sIgM/cIgM > sIgG/cIgG > sIgA/cIgA в 50-75 % случаев; CD5+ до 10 % случаев, CD10+ в 25-50 % случаев, BCL-2+ в 30-50 % случаев, BCL-6+ более чем в 50 % случаев, 40— 90 % опухолевых клеток Ki-67-позитивные.
С учетом иммунофенотипических характеристик в настоящее время выделяют диффузные В-крупноклеточные лимфомы:
1) фолликулярного происхождения (CD10+ и/или BCL-6+);
2) из активированных клеток центра фолликула с экспрессией одного маркера фолликулярного происхождения и одного активационного маркера (CD138 или MUM 1);
3) из активированных нецентрофолликулярных клеток (MUM l+ и CD138+).
Диффузные В-крупноклеточные лимфомы 1-й группы относятся к лимфомам с благоприятным клиническим течением.
Цитологическая характеристика диффузной В-крупноклеточной лимфомы. В цитограмме определяются бластные клетки однотипной морфологии или сочетание различных субпопуляций. Клеточный состав может быть представлен следующими клетками:
1) центробластами;
2) иммунобластами. Иммунобласт — крупная бластная клетка (15—29 мкм) с равномерно-сетчатой структурой хроматина, одним крупным или одним — тремя небольшими ядрышками, расположенными в центральной зоне ядра, умеренно выраженной базофильной цитоплазмой. Могут присутствовать признаки плазмоцитарной дифференцировки;
3) бластными клетками с полиморфными, в частности многодольчатыми, ядрами с небольшими ядрышками;
4) плазмобластами — крупными клетками с обильной интенсивно базофильной цитоплазмой, содержащей просветление вокруг округлого ядра — околоядерное гало, с насыщенным хроматином и неотчетливыми ядрышками.
В каждой диффузной крупноклеточной В-клеточной лимфоме определяются в том или ином количестве макрофаги с выраженными признаками фагоцитоза, значительное количество разрушенных бластных клеток с нитями ядерного детрита, «голыми» ядрами. Характерна высокая клеточность материала, в качестве «фона» отмечается большое количество цитоплазматических глобул.
Для диффузной крупноклеточной В-клеточной лимфомы, богатой Т-клетками и/или гистиоцитами, характерны немногочисленные дискретно расположенные крупные опухолевые клетки с округло-овальными или многодольчатыми ядрами среди выраженного мелкоклеточного фона, представленного мелкими лимфоидными клетками без признаков атипии и/или гистиоцитами. Могут в различном количестве встречаться плазматические клетки, эозинофильные лейкоциты.
Дифференциальную диагностику диффузной В-крупноклеточной лимфомы проводят с помощью иммуногистохимического исследования с атипичным подвариантом лимфомы Беркитта, ангиоиммунобластной Т-клеточной лимфомой. Если отмечается выраженная плазмоцитарная дифференцировка, в дифференциально-диагностический ряд необходимо включать плазмоклеточную (плазмобластную) миелому.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021