Что такое бактериальная хромосома
Научная электронная библиотека
§ 3.1.4. Строение клетки
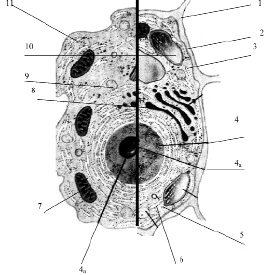
Размеры клетки широко варьируют от 0,1 мкм (некоторые бактерии) до 155 мм (яйцо страуса). У всех клеток, независимо от их формы, размеров, функциональной нагрузки обнаруживается сходное строение (рис. 3.13).
Рис. 3.13. Схема строения живой клетки: 1 – оболочка; 2 – мембрана; 3 – цитоплазма; 4 – ядро; 4а – ядрышко; 5 – рибосомы; 6 – эндоплазматическая сеть (ЭПС); 7 – митохондрии; 8 – комплекс гольджи; 9 – лизосомы; 10 – пластиды; 11 – клеточные включения
Снаружи клетка одета мембраной. Внутренняя часть клетки содержит многочисленные органоиды – структурные образования клетки, выполняющие определенные функции жизнедеятельности клетки.
1. Оболочка. Присутствует только у растительных клеток. Состоит из волокон целлюлозы. Функции оболочки: защита клетки от внешних повреждений, придает стабильную форму клетки, эластичность растительным тканям.
Повреждение наружной оболочки приводит к гибели клетки (цитолиз).
2. Мембрана. Тончайшая структура (75 Ǻ), состоит из двойного слоя молекул липидов и одного слоя белков. Такая структура обеспечивает уникальную эластичность и прочность мембране

Явление фагоцитоза – поглощение клеткой твердых частиц – впервые было описано русским врачом Мечниковым. Фагоцитарная особенность лежит в основе процесса иммунитета. Особенно развита у лейкоцитов, клеток костного мозга, лимфатических узлов, селезенки, надпочечников и гипофиза.
Пиноцитоз – поглощение клеткой растворов – состоит в том, что мельчайшие пузырьки жидкости втягиваются через образующуюся воронку, проникают через мембрану и усваиваются клеткой.
3. Цитоплазма – внутренняя среда клетки. Представляет собой гелеобразную жидкость (коллоидная система), состоит на 80 % из воды, в которой растворены белки, липиды, углеводы, неорганические вещества. Цитоплазма живой клетки находится в постоянном движении (циклоз).




4. Ядро – обязательный органоид эукариотических клеток. Впервые было исследовано и описано Р. Броуном в 1831 г. В молодых клетках расположено в центре клетки, в старых – смещается в сторону. Снаружи ядро окружено мембраной с крупными порами, способными пропускать крупные макромолекулы. Внутри ядро заполнено клеточным соком – кариоплазмой, основная часть ядра заполнена хроматином – ядерным веществом, содержащим ДНК и белок. Перед делением хроматин образует палочковидные хромосомы. Причём, хромосомы одинакового строения (но содержащие разные ДНК!) образуют пары, зрительно воспринимаемые как одно целое (рис. 3.14).
Рис. 3.14. Хромосомный набор человеческой клетки перед началом деления
Структурирование всех хромосом в пары свидетельствует о том, что число хромосом – чётное. Поэтому, его часто обозначают 2n, где n – количество хромосомных пар, а соответствующий набор хромосом называют диплоидным. Например, у голубей n = 40 (80 хромосом), у мухи n = 6 (12 хромосом), у собаки n = 39 (78 хромосом), у аскариды n = 1 (2 хромосомы). У человека n = 23 (46 хромосом). Однако, в половых клетках число хромосом в два раза меньше. Поэтому набор хромосом в половых клетках называется гаплоидным. Клетки, не являющиеся половыми называются соматическими. Иногда клетки с гаплоидным набором хромосом называют гаплоидными клетками, а с диплоидным набором хромосом – диплоидными клетками.
При слиянии двух родительских гаплоидных половых клеток образуется диплоидная клетка, дающая начало новому организму с набором генов отца и матери
Совокупность всех хромосом ядра (а значит и генов) клетки называется генотип. Именно генотип определяет все внешние и внутренние признаки конкретного организма.
В соматических клетках 44 Х-образные хромосомы (22 пары) у женщин и мужчин идентичны (сходны по строению), их называют аутосомами. А 23-я пара имеет конфигурацию ХХ – у женщин и ХY – у мужчин. Эти пары хромосом именуются половыми хромосомами.
В половых клетках 22 хромосомы также одинаковые у яйцеклеток и у сперматозоидов, а 23-я хромосома конфигурации Х – у яйцеклетки и Х или Y – у сперматозоидов. Поэтому при слиянии половых клеток и образовании пар хромосом, 23-я пара будет ( <ХY>или <ХХ>) определять пол будущего ребенка.
Необходимо помнить, что хотя в соматических клетках набор хромосом диплоидный (2n), однако, перед началом деления клеток происходит репликация ДНК, то есть, удвоение их количества, а, значит, и удвоение
количества хромосом. Поэтому перед началом деления соматической клетки в ней насчитывается 4n хромосом (рис. 16). Она становится тетраплоидной.
– хранение генетической информации;
– контроль за всеми процессами, происходящими в клетке: делением, дыханием, питанием и др.
4а. Ядрышко – структура, содержащаяся в ядре. Ядро может содержат 1, 2 или более ядрышек. Функция ядрышка – формирование рибосом.
Следует отметить, что не все клетки имеют оформленное ядро. Клетки, имеющие ядро называются эукариотическими или эукариотами. Клетки, не имеющие ядра, называются прокариотическими или прокариотами. Функции ядра у прокариот несёт одна нить ДНК (именуется хромосома), в которой хранится вся генетическая информация. К прокариотам относятся бактерии и сине-зеленые водоросли. Как правило, у прокариотов отсутствуют и некоторые другие органоиды. Размеры прокариотических клеток меньше, чем размеры эукариот.
5. Рибосомы – самые мелкие органоиды клетки. Были обнаружены в 1954 г. Французским ученым Паладом. Рибосомы были обнаружены в цитоплазме, а также на гранулярной ЭПС и в ядре.
Функция рибосом: обеспечение биосинтеза белка.
6. Эндоплазматическая сеть. Представляет собой каналы и полости, ограниченные мембраной. Различают две разновидности ЭПС: гранулярная ЭПС и агранулярная ЭПС. Гранулярная ЭПС морфологически отличается от агранулярной наличием на ее поверхности многочисленных рибосом (на агранулярной ЭПС рибосомы отсутствуют).
Функции эндоплазматической сети:
– участие в синтезе органических веществ: на гранулярной ЭПС синтезируются белки, на агранулярной – липиды и углеводы;
– транспортировка продуктов синтеза ко всем частям клетки.
Несложно уяснить, что гранулярная ЭПС характерна для клеток, синтезирующих белки (например клетки желез внутренней секреции), агранулярная ЭПС характерна для клеток-производителей углеводов и липидов (например клетки жировой ткани).
7. Митохондрии – крупные органоиды, состоящие из двойного слоя мембран: наружная – гладкая, внутренняя образует многочисленные гребнеобразные складки – кристы. Внутри митохондрии заполнены жидкостью (матрикс).
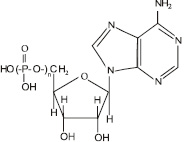
Функции митохондрий: основная функция митохондрий – обеспечение клетки энергией. Этот процесс происходит за счет синтеза аденозинтрифосфорной кислоты (АТФ) (рис. 3.15), в которой фрагмент
Рис. 3.15. Структурная формула аденозинфосфорных кислот. Для аденозинтрифосфорной кислоты n = 3, для аденозиндифосфорной кислоты n = 2, для аденозинмонофосфорной кислоты n = 1
При взаимодействии молекулы аденозинтрифосфорной кислоты с водой отщепляется один остаток фосфорной кислоты, в результате чего образуется аденозиндифосфорная кислота – АДФ и выделяется огромное количество энергии:
АТФ + Н2О = АДФ + Н3РО4 + 10 000 калорий.
Впоследствии от АДФ может отщепляться еще один остаток фосфорной кислоты, образуя АМФ – аденозинмонофосфорную кислоту.
АДФ + Н2О = АМФ + Н3РО4 + 10 000 калорий[37].
Освободившаяся энергия используется для жизнедеятельности клетки (КПД процесса превышает 80 %!).
Наряду с распадом АТФ и выделением энергии в клетке постоянно происходит синтез АТФ и накопление энергии (обратные реакции).
Количество митохондрий в клетке зависит от потребности последней в энергии. Так, в клетках кожи человека находится в среднем 5–6 митохондрий, в клетках мышц – до 1000, в клетках печени – до 2500!
8. Комплекс Гольджи. Итальянский ученый Гольджи обнаружил и описал структуру клетки, напоминающую стопки мембран, цистерны, пузырьки и трубочки. Расположена эта система чаще всего возле ядра.
Функции комплекса Гольджи: в полостях комплекса накапливаются всевозможные продукты обмена клетки, которые по каким-либо причинам не вывелись наружу. В последствии эти продукты могут быть использованы клеткой для процессов жизнедеятельности. Из пузырьков и цистерночек комплекса Гольджи в растительных клетках образуются вакуоли, заполненные клеточным соком.
9. Лизосомы – мелкие органоиды. Представляют собой пузырьки, окруженные мембраной. Внутри лизосомы заполнены пищеварительными ферментами (обнаружено 12 ферментов), которые расщепляют и переваривают крупные макромолекулы (белки, полисахариды, нуклеиновые кислоты).
Функции лизосом: растворение и переваривание макромолекул. Лизосомы участвуют в фагоцитозе. Понятно, что основная функция по перевариванию поступающих в клетку частиц принадлежит лизосомам.
10. Пластиды. Эти органоиды характерны только для растительных клеток. Форма напоминает двояковыпуклую линзу. Структура пластид напоминает таковую у митохондрий: двойной слой мембраны. Наружная – гладкая, внутренняя образует складки, называемые тилакоидами. На тилакоидах происходит основной жизненно важный для всех зеленых растений процесс – фотосинтез:
Пластиды бывают трех типов:
1) Хлоропласты – зеленые пластиды. Их цвет обусловлен наличием хлорофилла. Хлорофилл – основное вещество хлоропластов (имеет зеленый цвет). Только благодаря хлорофиллу возможен процесс фотосинтеза (см. раздел 4.2). Хлоропласты придают зеленый цвет растительным организмам.
2) Хромопласты – пластиды, имеющие различные окраски: от ярко-желтого до пурпурно-багряного. Наличие различных пигментов окрашивают плоды, цветки и осенние листья растений в соответствующие цвета. Этот факт особенно важен для привлечения насекомых к цветкам, как природный индикатор созревания плодов и др.
3) Лейкопласты – бесцветные пластиды, в которых происходит накопление запасных питательных веществ (например, крахмала).
Некоторые виды пластид могут переходить друг в друга: например, переход хлоропластов в хромопласты: созревание томатов, яблок, вишни, и т. д.; изменение окраски листьев в осенний период времени. Лейкопласты могут переходить в хлоропласты: позеленение картофеля на свету. Это доказывает общность происхождения пластид.
11. Клеточные включения. Вакуоли. Это непостоянные и необязательные составляющие клетки. Они могут появляться и исчезать в течение всей жизни клетки. К ним относятся капли жира, зерна крахмала и гликогена, кристаллы щавелево-кислого кальция и др. Жидкие продукты обмена называются клеточным соком и накапливаются они в вакуолях. В клеточном соке растворены сахара, минеральные соли, пигменты и т. д. Чем старше клетка, тем больше клеточного сока накапливает клетка. Молодые клетки практически не содержат вакуолей.
Помимо перечисленного некоторые специализированные клетки обладают специальными органоидами. К ним относятся:
– реснички и жгутики, представляющие собой выросты мембраны клетки, осуществляющие движения клетки. Они имеются у одноклеточных организмов и многоклеточных (кишечный эпителий, сперматозоиды, эпителий дыхательных путей);
– миофибриллы – тонкие нити мышечных клеток, участвующие в сокращении мышц;
– нейрофибриллы – органоиды, характерные для нервных клеток и участвующие в проведении нервных импульсов. Кроме того, в состав клеток входят центриоли – две (иногда более) цилиндрические структуры диаметром около 0,1 мкм и длиной 0,3 мкм. Место расположения центриолей в период между делениями клетки считается серединой клеточного центра. При делении клетки центриоли расходятся в противоположные стороны – к полюсам, определяя ориентацию веретена деления (рис. 16).
Следует иметь в виду, что, хотя животные и растительные клетки имеют много общего, но между ними существуют и серьёзные различия (табл. 3.1).
Более общая классификация клеток представлена на рис. 3.16.
Одно из основных отличий бактерий от архей, состоит в химическом составе мембраны. Бактерии отделены от внешней среды двойным слоем липидов (жиров и жироподобных веществ). Мембраны архей состоят из терпеновых спиртов.
Место бактериофагов в терапии инфекционных заболеваний желудочно-кишечного тракта
Место бактериофагов в терапии инфекционных заболеваний желудочно-кишечного тракта
Наиболее дискутабельным остается вопрос о целесообразности использования антимикробных препаратов (АМП) в лечении бактериальных ОКИ у детей. Назначая АМП в этих случаях, врач ожидает: уменьшения выраженности клинических симптомов, сокращения продолжительности заболевания, снижения частоты развития осложнений, прекращения выделения возбудителя, предупреждения дальнейшего распространения инфекции [4, 5].
В то же время доказано, что использование антибиотиков далеко не всегда является эффективным и безопасным при бактериальной диарее. Так, при энтерогеморрагическом эшерихиозе применение АМП приводит к массивному высвобождению шигаподобного токсина, следовательно, увеличивает риск развития гемолитико-уремического синдрома [6].
Назначение АМП при бактериальных диареях в значительном проценте случаев не только не приводит к санации макроорганизма от возбудителя, а, наоборот, способствует продолжительной персистенции бактериального агента в желудочно-кишечном тракте (ЖКТ) вследствие не только подавляющего влияния на аутохтонную микробиоту кишечника, но и прямого иммуносупрессивного действия [7, 8]. По данным отечественных и зарубежных исследователей, затяжное реконвалесцентное бактериовыделение сальмонелл формируется у значительного числа пациентов, получавших антибиотики в острую фазу инфекции, по сравнению с лицами, использующими исключительно
патогенетическую терапию [9, 10].
Экономический ущерб, наносимый возникновением антибиотикорезистентных форм бактерий, исчисляется десятками и сотнями миллионов долларов. Например, в странах Евросоюза он составляет как минимум 1,5 млрд. евро в год [11]. В сложившейся ситуации альтернативу АМП в терапии бактериальных диарей могут составить бактериофаги [12, 13].
Необходимо отметить, что в медицинском сообществе в настоящее время присутствует две полярные точки зрения на роль и место бактериофагов в терапии инфекционных заболеваний. Часть специалистов, ориентируясь на зарубежные протоколы и гадлайны, считают использование бактериофагов архаичным и небезопасным наследием прошлых десятилетий советской медицины; другие – широко применяют препараты фагов в своей клинической практике без каких-либо сомнений и при этом не опираются на исследования чувствительности и эффективности терапии.
Автору пришлось неоднократно беседовать с представителями обеих групп специалистов, и оказалось, что в большинстве случаев мало кто из них мог правильно ответить на вопрос, что представляют собой бактериофаги и каков их механизм действия. Бактериофаги – это вирусы, избирательно поражающие бактериальные клетки. В первую очередь необходимо понимать, что бактериофаги – это древние обитатели планеты и каждый грамм почвы, каждый кубический сантиметр воды и воздуха, продукты питания,
растения, животные содержат миллионы фаговых частиц (от 10 до 100 млн). Фаговые частицы в огромном количестве содержатся на кожных покровах, слизистых оболочках и в открытых полостях организма человека. Бактериофаги – самые вездесущие и наиболее распространенные существа на Земле, их насчитывают 1030–1032. Доказано, что бактериофаги играют важную роль в эволюции бактерий и реализации их патогенных свойств. Фаги способствуют формированию генетического разнообразия бактерий [14–16].
Выделяют вирулентные и умеренные бактериофаги. Вирулентные фаги: заражение бактерий ими всегда заканчивается разрушением бактерий и высвобождением зрелых фаговых частиц, готовых к поражению новых бактериальных клеток, – литический эффект. Умеренные бактериофаги: генетический материал фагов включается в хромосомы бактерий, такие фаги называются профагами и вызывают лизогенный эффект (лизогенную конверсию). Умеренные фаги интегрируются в бактериальную хромосому и размножаются синхронно с клеткой хозяина, не вызывая лизиса долгое время. Умеренные фаги могут переносить хозяйские гены (гены бактериальной клетки) от одной
бактериальной клетки к другой (фаговая трансдукция).
В настоящее время доказано, что множество факторов вирулентности у патогенных и условно-патогенных бактерий закодировано с помощью профаговых генов.
Так у Vibrio cholerae, Clostridium botulinum продукция токсинов обусловлена профагами [15, 16].
Бактериофаги – это высокоэффективные иммунобиологические препараты антимикробного действия, применяются для лечения и профилактики бактериальных инфекций, в том числе инфекций, связанных с оказанием медицинской помощи. Антимикробный эффект бактериофагов обусловлен внедрением фага в бактериальную клетку с последующим его размножением и лизисом инфицированной клетки. Вышедшие во внешнюю среду в результате лизиса бактериофаги повторно инфицируют и лизируют другие бактериальные клетки, действуя до полного уничтожения патогенных бактерий в очаге воспаления [14–17]. В настоящее время описано 13 семейств бактериофагов,
подразделенных более чем на 140 родов, содержащих более 5300 видов.
Бактериофаги широко применялись для лечения разных заболеваний с 1920-х годов как в СССР, так и зарубежных странах. Символично, что в 1930–1932 гг. Моррисон впервые применил массовую фаготерапию во время эпидемии холеры в Индии, затем долгие годы ученые считали, что с помощью бактериофагов можно управлять эпидемическим процессом при холере, однако эти мировоззрения оказались ошибочными [18].
Однако с 1940–1950-х годов производство и применение фагов на Западе практически прекратились. Препараты бактериофагов на сегодняшний день производятся лишь в России, Грузии и Польше. Однако в настоящее время интерес к бактериофагам возрождается во всем мире. Так, в 2006 г. Управление по контролю за продуктами и лекарствами Соединенных Штатов разрешило использование бактериофагов Listeria monocytogenes в качестве антимикробного компонента в сырах, а в 2007 г. – во всех готовых к употреблению продуктах. Препарат выпускается компанией Intralytix Inc. (США) и представляет собой смесь из шести фагов, активных в отношении L. monocytogenes. По инициативе этой же компании в 2008 г. была завершена I фаза клинических исследований препарата бактериофагов, содержащего восемь фагов, специфически лизирующих Pseudomonas aeruginosa, S. aureus и E. coli. Показана безопасность этого препарата при лечении венозных язв [18]. В августе 2009 г. корпорацией Nestlé Nutrition (Швейцария) в Бангладеш были инициированы клинические исследования по изучению безопасности и эффективности применения бактериофага E. coli в терапии ОКИ у детей в возрасте от 6 до 60 мес [19].
В настоящее время бактериофаги используются в качестве АМП при разных бактериальных инфекциях: желудочно-кишечного тракта (ЖКТ), ЛОР-органов, органа зрения, дыхательных путей, урогенитального тракта, генерализованных септических заболеваний, ожоговых ранах, хирургических инфекциях; для профилактики инфекций, связанных с оказанием медицинской помощи [20].
Фаги проникают через эпителиальные барьеры слизистых оболочек с помощью рецепторзависимого транспорта, активно осуществляемого специализированными клетками иммунной системы (М-клетками, бокаловидными) и, возможно, клетками эпителия кишечника и других отделов ЖКТ. Бактериофаг, введенный любым способом, поступает в общий ток крови, в крови не задерживается и адсорбируется тканями, оседая в первую очередь в лимфатических узлах, печени и селезенке. Выводится фаг из организма через кишечник и почки. После перорального приема фаговые частицы обнаруживаются через 1 ч в образцах крови, через 1–1,5 ч – на поверхности ожоговых ран и в бронхиальном содержимом, через 2 ч – в ликворе и моче. После однократного приема больными пациентами фаги выделялись с мочой в течение 5–6 сут с постепенным уменьшением титра. Гематоэнцефалический барьер не является барьером для проникновения фагов в центральную нервную систему. Необходимо отметить, что
скорость транслокации фагов, так же как и бактерий из ЖКТ в кровь, может существенно меняться в разных физиологических состояниях. При воспалительном ответе транслокация бактерий и, вероятно, фагов из кишечника значительно увеличивается [18].
Бактериофаги, используемые в составе лечебно-профилактических препаратов, должны иметь литический цикл развития (т.е. быть вирулентными), вследствие которого происходит гибель бактериальной клетки-мишени. По определенным участкам генов, кодирующим белок капсида бактериофага, можно быстро и с известной долей вероятности определить его принадлежность к семействам литических фагов.
В 1920–1940 гг. в Канаде и США бактериофаги широко использовались для лечения дизентерии, брюшного тифа и сальмонеллеза. Причем большинство исследователей показали их хорошую клиническую эффективность, в первую очередь снижение смертности на 30% и более по сравнению с группой сравнения [18].
Промышленное производство «кишечных» бактериофагов и их широкое использование в СССР были развернуты в 1940-е годы. Учитывая социально-экономические реалии того времени, большинство исследований посвящалось профилактике и лечению дизентерии. Следует отметить, что эффективность бактериофагов при ОКИ с давних пор изучалась и в ФГБУ НИИДИ ФМБА России. Изучение культур, выделенных от дизентерийных больных в бактериологической лаборатории НИИ детских инфекций под руководством профессора В.Н.Черновой, показало, что в 1968–1973 гг. бактериофагом лизировалось 98–99% выделенных культур шигелл Зонне, что подтверждало целесообразность его применения. Следующим этапом поиска рациональных методов лечения дизентерии явилось исследование эффективности новых форм дизентерийного поливалентного таблетированного бактериофага с ацидорезистентным покрытием и нетиповыми основаниями, синтезированного в Горьковском НИИ эпидемиологии и микробиологии (З.Н.Орлова) в 1969–1972 гг., ранее эффективность применения колипротейного и сальмонеллезного бактериофагов в свечах изучалась Б.М.Элинсон, И.Л.Гусарской (1965 г.).
Результаты лечения детей новыми формами бактериофагов были обобщены в кандидатской диссертации З.Н.Орловой «Эффективность лечения дизентерии у детей новой модификацией бактериофага с ацидорезистентным покрытием в сопоставлении с другими методами по клинико-иммунологическим данным» (1971 г.). Бактериофаги высокоспецифичны при лечении бактериальных инфекций, не вызывают развития резистентности микроорганизмов, являются самовоспроизводящимися организмами: ДНК бактериофага встраивается в хромосому бактерии, вследствие чего бактериальная клетка начинает продуцировать сотни бактериофагов, поражающих бактерии до их полного
уничтожения; бактериофаги в состоянии проникнуть глубоко в очаг инфекции. Они являются не только самовоспроизводящимися организмами, но и саморегулирующимися: когда все бактерии поражены бактериофагами, их количество, как и число бактериофагов, начинает уменьшаться. Бактериофаги оказывают стимулирующее действие на гуморальное и клеточное звенья иммунитета. В отсутствие бактерий, необходимых для размножения бактериофагов, последние быстро удаляются из организма [17, 18, 20, 21].
Традиционной формой выпуска бактериофагов является жидкий препарат (кроме таблетированных форм кишечных фагов), поэтому фаги используют для приема через рот, в виде клизм, аппликаций, орошений, введения в полости ран, вагины, носа, а также путем введения в дренированные полости – брюшную, плевральную, мочевого пузыря, почечной лоханки [18, 20].
Препараты бактериофагов при энтеральном и ректальном пути введения безопасны и нетоксичны для человека. Они не имеют противопоказаний к применению, кроме аллергических реакций, и могут быть использованы в сочетании с любыми другими лекарственными средствами. Препараты бактериофагов можно назначать беременным, кормящим матерям и детям, начиная с раннего возраста [17, 18, 20, 21]; они эффективны в монотерапии, но могут быть также использованы и в комбинации с антибиотиками [22]. Необходимо отметить, что в раннем детском возрасте (до 3–4 мес) использовать бактериофаги можно только по строгим показаниям, учитывая значимую частоту аллергических и диарейных побочных реакций у детей данной возрастной группы. Следует отметить, что побочные реакции в результате употребления фагов обычно связаны с массивным распадом бактериальных клеток с выделением эндотоксина под действием бактериофага. Нивелировать данные нежелательные явления можно при помощи включения в комплекс терапии энтеросорбентов. При использовании фагов в сочетании с терапевтическими дозами АМП отсутствует негативное воздействие
этих препаратов на развитие бактериофагов, но отмечается взаимное потенцирование их терапевтического эффекта. Установлено, что воздействие фагов на антибиотикоустойчивые штаммы бактерий может быть более активным по сравнению с воздействием на антибиотикочувствительные штаммы того же вида [18, 23].
Следовательно, показания к использованию бактериофагов при ОКИ можно сформулировать следующим образом:
• в качестве монотерапии – при стертых и легких формах инвазивных ОКИ;
• в сочетании с антибактериальной терапией или последовательно – при среднетяжелых и тяжелых формах ОКИ в период обратного развития симптомов;
• при бактериовыделении (у реконвалесцентных или транзиторных бактерионосителей);
• в комплексе терапии энтероколитов условно-патогенной и стафилококковой этиологии у детей раннего возраста;
• для коррекции нарушений микробиоценоза кишечника.
Дозы бактериофагов в зависимости от возраста приведены в табл. 1, 2. Бактериофаги назначаются 2–3 раза в сутки. Поскольку при приеме жидких препаратов бактериофагов перорально происходит частичная инактивация бактериофагов кислой средой желудка, целесообразно производить препараты бактериофагов в таблетках с кислотоустойчивыми капсулами и суппозиториях. В табл. 3 представлены бактериофаги, используемые в Российской Федерации для терапии и профилактики инфекционных диарей.
При острых кишечных инфекциях «кишечные» бактериофаги назначают в период разгара болезни (при наличии рвоты, фебрильной лихорадки, выраженного диарейного синдрома) наравне с основной этиотропной терапией [29]. В последние 10–15 лет в РФ большинство публикаций и научных исследований посвящено использованию сальмонеллезного бактериофага при реконвалесцентном бактериовыделении сальмонелл. Наши собственные исследования и исследования других авторов
свидетельствуют о высокой чувствительности циркулирующих штаммов сальмонелл к специфическому бактериофагу (82–96%) [24, 25].
Очень актуальным является исследование В.Г.Акимкина, посвященное купированию продолжительной нозокомиальной вспышки сальмонеллеза в Главном военном клиническом госпитале им. Н.Н.Бурденко, с использованием адаптированного сальмонеллезного бактериофага как в виде монотерапии, так и в комплексе с АМП фторхинолонового ряда [13, 26]. Таким образом, практика использования лечебнопрофилактических бактериофагов показала необходимость осуществления бактериологического мониторинга за возможными изменениями фаголизабильности по отношению к выделяемым культурам сальмонелл в стационаре. Доказано, что регулярная передача на производство свежевыделенных штаммов возбудителей ОКИ способствует повышению литической активности и расширению диапазона действия препаратов бактериофагов [26–28].
Применение бактериофагов по эпидемиологическим показаниям при ОКИ
Бактериофаги находят свое применение и с профилактической целью при чрезвычайных ситуациях природного характера (наводнения и т.д.), в очагах бактериальной инфекции, в первую очередь шигеллеза, сальмонеллеза и брюшного тифа, заболеваний, вызванных условно-патогенными возбудителями (протеем, синегнойной палочкой) [20].
В эпидемических очагах (шигеллеза, сальмонеллеза) бактериофаги применяют для фагирования детей, посещающих детские дошкольные учреждения, и работников пищевых предприятий, водопроводных и коммунальных сооружений и др. Фагирование всех общавшихся с источником ОКИ проводят при неблагоприятных санитарных условиях в очаге, а также при оставлении больного на дому. В качестве профилактики препараты фагов принимают ежедневно в виде разовой возрастной дозы: детям в возрасте от 1 года до 3-х лет – по 1 таблетке; от 3–8 лет – по 2 таблетки; взрослым – по 3 таблетки. Продолжительность приема как правило определяется
условиями эпидситуации.
Если необходимо давать жидкий бактериофаг (шигеллезный, сальмонеллезный или интести-бактериофаг), то пересчет следующий: 1 таблетка сухого бактериофага равна 20 мл жидкого фага. До приема жидкого бактериофага желательно выпить щелочной минеральной воды («Боржоми», «Ессентуки» и т.д.). Противопоказаний к применению бактериофага не имеется. Применение бактериофагов с профилактической целью хорошо зарекомендовало себя во время чрезвычайных ситуаций последних лет: наводнения в Крымске (2012 г.), паводка на Дальнем Востоке (2013 г.).
Наука не стоит на месте: создаются и внедряются новые препараты лечебно-профилактических фагов: разработаны бактериофаги против серраций и энтеробактеров, ведутся работы по созданию фаговых препаратов против Acinetobacter spp. и Helicobacter pylori [17]. Исторически сложилось так, что СССР занимал лидирующие позиции в области производства и применения лечебно-профилактических бактериофагов. Так, на филиалах ФГУП НПО «Микроген» Минздрава России в городах Уфа, Пермь и Нижний Новгород бактериофаги производятся с 1940-х годов. Препараты бактериофагов (производства ФГУП НПО «Микроген») постоянно обогащаются новыми фаговыми
клонами, что позволяет им соответствовать современным циркулирующим штаммам. Препараты бактериофагов являются высокостабильными и могут
храниться в течение длительного периода. Необходимо заметить, что только бактериофаги производства ФГУП НПО «Микроген» являются лекарственными средствами.
Успехи фаготерапии в разных отраслях медицины – это не наследие советской медицины, а доказанные научные явления, нашедшее широкое применение в практическом здравоохранении стран мира. Одним из самых перспективных направлений является изучение возможностей функционирования бактериофагов в биопленках, а следовательно, дальнейшие возможности профилактики и лечения инфекций, связанных с оказанием медицинской помощи.