Для чего вирусу нужны оболочечные белки вич
Гены и белки ВИЧ
Первая открытая рамка кодирует внутренние белки вириона. Эти белки вместе с белками, кодируемыми геном pol, прочитываются, как и у других ретровирусов, с полноразмерной РНК в 9300 нуклеотидов. В результате трансляции этой иРНК образуется предшественник с мол. Массой 55 кД. В процессе дальнейшего протеолитического расщепления этот белок нарезается на p17, p24, p9 и р7. Согласно наблюдениям, в сыворотках больных СПИД обнаруживаются антитела ко всем этим продуктам. Значительную фракцию составляют антитела к р24 — основному внутреннему белку вириона. Антитела к р24 обычно появляются на ранних стадиях заболевания и часто исчезают по мере его прогрессирования.
Pol. Как и у других ретровирусов, кодируемые этим геном белки считываются в виде gag-pol предшественника. Поскольку рамка считывания гена pol не совпадает с рамкой gag, при созревании иРНКpol должно происходить удаление небольшого интрона, сдвигающее рамку считывания. Анализ первичной нуклеотидной последовательности области перекрывания генов gag и pol выявляет присутствие там нескольких участков, которые могут выполнять функцию акцепторных сайтов сплайсинга. Другим механизмом совмещения рамок считывания является так называемый «перескок рамки» при трансляции. В результате рибосомы «перепрыгивают» через стоп-кодон, ограничивающий рамку gag, и прочитывают pol уже в правильной рамке считывания. Подобный механизм описан для некоторых ретровирусов.
Ген pol кодирует 3 фермента: протеазу (р22), обратную транскриптазу (р64/53) и эндонуклеазу (р31). Эти белки образуются в результате протеолитического расщепления предшественника с молю массой 150кД. Несмотря на относительно небольшое количество этих белков в вирионе (примерно 2 молекулы на вирион), антитела к ним выявляются в сыворотках больных СПИДом. Наиболее ярко выражена реакция с р31.
Env. и РНК, кодирующая белки оболочки вириона, образуется в результате сплайсинга, приводящего к удалению из геномной РНК большого интрона, содержащего гены gag, pol и sor. Образующаяся иРНК размером 4300 нуклеотида содержит открытую рамку с типичным инициирующим AUG, которая может направлять синтез белка, состоящего из 861 аминокислотного остатка с мол. массой 97.5 кД. Этот белок предшественник в дальнейшем обильно гликозилируется, в результате чего его мол. масса возрастает до 160 кД. Предшественник содержит 3 гидрофобные области, характерные для оболочечных белков других ретровирусов. Первый гидрофобный участок (с 17-й по 31-ю аминокислоты) соответствует сигнальному пептиду, второй находится в районе сайта протеолитического расщепления белка-предшественника, третий является частью трансмембранного белка. В результате протеолитического расщепления образуется 2 сильно гликозилированных белка: наружный белок оболочки gp120 и трансмембранный белок gp41. Интересной особенностью трансмембранного белка является наличие необычно длинной последовательности (длиной в 150 аминокислотных остатков) гидрофильных аминокислот вслед за гидрофобной частью трансмембранного белка. Эта последовательность, по-видимому, является внутриклеточным фрагментом gp41. Еще, как показали исследования, правильный процессинг gp160 происходит не во всех клеточных линиях. От чего это зависит, пока неизвестно.
3`-orf. Эта открытая рамка расположена между 8347-м и 8992-м нуклеотидами и простирается, таким образом, в U3 область 3`-LTR. Кодируемый этим геном белок имеет мол. массу 27 кД и транслируется со сплайсированной иРНК размером 1800 нуклеотидов.
Хотя антитела к этому белку удается выявить в крови больных СПИДом, он не является абсолютно необходимым для репликации вируса. Продукт 3`-orf оказывает влияние на цитопатогенность вируса.
Tat-3. Явление трансактивации было впервые описано для ретровирусов человека HTLV-1 и HTLV-2. Белок, осуществляющий функцию трансактивации, кодируется у этих вирусов небольшой открытой рамкой, расположенной на 3`-конце генома после гена env. Механизм его действия заключается в активации транскрипции структурных генов вируса, вследствие чего ген, кодирующий белок-трансактиватор, был назван tat (transactivator of transcription).
Феномен трансактивации выражен у ВИЧ на несколько порядков сильнее, чем у HTLV-1 и HTLV-2. Как сейчас стало ясно, за этот процесс у ВИЧ отвечают по крайней мере, 2 гена: tat-3 и art (trs). Первый из них кодируется иРНК размером около 2000 нуклеотидов, образующейся в результате сложного сплайсинга. Механизм действия белка tat-3 у ВИЧ значительно сложнее, чем у аналогичных белков tat вирусов HTLV-1 и HTLV-2.
Продукт гена tat-3 — белок с мол. массой 14 кД, выявляемый с помощью сывороток больных СПИД. Мутации в 5`-области первого кодирующего экзона tat-3 нарушают способность вируса синтезировать структурные белки и реплицироваться. Эти мутации могут быть комплементированы в клеточных линиях, постоянно экспрессирующих tat-3 белок. Сейчас получены линии как В- так и Т-лимфоцитов, стабильно трансформированных tat-3 геном и продуцирующих белок-трансактиватор. Другие клеточные линии, например HeLa, продуцирующие функциональный tat-3 белок, также могут поддерживать размножение мутантного по tat-3 ВИЧ. Использование подобных клеточных линий и клонированных провирусных ДНК, содержащих различного размера делеции в tat-3 гене, позволило изучить механизмы действия кодируемого этим геном белка.
Art (trs). Другим белком, участвующим в регуляции экспрессии структурных генов ВИЧ является продукт гена art (antirepression transactivator — антирепрессорный трансактиватор). Транслируется он, по-видимому, с иРНК, принадлежащей к тому же классу молекул размером 2000 нуклеотидов, что и иРНКtat-3. Кодирующие экзоны гена art перекрываются экзонамиtat-3, а при сплайсинге используются те же акцепторные и донорные сайты. Однако при трансляции art функционирует инициаторный AUG с координатой 5500, а не 5412, как для гена tat-3. В результате, art читается со сдвигом рамки отностительно tat-3, что приводит к уменьшению ее кодирующей рамки в первом транслируемом экзоне с 214 до 76 нуклеотидов и к увеличению во втором с 44 до 271 нуклеотида. Синтезируемый белок состоит из 116 аминокислотных остатков, причем основная доля приходится на аминокислоты, проявляющие основные свойства. Подобные белки обладают сродством к нуклеиновым кислотам и часто регулируют экспрессию генов.
Действие продукта art осуществляется на посттранскрипционном уровне. По-видимому, он активирует трансляцию иРНК структурных генов gag и env, снимая действие специфических негативных регуляторов. Наряду с этим продукт art участвует и в регуляции сплайсинга РНК, в связи с чем для указанного гена было предложено другое название — trs (transregulator of splicing — трансрегулятор сплайсинга).
СПИД: как ВИЧ разрушает нашу иммунную систему
СПИД: как ВИЧ разрушает нашу иммунную систему
Распространенность СПИДа в мире на 2009 год.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: СПИД это болезнь иммунной системы, вызываемая вирусом иммунодефицита человека (ВИЧ). При СПИДе у человека медленно, но верно (в течение нескольких лет) развивается тотальный иммунодефицит, когда организм не может справиться почти ни с какими микробами (даже теми, которые никогда не заражают здорового человека). Так как иммунитет борется не только с микробами, но и с раковыми клетками, еще у заболевшего СПИДом резко повышается вероятность заработать рак. ВИЧ использует изощренные механизмы обхода и уничтожения нашей иммунной системы, всегда идя на шаг впереди нее.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучший обзор».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система
Для того чтобы разобраться, как вирус иммунодефицита человека (а именно так расшифровывается ВИЧ) разрушает иммунную систему, нужно прежде всего понять, что же это такое — иммунная система. Согласно одному из определений (по Р.В. Петрову), иммунитет — это способ защиты организма от живых тел и веществ, несущих в себе признаки генетической чужеродности. Проще говоря, иммунитет — это то, что защищает нас от бактерий, вирусов, любых высокомолекулярных чужеродных веществ (вспомним иммунитет против змеиного яда), попавших в организм, а также раковых клеток. В его основе лежат фагоциты (у животных называемые макрофагами), собственно уничтожающие (поглощающие) чужеродные тела, а также Т- и В-клетки иммунитета, осуществляющие точное «наведение» фагоцитов на патоген. При проникновении микроба в организм фагоциты его поглощают и переваривают [29].
Первичное распознавание врага происходит при помощи Toll-like рецепторов, или TLR [30]. Эти молекулы распознают структуры, общие для многих классов патогенов, но отсутствующие у человека (к примеру, TLR5 распознает белок флагеллин — главный компонент жгутиков бактерий, — а TLR3 активируется при наличии двухцепочечной РНК, появляющейся в жизненном цикле многих вирусов, в частности вируса гриппа А). После поглощения микроба его остатки «показываются» (презентируются) Т-хелперам. Т-хелперы активируются, и в свою очередь помогают активироваться B-лимфоцитам (последним для активации нужны молекулы патогена и сигналы активации от Т-хелпера). После этого B-лимфоциты превращаются в плазматические клетки и начинают синтез антител — молекул иммунитета, маркирующих вещества, подобные тем, что активировали B-лимфоциты. Антитела циркулируют в кровотоке и маркируют структуры патогена. Маркированные микробы и другие чужеродные тела поглощаются фагоцитами более эффективно.
Такой «сценарий» работает, когда микроб находится вне клеток организма (в случае заражения большинством бактерий и грибов). Если же враг проникает внутрь клетки (вирусы, некоторые бактерии, простейшие), а также когда враждебной становится сама клетка организма (в случае рака), в дело вступают Т-киллеры. Они находят и уничтожают зараженные клетки, после чего остатки этих клеток поглощаются все теми же фагоцитами. Для активации Т-киллерам требуются Т-хелперы. Помимо Т-киллеров в этом «сценарии» участвуют антитела (и, соответственно, B-лимфоциты), но их роль меньше, чем T-киллеров. Разумеется, в иммунитете есть и другие участники, но основной акцент в борьбе с ВИЧ приходится на тех, что были названы выше.
Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Рассмотрим жизненный цикл ВИЧ (см. видео). Первая стадия — это проникновение вируса. Сначала любой вирус должен как-нибудь «зацепиться» за клетку, и у разных вирусов для этой цели есть разные «якоря». Имеется таковой и у ВИЧ — белок gp120, который способен взаимодействовать с белком СD4 поверхности человеческой клетки. Это рецептор, присутствующий на многих клетках организма, но больше всего его на Т-хелперах (другое их название — СD4 + T-лимфоциты), — именно на них и направлен ВИЧ в первую очередь. При первоначальном связывании gp120 с CD4 вирусный белок изменяет свою форму и связывается с другими белками поверхности клетки — СХСR4 и ССR5, после чего происходит погружение другого вирусного белка — gp41 — в мембрану клетки. Вслед за этим оболочки клетки и вируса сливаются, и наследственный материал вируса попадает в цитоплазму клетки.
Видео. Жизненный цикл ВИЧ.
Нормальная функция СХСR4 и ССR5 — рецепция цитокинов (небольших растворимых молекул иммунной системы, посредством которых клетки иммунитета «общаются» друг с другом и другими клетками организма). Именно с мутацией ССR5 (Δ32 CCR5) связана врожденная устойчивость некоторых людей, гомозиготных (имеющих 2 копии мутированного CCR5) по этому гену, к ВИЧ [12], [18] (таких людей до 2% в Европе, Индии и странах Ближнего Востока [13]). К сожалению, эта устойчивость не является полной [3]; есть штаммы, заражающие и таких людей. Зато она в какой-то степени проявляется даже у гетерозигот (имеющих одну копию мутированного и одну копию обычного ССR5 ) [12], [18].
После проникновения наследственного материала ВИЧ в клетку происходит процесс обратной транскрипции, то есть перенос информации с вирусной РНК на ДНК. Происходит это потому, что вирусный геном записан в виде РНК, а геном человека — в виде ДНК. Вирусу же «хочется» записать себя в геном клетки, ведь именно он управляет последней. К тому же, если иммунитет имеет средства для распознавания вирусных белков и РНК, то ДНК, интегрированную в геном клетки, иммунитет распознать не может.
Обратная транскрипция осуществляется вирусным белком обратной транскриптазой [31]. Обратная она потому, что обычно в клетке все наоборот — информация переносится с ДНК на РНК (а с РНК — в последовательность аминокислот белков). РНК по сравнению с ДНК очень нестабильна, и поэтому для ВИЧ характерна огромная скорость мутации — в десятки тысяч раз быстрее, чем для человека. Если скорость нейтральных мутаций для ДНК составляет у различных видов и для различных генов в среднем меньше 10 −9 замен на сайт в год, то скорость мутирования генетического материала РНК-вирусов — около 10 −3 замен на сайт в год (у гена env ВИЧ: 10 −2 –10 −3 замен на сайт в год [21]). Это одна из причин, почему иммунная система не может справиться с ВИЧ — он слишком быстро изменяется.
«Будильником» для вируса служит активация клетки: промотор вируса содержит последовательность, гомологичную последовательности NF-κB [10], [15], каковая есть у многих генов иммунитета. (Промотор регулирует работу гена и определяет, как, когда и в каких количествах будет появляться белок в той или иной клетке.) Вспоминая о том, что ВИЧ заражает в основном Т-хелперы, мы получаем интересную картину: пока клетка не активирована, вирус «спит»; как только клетка начинает выполнять свою функцию (иммунитет) — вирус «просыпается» и убивает эту клетку. Можно также добавить, что при ВИЧ-инфекции активируются в первую очередь те клоны Т-клеток, которые специфичны для ВИЧ-белков.
Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
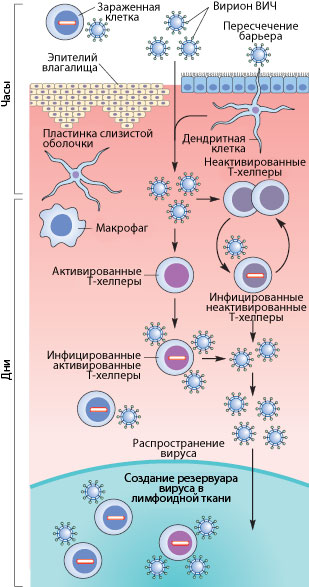
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Но даже в отсутствии микротравм ВИЧ может проникнуть внутрь организма через дендритные клетки (разновидности макрофагов), которые могут выпускать свои отростки в просвет слизистой. Там они захватывают вирусы и бактерии, после чего происходит презентация захваченного материала Т-хелперам. Таким образом организм готовится «тепло встретить» микробов, присутствующих в окружающей среде. Но в нашем случае, дендритные клетки лишь заражаются вирусом — напрямую свободными вирионами или же при контакте с зараженными лимфоцитами, которые могут присутствовать в сперме (общее число лимфоцитов в сперме — до 1 млн/мл и больше).
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
О том, как вести себя, чтобы не заразиться ВИЧ, и что делать, если это все-таки произошло, читайте в статье «Связанные одной лентой» [33]. — Ред.
Заключение
На данный момент имеется огромное количество информации о ВИЧ; известны его структура, последовательность генома, жизненный цикл; изучен почти каждый шаг вируса в организме. Уже сейчас на стадии клинических испытаний находится множество лекарственных средств, а ВААРТ (высокоактивная антиретровирусная терапия) позволяет зараженному ВИЧ иметь почти такую же продолжительность жизни, как у здорового человека. Науке известно и два случая полного излечения от ВИЧ. Один из них известен как случай «берлинского пациента», которому пересадили костный мозг от донора с мутацией Δ32 ССR5. Другой прецедент произошел в США, где ребенка, родившегося от ВИЧ-инфицированной матери, сразу после рождения подвергли ВААРТ. Через два года после рождения девочки мать отказалась продолжать ее лечение, и через 10 месяцев при повторном осмотре врачи констатировали полное выздоровление девочки.
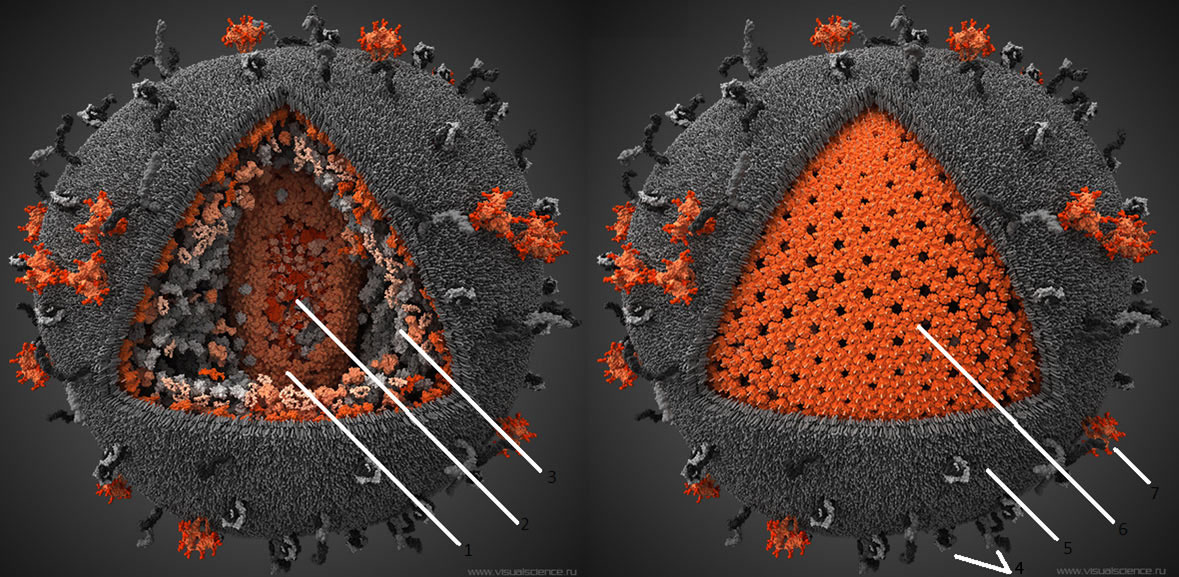
Рисунок 4. Компьютерная модель ВИЧ. Серым цветом показаны человеческие структуры, «украденные вирусом из клетки», красным — вирус-специфические белки. 1 — капсид вируса, состоит из 250 гексамеров и 12 пентамеров белка p24. 2 — Геном вируса, а также связанные с ним белки, представлен двумя идентичными молекулами РНК по
10000 нуклеотидов в каждой. Всего геном включает девять генов, которые в результате альтернативного сплайсинга кодируют 15 различных белков. 3 — Различные белки, захваченные вирусом из хозяйской клетки. 4 — Человеческие белки, обычно находящиеся на поверхности мембраны клеток. Захваченые в результате отпочковывания, они увеличивают вирулентность вируса. 5 — Внешняя оболочка ВИЧ, ведущая свое происхождение от цитоплазматической мембраны клетки, от которой когда-то отпочковался вирион. 6 — Матрикс, образованный тримерами белка р17. 7 — Тримерные комплексы белков gp120 и gp41, при помощи которых вирус проникает в клетку. На поверхности среднего вириона насчитывается около 20 таких тримеров. Чтобы увидеть рисунок в полном размере, нажмите на него.
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.
Что такое ВИЧ
Вирус иммунодефицита человека (ВИЧ) отнесен к семейству ретровирусов (Retroviridae), подсемейству медленных вирусов (Lentivirus).
В настоящее время описаны 2 серотипа вируса: ВИЧ-1 и ВИЧ-2, различающиеся по структурным и антигенным характеристикам. Наибольшее эпидемиологическое значение имеет ВИЧ-1, который доминирует в современной пандемии и имеет наибольшее распространение на территории Российской Федерации. По данным электронной микроскопии, вирионы ВИЧ имеют округлую форму диаметром 100-120 нм. Наружная мембрана вируса построена из белков клетки хозяина и пронизана собственными белками вируса, которые обозначены как оболочечные белки.
Таблица 1. Группы белков ВИЧ-1 и ВИЧ-2
Нуклеоид вируса имеет округлую форму, но принимает продолговатую после отпочковывания вирусной частицы от клетки. Оболочка нуклеотида содержит протеин с молекулярной массой 24кд (р24). Между наружной оболочкой вириона и нуклеоидом существует каркас, состоящий из матриксного белка 17кд (р17).
В геноме ВИЧ выделены гены: env, pol, gag, отвечающие соответственно за продукцию белков оболочки, ферментов, ядерных структур и некоторые другие гены: tat, rev, vif, vpr, vpu, nef. В зависимости от строения отдельного фрагмента гена env в последнее время стали выделять «субтипы», обозначаемые заглавными буквами латинского алфавита А-Н, О и т.д.
Нагревание до температуры 56°С в течение 30 мин приводит к снижению инфекционного титра вируса в 100 раз, при 70°- 80°С вирус гибнет через 10 мин; через 1 мин инактивируется 70% этиловым спиртом, 0,5% раствором гипохлорита натрия, 1% глутаральдегидом, 6% перекисью водорода. ВИЧ относительно мало чувствителен к УФ-облучению, ионизирующей радиации.
Гликопротеин gр120 обусловливает присоединение ВИЧ к рецепторам СD4 клеток человека. При попадании ВИЧ в клетку под действием обратной транскриптазы синтезируется ДНК ВИЧ, встраиваемая в ДНК клетки-хозяина, которая в дальнейшем начинает продуцировать вирусные частицы.
Адаптивный иммунитет основан на свойствах Т- и В-лимфоцитов избирательно отвечать на чужеродные вещества (антигены) с образованием специфической памяти и продукцией антител.
Таблица 3. Типы клеток, поражаемых ВИЧ
| Тип клеток | Ткани и органы |
| Т-лимфоциты, макрофаги | Кровь |
| Клетки Лангерганса | Кожа |
| Фолликулярные дендритные клетки | Лимфоузлы |
| Альвеолярные макрофаги | Легкие |
| пителиальные клетки | Толстая кишка, почки |
| Клетки шейки матки | Шейка матки |
| Клетки олигодендроглии, астроциты | Мозг |
В начальных стадиях болезни в организме вырабатываются вируснейтрализующие антитела, которые подавляют свободно циркулирующие вирусы, но не действуют на вирусы, находящиеся в клетках (провирусы). С течением времени (обычно после 5-6 лет) защитные возможности иммунной системы истощаются, происходит накопление свободных вирусов в крови (возрастает т.н. «вирусная нагрузка»).
Оппортунистические инфекции, как правило, имеют эндогенное происхождение и возникают за счет активации собственной микрофлоры человека вследствие снижения напряженности иммунитета (например, эндогенная активация микобактерий туберкулеза из очагов Гона).
Цитопатическое действие ВИЧ приводит к поражению клеток крови, нервной, сердечно-сосудистой, костно-мышечной, эндокринной и других систем, что определяет развитие полиорганной недостаточности, характеризующейся разнообразием клинических проявлений и неуклонным прогрессированием ВИЧ-инфекции.