Для чего используется карбид
Что такое карбид. Свойства карбида. Применение карбида
Забава детства. Так многие вспоминают о карбиде, особенно бывшие мальчишки, а ныне, конечно, взрослые мужчины.
Они брали камешки на строительных рынках. Покупать не покупали, а так, таскали с развалов и из кузовов грузовиков.
Любовались и белесыми пузырями, которые карбид давал, попадая в лужи. Однако, кому обязаны таким весельем, сорванцы прошлых лет, зачастую не знали.
Что такое карбид? Попробуем ответить на вопрос, кажущийся неважным в детстве.
Что такое карбид
Карбит – не конкретное вещество, а группа соединений элементов с углеродом. Последний должен быть более электроотрицательным, чем «сосед».
Это обязательное условие, исключающее из ряда карбидов галогениды и оксиды углерода.
Под электроотрицательностью понимается способность атома сдвигать к себе электроны других веществ.
Электротрицательность углерода равна 2,6. Это данные шкалы Полинга. Она выстроена с учетом, что ионность в ковалентной связи делает эту связь прочнее.
Получается, электротрицательность вторых элементов в карбидах должна быть меньше 2,6.
Большинство подходящих элементов – металлы. Но, около 15% карбидов их не содержат.
Есть и цветные дуэты с углеродом, к примеру, карбид железа. Это всем знакомый цемент. Окрас у соединения серый.
Получается, свойства карбидов могут разниться. Несовпадения рассмотрим в главе «Виды». Пока же, изучим общие характеристики класса соединений.
Свойства карбида
Особенно отличились карбиды переходных металлов. Это элементы побочных подгрупп периодической системы. У всех переходных металлов есть электроны на d- и f-орбиталях.
Обобщает карбиды и высокая температура плавления. Как правило, она выше, чем у входящего в соединение металла.
Если он из переходных, размягчение может начинаться лишь при 3000 градусов Цельсия.
Интересно, что температура плавления поднимается вместе с номером группы, к коей принадлежит «сосед» углерода.
Где карбид можно понять по структуре соединений. Их решетки, зачастую, дефектны.
Это значит, есть отклонения от теоретической схемы, разрывы и смещения. Именно поэтому свойства карбидов могут в 100, а то и 1000 раз разниться с высчитанными по формулам.
Виды карбидов
Основных видов карбидов три. Первый – ковалентные соединения. Валентность – предрасположенность к определенному числу химических связей.
Ковалентная связь – это перекрытие валентных облаков разных элементов. То есть, у них образуются общие электронные пары. Именно такие лежат в основе ковалентных карбидов.
В итоге, карбиды группы трудно расплавить, — решетка не хочет рушиться. Прочность связи делает оба соединения твердыми.
Карбид кремния алмаз не «побеждает», но свои достойные 8 баллов по шкале Мооса имеет.
Второй вид карбидов – ионный. Его, так же, именуют солеобразным. Все образованны металлами 1-ой и 2-ой групп таблицы Менделеева.
В класс включен и карбид алюминия. Соединения группы разлагаются не только кислотами, но и водой.
При реакции ионных карбидов с водой выделяется водород. В жидкости формируется и выпадает в осадок гидроксид металла.
Реакция протекает бурно. Резкий выброс на поверхность воды водорода и дает то самое пузырение.
Третий вид карбидов – ионно-ковалентно-металлические, попросту, металлоподобные.
Такие соединения формируются элементами 4-ой, 5-ой, 6-ой, 7-ой групп периодической системы. Исключения: — карбиды никеля, кобальта и железа.
Если у ковалентных карбидов химическая активность низкая, а у ионных – высокая, то у третьего вида соединений она средняя.
Примечательно строение молекул. Их основа – атомы металла. Атомы же углерода находятся в пустотах между ними.
Поэтому, к примеру, карбид вольфрама называют внедренным. Имеется в виду, что углерод внедрился в кристаллическую решетку металла.
Такое строение обеспечивает рекордную прочность и высокую температуру плавления. Еще одно известное соединение группы – карбид титана.
Применение карбида
Карбид титана стал основой безвольфрамовых, но столь же твердых сплавов.
К тому же, соединение служит покрытием инструментария, в основном, промышленного и строительного.
Такое напыление сводит к минимуму износ деталей и позволяет обрабатывать ими даже самые твердые материалы.
Карбид кальция нужен при сварочных работах. Из соединения получают ацетилен. Карбид служит его источником, а заодно, и топливом для машин кислородной сварки.
Ацетилен – газ. Одного его достаточно для работы аппаратов. Но, есть еще и вода. Карбид кальция вступает с ней в бурную реакцию.
Итог – не только пузырьки, нравящиеся детям, но и обилие тепла – еще одного источника энергии.
Карбид бора применяют в качестве огнеупора. Температура плавления соединения составляет почти 2500 градусов.
Прочность карбида позволяет добавлять его в бронежилеты. Защитить материал способен не только от пуль, но и радиации.
Поэтому, один из ответов на вопрос, где взять карбид бора, — в защитных экранах, задерживающих излучение.
Список карбидов и их роли в жизни общества может занять многие страницы. Соединений несколько десятков и у каждого из них есть применение, причем, не одно. Нет и единственной схемы получения карбидов.
Придется ограничиться общими фразами. Однако, и в них есть толика полезной информации.
Получение карбидов
Большинство карбидов именно получают, а не добывают. Первый синтез проведен в начале 19-го столетия.
Он оказался неустойчивым, в отличие от третьего синтезированного соединения углерода с железом.
Смотря на опытные образцы, ученые не могли понять, где найти карбид за пределами лабораторий.
Минералы, в которых металлы соединены с углеродом открыли лишь в начале 20-го века.
Судя по дате открытия карбидных минералов, они не являются распространенными.
Поэтому, в промышленных масштабах героев статьи до сих пор синтезируют. Масса карбида может получиться, к примеру, из древесного угля и оксидов металлов.
Цена карбида
Карбид кальция купить предлагают примерно за 40-90 рублей за килограмм. Соединение углерода с бором стоит от 100-та рублей за кило.
Купить карбид кремния предлагают примерно по 160 рублей за 1000 граммов.
А вот за кило карбида гафния придется выложить около 21 000 рублей, причем, при оптовых закупках.
То есть, стоимость материала во многом зависит от присутствующего в нем металла, или неметалла. Существует даже карбид золота.
Он, кстати, способен взорваться при простом пересыпании порошка. Так что, даже за большую цену, доставить сырье потребителю – задача не из легких.
Что такое карбид кальция для сварки

Карбид кальция в сварке
Для сварочных работ карбид является чуть ли не идеальным веществом, потому что при взаимодействии с водой выделяет в окружающее пространство летучий газ ацетилен, который служит основой металлизации, напайки, кислородной сварки и множества иных процессов, относящихся к обработке металлических сплавов.

Так как при воздействии воды карбид выделяет большое количество ацетиленового газа и тепловой энергии, это существенно затрудняет его хранение. Чтобы избежать порчи вещества, его нередко укладывают в герметичные стальные резервуары. При открытии этих металлических сосудов необходимо избегать открытого пламени и искр, иначе могут быть печальные последствия.
Карбидная пыль (частички до 2 мм) непригодна для применения, потому что растворяется в воде практически моментально. Кроме того, при хранении большого количества пыли увеличивается риск, что применение состава в итоге приведет к взрыву резервуара. Специалисты отмечают, что килограмм рассматриваемого вещества способен выделить при взаимодействии с водой более 260 кубических дюймов ацетилена.
Карбид часто используется для газовой резки и сварки. При горении ацетилен контактирует с кислородом и достигает температуры 3150, что делает этот газ совершенно незаменимым при обработке тугоплавких металлических сплавов. В целях безопасности ацетилен делают в особых генераторах на основе угля, нефти, природного газа или карбида кальция.
Особенности применения
В сварке это вещество используют везде. Делают это по следующей схеме:
Карбид при сварочных работах выполняет функции топлива, насыщающего генератор газа. И без его применения будет трудно применять ацетиленовую горелку. Ведь газовый баллон очень нелегко перемещать. А карбидные кусочки достаточно положить в герметичный сосуд и транспортировать на совершенно любые расстояния, предотвратив появление влаги.
Требования безопасности
В связи с тем, что это опасный материал, работать с ним нужно, строго соблюдая правила безопасности. Основные правила, которые обязательно должны выполнять при сварке с помощью карбида:
Соблюдая эти правила, можно безопасно пользоваться карбидом для сварки. Кроме того, это вещество позволяет сэкономить и сократить расход ацетилена.
Карбид кальция: свойства и применение. Получение ацетилена
Карбиды – это группа неорганических соединений углерода с металлами, а также с кремнием или бором (поскольку эти элементы проявляют металлические свойства). Карбид кальция – одно из наиболее востребованных веществ этой группы. О свойствах и применении соединения читайте ниже.
История получения
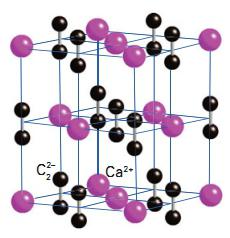
Карбид кальция – соединение, получившее широкое применение в современной промышленности. В 1862 году немецкий химик Фридрих Велер впервые синтезировал молекулу этого вещества. Получение карбида кальция он осуществил следующим образом. Ученый приготовил расплав кальция с цинком, а затем нагрел его с углем. В результате получился карбид. Химическая формула соединения – CaC2. Промышленный способ получения карбида предложил ученый Муассан в 1892 году. Другие названия вещества – ацетиленид кальция, или углеродистый кальций. Кристаллическая решетка соединения выглядит следующим образом:
Физические свойства
По своим физическим свойствам карбид кальция является кристаллическим веществом с температурой плавления 2300 о С. Эта цифра является справедливой лишь для чистого соединения. Карбид, содержащий примеси, может иметь другие показатели температуры плавления. Основное агрегатное состояние вещества – твердое, а цвет варьирует от серого до коричневого.
Химические свойства
Карбид кальция хорошо впитывает воду. Этот процесс сопровождается химической реакцией разложения. Важно, что карбидная пыль обладает раздражающим действием на слизистые оболочки, кожу и органы дыхания. Поэтому во время работы с соединением необходимо использовать противогазы либо противопылевые респираторы. С кислородом карбид кальция взаимодействует при высокой температуре с образованием карбоната кальция. Реакция с азотом приводит к синтезу цианамида кальция. Также при высоких температурах карбид кальция вступает в реакции соединения с хлором, фосфором, мышьяком. Но все-таки одним из важнейших свойств соединения считается разложение водой.
Получение
Производство карбида кальция заключается в следующем. Негашеную известь и предварительно измельченный кокс смешивают. Полученную смесь подвергают расплавлению в электрических печах. Кокс и оксид кальция берутся в равных по массе частях. Процесс происходит при температуре 1900 о С. Расплав выходит из печи и в дальнейшем разливается по специальным формам. Затем уже затвердевший карбид кальция дробят и сортируют по размеру кусков. Гранулы вещества разделяются на четыре фракции в соответствии с их размерами: 25×80, 15×25, 8×15, 2×8, которые определяются ГОСТом 1460-56. По своему составу технический карбид кальция содержит 75-80% основного вещества. На долю примесей, таких, как углерод, известь и других, приходится до 25% от общей массы полученной смеси. Кроме того, содержащийся в техническом карбиде сульфид и фосфид кальция обусловливают довольно неприятный его запах. Представим реакцию получения СаС2: СаО + 3С → СаС2 + СО↑. Образование ацетиленида кальция сопровождается поглощением тепла. Поэтому логично предположить, что реакция его разложения, напротив, идет с выделением энергии.
Транспортировка и хранение
По причине того, что влага моментально разлагает карбид с выделением большого количества тепла и образованием взрывоопасного газа ацетилена, хранить вещество необходимо в герметично закупоренных барабанах или бидонах. Следует помнить, что ацетилен легче воздуха и способен скапливаться в верхних зонах помещения. Этот газ, помимо наркотического действия, обладает способностью к самовоспламенению. Поэтому использовать карбид кальция необходимо с большой осторожностью. Расфасовке на производстве уделяется особое внимание. Готовое вещество помещается в специальные барабаны (тара, напоминающая консервные банки). Такая упаковка требует аккуратного вскрытия. При этом должен использоваться инструмент, не приводящий к образованию искр (молоток или специальный нож). В случае попадания карбида на кожу или слизистые оболочки необходимо немедленно промыть пораженный участок водой и обработать место вазелином или жирным кремом. Транспортировка соединения осуществляется с использованием только крытых видов транспорта. Воздушная доставка карбида запрещена. Помещения, где хранится СаС2, должны быть хорошо проветриваемыми. Также не разрешается хранить карбид совместно с другими химическими веществами. Это может привести к нежелательным, а, возможно, и опасным, реакциям. Срок хранения карбида составляет полгода.
Применение
Область применения карбида кальция чрезвычайно широка. В первую очередь это промышленный синтез. Карбид кальция используется для производства синтетического каучука, уксусной кислоты, ацетона, этилена, винилхлорида, стирола. Также он находит применение в получении цианамида кальция. Это вещество ценно своим использованием в синтезе различных удобрений и цианистых веществ. В сельском хозяйстве любому агроному известно такое название, как карбидно-карбамидный регулятор. Он применяется для регуляции роста растений. А для его получения также используется карбид кальция. Кроме того, это соединение находит применение в процессе производства цианамида кальция. Эта реакция основана на нагревании карбида кальция с азотом. Восстановление щелочных металлов также не обходится без применения описываемого нами вещества. Карбид кальция применяется и в процессе газосварки. Например, широко используются карбидные лампы. Принцип их работы основан на взаимодействии в специальной емкости карбида с водой и сгорании на выходе из аппарата конечного вещества реакции – ацетилена. Посмотрите на фото карбидной лампы.
Производство ацетилена
Одной из важнейших областей применения карбида кальция является его использование в получении ацетилена. Заслуга в открытии этого способа также принадлежит немецкому ученому-химику Фридриху Велеру. В основе этого промышленного процесса лежит реакция разложения карбида под воздействием воды. СаС2 + 2 Н2О → С2Н2 + Са(ОН)2↓. На выходе образуется газ ацетилен и гашеная известь, выпадающая в осадок. Процесс сопровождается выделением большого количества тепла. Объем газа на выходе зависит от того, насколько чистый используется для реакции карбид кальция. Ацетилен, образующийся в результате, может иметь различный объем – 1 кг исходного вещества может дать от 235 до 290 литров газа. Что касается скорости протекания реакции, то она зависит как от малого процента примесей в карбиде кальция, так и от температуры воды, а также ее чистоты. Если рассматривать теоретическую реакцию производства ацетилена из карбида, то в ней на 1 кг карбида достаточно 560 мл воды. Однако на практике объем воды для проведения реакции увеличивается. На 1 кг карбида кальция в условиях промышленного синтеза требуется от 5 до 20 литров воды. Такое количество необходимо для того, чтобы ацетилен лучше охлаждался, а также для обеспечения оптимальной безопасности при работе. Ниже изображен немецкий химик Фридрих Велер.
Лабораторный опыт получения ацетилена
Многим из школьных уроков химии знакома реакция взаимодействия карбида с водой. Обычно этот опыт позволяет продемонстрировать реакцию получения ацетилена, а также физические и химические его свойства. Процесс выделения газа при этом происходит достаточно бурно, поэтому трубка, отводящая ацетилен из колбы с действующими веществами, помещается в чашу с водой. Это обеспечивает менее активное и стремительное движение газа. Кроме того, в лабораторных условиях можно использовать и другой способ, чтобы сделать не слишком бурной реакцию разложения такого соединения, как карбид. Ацетилен при этом идет равномерно и спокойно. Для этого вместо воды необходимо взять насыщенный раствор поваренной соли. Также в лаборатории при проведении этой реакции следует осторожно добавлять воду в карбид, помещенный в объемную колбу, а не наоборот.
Для чего используется карбид
Ваша корзина пуста, для оформления заказа выберите товар в каталоге
Доставка продукции осуществляется компанией ХИМОПТТОРГ во все регионы Центральной России:
Карбид кальция: применение и меры безопасности
Определение
– химические соединения которые получаеются в результате щелочных реакций углерода с металлами. В большинстве случаев получаются сверхтвердые сплавы, сравнимые по своим твердостным характеристикам с алмазом.
Сейчас небольшой экскурс в историю возникновения этого химического соединения.
Коротко об истории
Томас Уилсон и Фердинанд Муассан, действуя обособленно, практически единовременно разработали способ выпуска карбида кальция в электрической плавильной печи. Это открытие стало толчком для запуска индустрии получения технического карбида кальция.
Технология
В производстве карбида кальция участвуют два элемента: оксид кальция (CaO) известный также как негашеная известь и углеродные соединения в виде кокса (антрацита, каменного угля):
CaO + 3C = CaC2 +CO
Оба компонента подвергаются измельчению и последующему обжигу и расплавлению посредством электродугового способа.
Готовый раствор доходит до твердого состояния в специальных формах, а впоследствии подвергается дроблению и сортировке.
| Содержание СаС2 в техническом карбиде, % | 78 | 74 | 69 | 63 | 60 | 56 |
| Н/м³(Удельный вес) технического карбида | 2,3 | 2,35 | 2,4 | 2,43 | 2,48 | 2,5/td> |
| Элемент | Процентное содержание от массы |
| Карбид кальция | 72 |
| Известь | 17 |
| Углерод | 1 |
| Окись магния | 0,3 |
| Сера | 0,3 |
| Железо и аллюминий | 2,6 |
| Кремний | 2 |
| Другие компоненты | 4 |
Минимальный температурный порог образования карбида кальция 1619°С. Как правило, процесс производства ведется при 1900-1950°С. Температурный рост приведет к распаду карбида кальция на металл и углерод.
При наличии небольшой электродуговой печи и источника тока можно воспроизвести процесс образования карбида кальция:
Можно выделить ряд факторов, влияющих на быстроту формирования и качественные характеристики конечного продукта:
Несмотря на модернизацию промышленных процессов, производство карбида кальция остается трудозатратным, требующим больших площадей и финансовых вложений.
Особенности
Складирование и перевозка
Карбид кальция нужно фасовать во влагозащищенных емкостях, резервуарах, чтобы исключить доступ влаги и не допустить процесса распада. Процедуре расфасовки и распаковки стоит уделить особое внимание
Полезные стороны
Агрегация карбида кальция и азота используется в получении цианамида кальция.
Он относится к нитратным стимуляторам, активно используемым в агрономии. Эта соль становится исходным компонентом при синтезе мочевины, гуанидина.
В металлургии служит для раскисления металлов и десульфурации (понижение содержания кислорода и серы соответственно).
А какую забаву вызывало у детей похитить со стройки камушек карбида и бросать в лужи, любуясь шипением и бурлением. А особо смелые подносили спичку к исходившему газу, и загоралось голубое пламя.
Полезный газ
Изначально карбид кальция применялся исключительно для получения ацетилена. Это органическое соединение использовали для создания карбидных ламп, применяемых для освещения улиц. Такие источники света используют и сегодня в спелеологии, как походное снаряжение, на маяках.
Ацетилен – полупрозрачный, водорастворимый газ используется для получения таких органических соединений, как хлорэтан, поливинилхлорид, стирол.
Существует ряд синтетических продуктов, производных ацетилена. Например, комбинации с хлором дают продукты, превосходно растворяющие органические соединения, а также неорганические: серу, фосфор. Поскольку такие продукты являются негорючими, они успешно используются при вытяжке жиров. Ацетилениды кальция (соли ацетилена) с ионами серебра, меди и ртути используются в создании взрывчатых веществ. Особенно сильной разрушающей взрывной силой обладает соединение с золотом.
В функционировании реактивных двигателей участвует коктейль ацетилена и аммиака.
Ацетилен в соединении с H2O образует ацетальдегид, из которого изготавливается синтетическая уксусная кислота, ацетон, искусственные смолы и этиловый или водочный спирт
Всем известные клей ПВА, грампластинки, рекламные баннеры также являются производными этого газа.
Техника безопасности
Как уже отмечалось ранее, карбид кальций – это взрывоопасное вещество и для соблюдения безопасности в работе с ним нужно следовать нескольким обязательным условиям:
– источник производства многих органических и неорганических соединений, которые широко используются в разных сферах жизни человека. Многие из них не имеют аналогов. Но, наряду с неисчерпаемой пользой этого вещества, не стоит забывать и о вреде, который он может нанести человечеству и экологии, ведь он относится к первому классу опасности, обладает взрыво и пожароопасными действиями.