Диспепсия беременных что это такое симптомы
Диспепсия беременных что это такое симптомы
Расстройства верхнего отдела пищеварительного канала (ВОПК) являются наиболее частыми осложнениями беременности. У ряда женщин развиваются расстройства ВОПК, возникающие только при беременности. Другие же женщины страдают хроническими заболеваниями ВОПК еще до беременности, требующими специального рассмотрения при наступившей беременности. Понимание механизмов клинических проявлений и распространенности различных расстройств ВОПК при беременности необходимо для оптимизации помощи этим больным.
Рассматриваемые ниже заболевания ВОПК объединены не только близостью анатомического расположения, но и тесной этиопатогенетической связью. По этой причине заболевания ВОПК имеют общие клинические симптомы, диагностические признаки и сходные подходы к лечению, нередко сочетаются и даже переходят друг в друга.
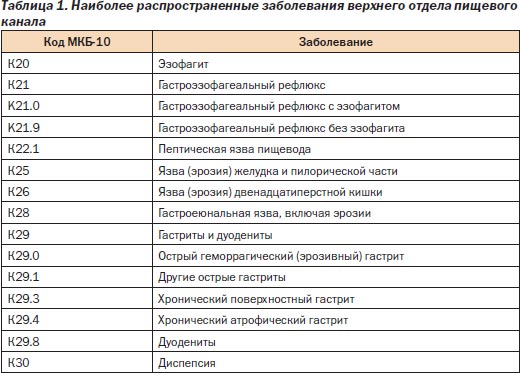
Унификация клинических классификаций в гастроэнтерологии остается одной из нерешенных проблем в Украине. Важную объединяющую роль играет международная статистическая классификация болезней десятого пересмотра (МКБ-10), основные рубрики которой, относящиеся к рассматриваемым вопросам, представлены в табл. 1.
В случаях если заболевания ВОПК действительно осложняют беременность и являются признаком гестоза, то они могут шифроваться с индексом «О»: O99.6 Болезни органов пищеварения, осложняющие беременность, деторождение и послеродовой период.
Обследование беременных женщин с патологией ВОПК
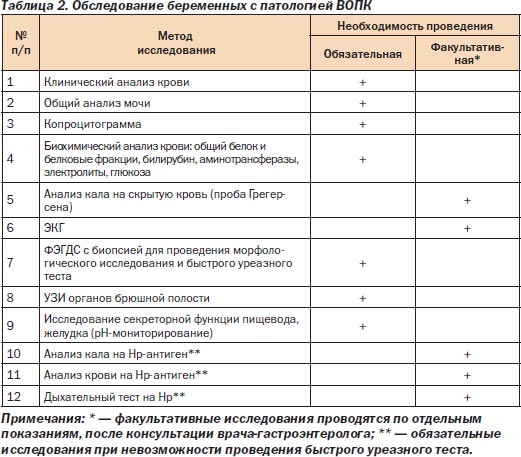
Методы исследования, используемые при всех заболеваниях ВОПК, сходны (табл. 2). Однако при отдельных заболеваниях значимость исследований (обязательная, факультативная) может меняться.
Рентгеноскопия пищевода и желудка беременным противопоказана.
Эрадикация Helicobacter рylori (Нр) согласно Маастрихтским консенсусам II-2000 и III-2005 у беременных не проводится, в связи с этим установление факта инфицирования имеет чисто академический интерес.
Решение вопроса о проведении эрадикации Нр должно быть поставлено (обязательно!) после родоразрешения и окончания периода кормления грудью.
Установление окончательного диагноза ВОПК должно быть подтверждено морфологически. Абсолютных противопоказаний к фиброэзофагогастродуоденоскопии (ФЭГДС) нет.
Относительные противопоказания к ФЭГДС:
1. Тяжелые нарушения сердечного ритма.
2. Острая фаза инфаркта миокарда.
4. Частые приступы стенокардии и бронхиальной астмы.
5. Сердечная недостаточность IIБ-III ст.
6. Атлантоаксиальный подвывих.
7. Эпилептические припадки.
8. Коагулопатия (время кровотечения > 10 мин).
При проведении ФЭГДС обязательно выполняются биопсии для проведения быстрого уреазного теста и гистологического исследования.
Исследование секреторной функции желудка
Проводится по показаниям, но при отсутствии раннего токсикоза.
В настоящее время существует три основных метода определения кислотообразующей функции желудка:
1. Внутрижелудочная рН-метрия.
2. Фракционное исследование желудочного сока с помощью тонкого зонда с применением стимуляторов желудочной секреции (в Европе и США запрещено).
3. Беззондовые методы — определение кислотности с помощью ионообменных смол («Ацидотест»). Беззондовые методы малоинформативны и в настоящее время применяются редко.
При хроническом Нр-гастрите секреторная функция желудка может быть изменена, но выраженность изменений зависит от стадии гастрита. При антральном гастрите (ранняя стадия) кислотообразовательная и пепсинообразовательная функции в норме или (чаще) повышены; при пангастрите (поздняя стадия) — снижены, но состояния ахлоргидрии, как правило, не бывает.
У беременных фракционное исследование желудочного сока не рекомендуется, а беззондовые методы не проводятся.
— кратковременная (до 3 ч);
— продолжительная (24 ч, мониторинг);
— с использованием радиокапсул;
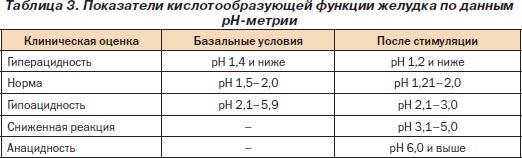
Метод основан на электрохимическом способе измерения рН. Степень кислотности или щелочности растворов выражается концентрацией в них активных ионов водорода (Н+) в единицах рН. РН является логарифмом активных Н+ в водном растворе, взятым с обратным знаком (табл. 3).
Кратковременная рН-метрия — наиболее широко используемый метод. Зонды диаметром 7 мм вводятся через инструментальный канал эндоскопа перорально или трансназально.
Показания и противопоказания такие, как для ФЭГДС.
Для стимуляции желудочной секреции у беременных возможно использование только пероральных завтраков.
Тошнота и рвота беременных
Тошнота с рвотой или без нее характерна для раннего периода беременности. Тошнота отмечается у 50–90 % беременных и вызывает жалобы и беспокойство у 25–50 % беременных. Чаще встречается, если плод женского пола.
Патофизиология данного состояния является предметом обсуждения. Это может быть проявлением гормональной перестройки и моторных расстройств ЖКТ в сочетании с психосоциальными факторами. Основное значение имеет эволюционная защита плода в период эмбриогенеза от вредных субстанций, содержащихся в пище, таких как микроорганизмы в мясных продуктах и токсины в растениях. Это подтверждается значительно меньшим числом выкидышей и мертворождаемости у женщин с тошнотой в ранний период беременности.
Клинические проявления
Тошнота при беременности, обычно кратковременная и самокупирующаяся, встречается у 91 % женщин в І триместре. Тошнота обычно начинается на 9–10-й неделе беременности (редко с 6-й), достигает пика на 11–13-й неделе и прекращается на 12–14-й неделе. У 1–10 % беременных симптомы сохраняются до 20–22-й недели беременности.
В мягкой форме она известна как «утренняя болезнь беременных», обычно возникает по утрам и не беспокоит женщин в течение дня.
Для тошноты и рвоты беременных характерна гиперсаливация.
При тошноте и рвоте беременных возможны:
— повышенная утомляемость, слабость, головокружение;
— ухудшение (искажение, извращение) вкуса;
— невозможность концентрации внимания.
При установлении диагноза необходимо исключить заболевания ЖКТ, эндокринной, мочевой и нервной системы, а также аллергические реакции (на пищевые продукты, производственные аллергены, медикаменты и другие вещества).
Персистирование тошноты и рвоты во ІІ и ІІІ триместре должно быть немедленно рассмотрено как возможный признак других состояний и заболеваний:
— гастроэзофагеальной рефлюксной болезни;
— язвенной болезни (ЯБ) желудка и двенадцатиперстной кишки;
— инфекций мочевыводящей системы;
— многоводия.
Лечение
Лечение тошноты у беременных зависит от выраженности симптомов.
При легком (мягком) течении лечение должно включать немедикаментозные воздействия: ободрение, прогулки на свежем воздухе, выявление и исключение провоцирующих факторов, изменение характера и режима питания (уменьшение объема и увеличение частоты приема пищи).
Устранение провоцирующих внешних факторов, в том числе и производственных (беременная нуждается в освобождении от работы).
Диета
Рекомендуется частое, дробное питание, увеличение приема углеводов и ограничение жиров. Отдых после приема пищи.
Прием пищи начинается с питья чистой воды комнатной температуры (0,5–1 стакан). В дальнейшем диета расширяется за счет крахмалсодержащих продуктов (кисель), затем крекеров и картофеля (печеного, вареного).
Беременным следует придерживаться следующих основных рекомендаций:
— есть при появлении чувства голода;
— есть часто и малыми порциями;
— избегать жира, специй;
— избегать пищи с неприятным запахом и вкусом (для беременной);
— исключить прием препаратов железа;
— использовать высокобелковые (мясные) завтраки;
— употреблять напитки, обогащенные углеводами (сладкие);
— употреблять напитки, бульоны, крекеры, а также желатин и замороженные десерты;
— настои трав (чаи): мята перечная или кудрявая, имбирь, лист малины.
Беременной следует объяснить, что фитопрепараты — это тоже лекарства и употребление их в больших количествах небезопасно.
Так, имбирь, являющийся безопасным и эффективным препаратом при тошноте и рвоте беременных, в дозах более 20,0 г/сут (сухого корня) может обладать мутагенными свойствами и относиться к категории С (FDA).
В тяжелых случаях возможно энтеральное питание (назогастральный зонд).
При среднетяжелом и упорном течении тошноты и рвоты в дополнение к общим мероприятиям могут быть назначены противорвотные препараты.
Возможно также использование психорелаксации, акупрессуры и гипноза.
Прогноз для матери и плода благоприятный.Более того, женщины с легкой степенью тошноты и рвоты имеют лучшие исходы беременности по сравнению с женщинами, не имеющими этих симптомов.
Чрезмерная рвота беременных
Встречается с частотой 3–10 случаев на 1000 беременностей. Чаще у городского населения.
Чрезмерная рвота беременных (Hyperemesis gravidarum) (ЧРБ) — рвота, осложняющая течение беременности, то есть относящаяся к ее осложнениям. Чрезмерная рвота беременных характеризуется упорной (неукротимой) тошнотой и рвотой в ранний период беременности и ведет к нарушениям водного и электролитного баланса,кетозу иснижению массы тела.
ЧРБ в отличие от тошноты и рвоты беременных беспокоит женщин не только по утрам, но и в течение дня. ЧРБ развивается примерно у 2 % беременных с тошнотой и рвотой беременных.
ЧРБ является проявлением гестоза и кодируется с индексом «О».
O21 Чрезмерная рвота беременных
O21.0 Рвота беременных легкая или умеренная
O21.1 Чрезмерная или тяжелая рвота беременных с нарушениями обмена веществ
O21.2 Поздняя рвота беременных
O21.8 Другие формы рвоты, осложняющей беременность
O21.9 Рвота беременных неуточненная
ЧРБ обычно впервые диагностируется в начале І триместра, с 4-й по 10-ю неделю. Симптоматика может сохраняться до 18–20-й недели.
Для ЧРБ характерны:
— снижение массы тела ≥ 5 % от исходной;
— недостаточное питание (malnutrition), проявляющееся симптомами полигиповитаминоза;
— кетоз, гипокалиемия, кислотно-щелочной дисбаланс;
— повышение уровней ферментов печени (трансаминазы, щелочная фосфатаза);
Факторами риска ЧРБ являются:
— хронические заболевания, сопровождающиеся нарушением трофики тканей и пониженным питанием;
— возрастные первородящие (старше 30 лет);
— низкий образовательный и социальный уровень беременной;
— тошнота и рвота беременных в период предыдущей беременности.
Дополнительными факторами риска также являются предшествующие беременности заболевания и состояния:
— заболевания щитовидной железы;
Несвоевременное и/или неадекватное лечение ЧРБ может приводить к осложнениям, таким как:
— разрыв и перфорация пищевода;
Другие осложнения (менее значимые):
— глубокий венозный тромбоз;
— ТЭЛА, центральный понтиальный миелиноз, рабдомиолиз, недостаточность витамина К и коагулопатия, разрыв селезенки;
— сепсис (в т.ч. и грибковый), локальные инфекции;
— жировая инфильтрация плаценты.
Диагностика и дифференциальная диагностика
Дополнительно к общим исследованиям, проводимым при диагностике заболеваний ВОПК (табл. 2), при ЧРБ проводятся следующие исследования:
— анализ мочи на кетоны;
— анализ крови на электролиты, кетоны, креатинин и кислотно-щелочное равновесие (КЩР), трансаминазы;
— анализ крови на амилазу/липазу;
— тиреотропный гормон гипофиза (ТТГ), свободный трийодтиронин (Т3) и тироксин в крови (Т4);
— при пролонгации ЧРБ позднее 20–22-й недели беременности для дифференциальной диагностики по строгим показаниям проводятся магнитно-резонансная (предпочтительнее) и компьютерная томография органов брюшной полости (ОБП).
В 50 % случаев ЧРБ отмечается повышение уровней трансаминаз, уменьшающихся по мере купирования состояния, однако требующее исключения гепатита. Обычно повышение трансаминаз является незначимым и не превышает 30 % верхней границы нормы, однако в некоторых случаях бывает более.
Амилаза повышается у 10 % беременных с ЧРБ и требует исключения панкреатита.
ЧРБ часто (в 50–60 %) ассоциируется с транзиторным гипертиреоидизмом и супрессией ТТГ, но требует исключения заболеваний щитовидной железы.
Наличие инфекций мочевыводящей системы и даже бессимптомной бактериурии способствует пролонгации ЧРБ и усилению симптомов.
Лечение
1. Проведение диетических и режимных мероприятий, рекомендуемых при тошноте и рвоте беременных легкой и средней тяжести.
2. Медикаментозное лечение начинают с назначения сбалансированных витаминно-минеральных комплексов, затем пиридоксина (витамин B6) и тиамина (витамин В1) при рвоте продолжительностью ≥ 3 недели.
Противорвотные (антиэмические) препараты назначаются только в указанной последовательности, при неэффективности предыдущих групп препаратов:
2.1. Антиэмические препараты І группы, относящиеся к группе А (FDA, USA, 2007) либо вообще не рассматриваемые как потенциально опасные для матери и плода:
— пиридоксин (витамин B6) 5% р-р — 0,25–0,5 мл 2–3 р/сут;
— авиоплант (порошок корневища имбиря) — 250 мг 4 р/сут;
— мятные таблетки — 2,5 мг 4 р/сут.
Возможно сочетание препаратов І группы между собой.
2.2. Антиэмические препараты ІІ группы, относящиеся к группе В (FDA, USA, 2007), являются безопасными для животных, однако безопасность для людей окончательно не установлена. Действуют системно, проникают через плаценту.
Могут использоваться со II триместра беременности.
2.2.1. Антиэмические препараты ІІ группы, относящиеся к пропульсантам:
— метоклопрамид (метукал, церукал) р-р — 2,0 мл (10 мг) в/м, в/в 2– 3 р/сут, затем 1 табл. (10 мг) 3–4 р/сут за 30 мин до еды и перед сном, до 4 нед.
2.2.2. Антиэмические препараты ІІ группы, которые чаще позиционируются как антигистаминные средства:
— дименгидринат (авиомарин, дедалон, драмина) — по 50 мг 4–6 р/сут (до 400 мг/сут), парентеральные формы в Украине не зарегистрированы;
— дифенгидрамин (димедрол, кальмабен) 1% — 1,0 в/м, в/в 1,0– 5,0 мл, затем табл. 0,05 г 3–4 р/сут до 300 мг/сут;
— препараты, используемые в США, — Doxylamine (Unisom), Cyclizine (Marezine) и Meclizine (Antivert) — в Украине не зарегистрированы.
2.3. Антиэмические препараты ІІІ группы, относящиеся к группе С (FDA, USA, 2007), разрешены к применению у беременных по строгим показаниям. Имеются отдельные сведения об опасности для плода. Действуют системно, проникают через плаценту. Могут использоваться только со II триместра беременности:
— скополамин (бускопан, спазмобрю) р-р — 2,0 (20 мг) п/к, в/м, в/в 2–3 р/сут, затем в табл. по 10 мг 3–5 р/сут;
— прометазин (пипольфен) р-р 2,5% — 2,0 (50 мг) в/м, в/в 2–3 р/сут, затем табл. 25–12,5 мг 4–6 р/сут (до 150 мг/сут);
— хлорпромазин (аминазин) р-р 2,5% — 1,0–2,0 (25–50 мг) в/м, в/в 2– 3 р/сут (не более 3 раз), затем табл. 50 мг 3 р/сут (до 150 мг/сут);
— ондансетрон (домеган, зофетрон, зофран, изотрон, осетрон, сетрон, эмесет, эметрон) р-р 0,2% — 2,0 (4 мг) или 0,2% — 4,0 (8 мг) в/в медленно капельно на 100 мл физраствора 1– 2 р/сут, затем табл. 4–8 мг 2 р/сут (до 150 мг/сут);
— препараты, используемые в США, — Prochlorperazine (Compazine), Trimethobenzamide (Tigan), Droperidol (Inapsine) — в Украине не зарегистрированы.
2.4. Препараты других групп используют в рефрактерных случаях ЧРБ:
— метилпреднизолон (метипред, медрол) — 16 мг внутрь или в/в 3 р/сут (через 8 ч) в течение 3 дней с дальнейшим титрованием до наиболее низкой эффективной дозы. Потенциально опасен. Относится к группе С (FDA, USA, 2007);
— апрепитант (эменд) капс. 80 мг 2 р/сут. Тератогенный эффект не определен, лучше использовать в сочетании с глюкокортикоидами.
Беременным с ЧРБ назначают минимально эффективную дозу и периодически предпринимают попытки к отмене препарата и/или переходу к использованию более безопасных препаратов.
3. Восполнение потери жидкости, коррекция нарушений электролитного обмена и КЩР.
При невозможности осуществления естественного питания (per os) пища и изотонические растворы даются через назоэнтеральный зонд. По мере улучшения состояния возобновляется пероральное питание, причем зондовое кормление должно быть прекращено за 1 час до пробного завтрака. Потребление белка должно составлять 1,3 г/кг/сут. Парентеральное введение питательных смесей должно проводиться по строгим показаниям и имеет много побочных эффектов.
Уровень гликемии должен строго контролироваться и поддерживаться на уровне 5,0–7,0 ммоль/л, несмотря на хорошую переносимость беременными больших уровней гликемии.
Парентеральное питание осуществляется через центральный венозный катетер. Беременные на парентеральном питании должны быть обследованы 2 раза в неделю с определением электролитов и кислотно-щелочного равновесия и 1 раз в неделю для исследования коагуляционного статуса, функциональных проб печени, креатинина, гликемии и трансаминаз. При парентеральном питании необходимо помнить об эссенциальных жирных кислотах, минералах и витаминах. В частности, важно получение беременными фолиевой кислоты не менее 400 мг/сут. Обязательно добавляется К+ 40 мгЭкв/л (но не более 80 мгЭкв/л). Рекомендуется 10 мгЭкв/л в час при адекватном выделении мочи.
При явлениях энцефалопатии назначают глюкозу и тиамин.
При неэффективности всех видов лечения и персистировании выраженных водно-электролитных расстройств показано прерывание беременности.
Прогноз при купировании ЧРБ для матери и плода благоприятный.
При отсутствии лечения беременных с ЧРБ в США и Европе зарегистрированы случаи смерти.
Диспепсия
Диспепсия, относящаяся к рубрике К30 (МКБ-10), является объединяющим понятием для заболеваний верхнего отдела пищеварительного канала.
В настоящее время под желудочной диспепсией (Д) подразумевают любые верхнеабдоминальные или ретростернальные боли, дискомфорт, изжогу, тошноту, рвоту или другие проявления, указывающие на заинтересованность ВОПК.
OMGE (Всемирная ассоциация гастроэнтерологов) рекомендует к использованию следующее определение.
Диспепсия (Д) — это наличие болей или дискомфорта в верхней части живота, которые обычно сопровождаются другими симптомами (тошнота, изжога, отрыжка, анорексия, раннее насыщение и переполнение), связанными или не связанными (непосредственно) с приемами пищи.
Рассмотрение диагноза Д при беременности актуально лишь в случаях отсутствия тошноты и рвоты беременных и невозможности установления диагноза «хронический гастрит» (ХГ) в соответствии с приказом МЗ Украины № 271 (патоморфологическая оценка биоптатов).
Д устанавливается на первичном приеме при отсутствии типичной клинической картины каких-либо заболеваний и требует дальнейшего обследования пациента.
Д является предварительным, «стартовым» диагнозом для начала обследования и лечения больных с патологией ВОПК и «диагнозом исключения», если является окончательным диагнозом. Диагноз Д предназначен для ведения больных со «стертыми» клиническими проявлениями заболеваний ВОПК, которые тем не менее требуют лечения на период обследования.
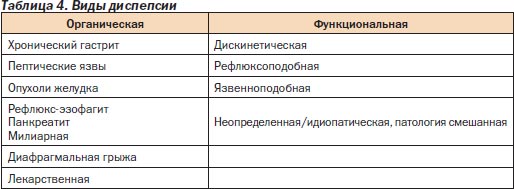
В развитых странах диагноз «диспепсия» устанавливается в 10–40 % случаев при первичном осмотре (в США — 10 %) и служит отправной точкой для обследования больного. Д может быть связана как с органическими, так и с функциональными расстройствами (табл. 4).
Разделение Д на органическую и функциональную условно и часто носит временный характер. Если в ходе обследования выявляются органические изменения ВОПК, то диагноз Д не ставится, а указывается конкретный диагноз в соответствии с выявленной патологией (например, хронический гастрит).
Если при дальнейшем обследовании не обнаруживаются признаки органических расстройств ЖКТ, то возможна постановка диагноза Д как окончательного.
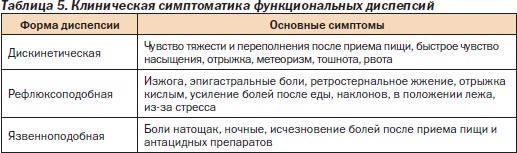
Клиническая картина функциональной Д сопровождается многочисленными невротическими проявлениями: слабостью, головными болями, кардиалгиями, раздражительностью, психоэмоциональной лабильностью, неустойчивым настроением, парестезиями в эпигастрии, а также признаками депрессии (табл. 5).
При существовании признаков Д более 3 месяцев может применяться термин «хроническая диспепсия».
Обследование больных диспепсией
Обследование больных с Д проводится в соответствии с общей методикой обследования больных с патологией ВОПК (табл. 2). Однако по показаниям могут быть выполнены дополнительные исследования:
1. Колоноскопия (для диагностики Д у беременных не проводится).
2. Суточное мониторирование рН пищевода и желудка.
3. УЗИ щитовидной железы и органов малого таза.
4. Исследование гастродуоденальной моторики:
— УЗ-определение скорости опорожнения желудка;
NB! Ирригоскопия у беременных не проводится.
При функциональных Д с помощью ФЭГДС определяют: норму или повышение тонуса желудка, наличие выраженного сосудистого рисунка, отчетливые складки (табл. 6).
Диспепсия у беременных
. или: Нарушение пищеварения, диспептический синдром, бродильная диспепсия, гнилостная диспепсия, желудочная диспепсия, неязвенная диспепсия
Диспепсия — это совокупность симптомов, возникающих при нарушении процессов переваривания пищи в желудке и замедлении опорожнения желудка. Диспепсия возникает не только при заболеваниях желудка, но и при нарушениях в работе других органов и систем.
Симптомы диспепсии у беременной
Формы диспепсии у беременной
Выделяют две основные группы диспепсических расстройств.
Причины диспепсии у беременной
Врач терапевт поможет при лечении заболевания
Диагностика диспепсии у беременной
Лечение диспепсии у беременной
Перед назначением лечения необходима консультация акушера-гинеколога.
При возникновении симптомов, характерных для диспепсии, можно применять немедикаментозные методы лечения:
Осложнения и последствия диспепсии у беременной
Осложнения чаще всего связаны с основным заболеванием и состоянием, которое явилось причиной возникновения диспепсии, в частности:
Профилактика диспепсии у беременной
ИНФОРМАЦИЯ ДЛЯ ОЗНАКОМЛЕНИЯ
Необходима консультация с врачом
Оганесян Татьяна Сергеевна, врач-гастроэнтеролог.
Певцова Анастасия Владимировна, врач-методист, акушер-гинеколог, медицинский редактор.
Ельчанинова Ольга Николаевна, редактор.
Что делать при диспепсии?
Функциональная диспепсия
Термин «диспепсия» сравнительно часто употребляется врачами в практической работе при обследовании больных, однако нередко интерпретируется по-разному, хотя буквально под этим термином подразумевается нарушение пищеварения. Тем не менее на практике, ког
Термин «диспепсия» сравнительно часто употребляется врачами в практической работе при обследовании больных, однако нередко интерпретируется по-разному, хотя буквально под этим термином подразумевается нарушение пищеварения. Тем не менее на практике, когда речь заходит о больных с диспепсией, чаще всего принимаются во внимание такие симптомы, как боли и неприятные ощущения, возникающие в животе во время приема пищи или в различное время после него, метеоризм, нарушение стула.
Этиопатогенетические аспекты диспепсии. Диспепсия как симптом многих заболеваний желудочно-кишечного тракта встречается относительно часто как при функциональных, так и при органических заболеваниях. Различные причины могут привести к появлению симптомов, обычно включаемых в синдром диспепсии. Функциональная диспепсия в гастроэнтерологической практике выявляется в 20–50% случаев, при этом у большей части больных сочетается с хроническим гастритом. Риск появления функциональной диспепсии связывают не только с нарушением диеты [28, 31], но и с приемом больными нестероидных противовоспалительных препаратов, а также и с такими, казалось бы, «нетрадиционными» факторами, как низкий образовательный уровень, аренда жилья, отсутствие центрального отопления, совместный сон (у сибсов), нахождение в браке. У некоторых больных появление симптомов диспепсии может быть связано с табакокурением и даже с психологическими нарушениями.
Для функциональной диспепсии считается характерным отсутствие каких-либо заметных желудочно-кишечных (включая и пищевод) поражений [1, 21, 24, 25]. Это подразумевает лишь наличие или отсутствие гастрита и исключает не только относительно небольшие по протяженности очаговые поражения (язвы, эрозии), но и такие, в ряде случаев относительно большие по протяженности, диффузные поражения, как рефлюкс-эзофагит, саркома, лимфоматоз желудка и др.
В настоящее время все чаще «хронический гастрит» рассматривается в качестве морфологического понятия, включающего комплекс воспалительных и дистрофических изменений слизистой оболочки желудка. Появляющиеся у части больных различные клинические симптомы, ранее обычно связываемые с воспалительными изменениями слизистой оболочки желудка и считающиеся характерными для хронического гастрита (при отсутствии органических изменений желудка), в настоящее время рассматриваются как функциональные проявления, не обусловленные теми морфологическими изменениями, которые составляют суть понятия «гастрит».
Патогенез синдрома функциональной диспепсии как в целом, так и большинства его симптомов пока еще неясен. Однако замечено, что диспепсические нарушения при функциональной диспепсии [15, 22], в том числе и сочетающейся с хроническим гaстритом, возможны у больных с ослабленной моторикой антрального отдела желудка, приводящей к замедлению эвакуации содержимого желудка в двенадцатиперстную кишку, в основе появления которой, вероятно, лежит нарушение антрумдуоденальной координации, с перемежающимся характером желудочных дисритмий (нарушений ритма). Лишь патогенез симптома быстрого насыщения желудка, связанного с замедлением опорожнения желудка, кажется, достаточно ясен.
Однако у части больных с нормальной двигательной функцией желудка также возможны симптомы функциональной диспепсии (в том числе и у пациентов с гастроэзофагеальной рефлюксной болезнью), что, скорее всего, связано с висцеральной повышенной чувствительностью желудка, в основном к растяжению. Повышенная чувствительность желудка к растяжению может быть связана с нарушением рецепторного восприятия нормальных раздражителей, включая мышечные перистальтические сокращения, а также растяжение стенок желудка пищей. У части больных диспепсические нарушения возможны и при повышенной секреции соляной кислоты (в связи с увеличением продолжительности контакта кислого содержимого желудка с его слизистой оболочкой).
Возможно, существует последовательная связь между клиническими симптомами функциональной диспепсии [8], в частности появлением дискомфорта после приема пищи (особенно после употребления продуктов и напитков, раздражающих слизистую оболочку желудка), и ослаблением релаксации желудка. Действительно, во многих сообщениях отмечается увеличение частоты появления клинических симптомов, характерных для функциональной диспепсии, после приема больными определенной пищи [9], однако почти нет сообщений, свидетельствующих о том, что употребление какой-либо пищи приводит к снижению или исчезновению этих симптомов [13, 18].
Симптоматика функциональной диспепсии. Большинство клинических симптомов, отмечаемых при органической диспепсии, встречаются и при функциональной диспепсии. Среди симптомов функциональной диспепсии можно выделить следующие: чувство тяжести, распирания и переполнения желудка, преждевременного (быстрого) насыщения, «вздутия» живота после приема пищи; появление неспецифической боли, жжения в эпигастральной области, изжоги, отрыжки, регургитации, тошноты, рвоты, срыгивания, слюнотечения, анорексии [7, 9, 19, 24]. Частота развития тех или иных симптомов функциональной диспепсии, время возникновения, интенсивность и продолжительность, по нашим наблюдениям, могут быть различными. Комплекс всех симптомов, считающихся характерными для функциональной диспепсии, в период значительного ухудшения состояния больных встречается лишь у небольшой части больных; в частности, по нашим наблюдениям, среди пациентов, госпитализированных в стационар, — в 7,7% случаев (у 13 из 168 больных).
Большая часть больных с функциональной диспепсией, в том числе и сочетающейся с хроническим гастритом, относительно редко обследуются и лечатся не только в стационарах, но и в амбулаторно-поликлинических условиях. Только немногие пациенты при ухудшении состояния обращаются к врачу, настаивая на госпитализации в стационар для уточнения диагноза и лечения.
При обследовании больных хроническим гастритом с функциональной диспепсией, госпитализированных в ЦНИИ гастроэнтерологии, боль в эпигастральной области отмечалась в 95,5% случаев, тошнота — в 13,4% случаев; чувство тяжести в эпигастральной области — в 91,1% и чувство раннего насыщения, возникающее во время или сразу же после приема пищи, — в 87,5% случаев; отрыжка — в 67,9%, «вздутие» живота — в 77,7% случаев.
По-видимому, различия в контингенте обследованных больных с функциональной диспепсией влияют на частоту развития тех или иных симптомов этого синдрома, представляемых в литературе различными исследователями. Так, по другим данным [26], у больных с функциональной диспепсией боль в верхних отделах живота установлена лишь в 36% случаев: только 60% из этих больных предъявляли жалобы на боль, возникающую после приема пищи, 80% пациентов беспокоили ночные боли (в то же время боль в животе, которая мешала больным спать, — в 89,3% случаев). Чувство раннего насыщения больные отмечали в 85,7% случаев, жжение (изжогу), в основном в эпигастральной области, — в 88,4% случаев, тошноту — в 92,9% случаев.
Достаточно известно, что периодически возникающая изжога (жжение) возможна у больных и при нормальном по времени контакте соляной кислоты со слизистой оболочкой пищевода и/или желудка (43%); у таких больных нормальное давление нижнего сфинктера пищевода составляет 10 мм рт. ст. и более. Приблизительно у 30% лиц, постоянно принимающих антацидные препараты для устранения изжоги (жжения), отмечается повышенная висцеральная чувствительность пищевода к механическим или химическим стимулам (при нормальных данных эзофагоскопии и суточной рН-метрии) [29]. В отличие от органической диспепсии такой характерный для диспепсии симптом, как чувство быстрого насыщения после приема пищи, отмечается лишь у больных с функциональной диспепсией. Кроме того, чрезмерная отрыжка, рвота по утрам чаще беспокоят больных с функциональной диспепсией.
К сожалению, описание различных симптомов, считающихся характерными для диспепсии вообще, в том числе и функциональной диспепсии, а также интерпретация этих симптомов разными больными вносят определенную путаницу при сопоставлении данных, полученных и представляемых различными исследователями. В частности, боль в животе (и даже за грудиной) может «трактоваться» больными и как чувство жжения, спазма и неопределенного ощущения, изжога — как чувство жжения не только за грудиной, но и в эпигастральной области, регургитация — как «появление кислоты» в полости рта.
Диагностика функциональной диспепсии. Известно, что диагноз функциональной диспепсии устанавливается на основании изучения и анализа симптомов, анамнеза заболевания, результатов физикального обследования больных, а также данных лабораторно-инструментального обследования, по существу, — посредством исключения органических заболеваний, при которых возникли симптомы диспепсии, т. е. исключения органической диспепсии.
Неоднократно предлагалось при постановке диагноза функциональной диспепсии учитывать те или иные сроки появления симптомов, которые рассматриваются в качестве характерных для этого синдрома, частоту их возникновения, продолжительность (в течение определенного времени, в том числе и в течение одного года), однако вряд ли такой подход к обследованию больных найдет широкое применение. Интенсивность, частота и время появления симптомов диспепсии могут быть различными. При этом значительная часть больных настолько привыкают к симптомам диспепсии, что зачастую и не обращают на них внимания (да и в течение продолжительного времени не воспринимают их как проявление какой-либо болезни). Иногда те или иные препараты принимают (без консультации с врачами) с целью устранения неприятных ощущений различного типа. И наконец, чаще всего больной не может точно вспомнить время появления многих диспепсических расстройств, частоту их возникновения (даже интенсивных по выраженности симптомов). Поэтому, как правило, начало развития функциональной диспепсии, а нередко и ее течение врач может проследить со слов больных лишь приблизительно.
Дифференциальная диагностика. При дифференциальной диагностике симптомов диспепсии следует учитывать следующее: в 40% случаев симптомы диспепсии встречаются у больных с доброкачественными язвами желудка и двенадцатиперстной кишки различной этиологии, с гастроэзофагеальной рефлюксной болезнью и раком желудка. У 50% больных причина появления клинических симптомов диспепсии остается неясной, поэтому нередко они ошибочно рассматриваются как проявления функциональной диспепсии. Именно поэтому при дифференциальной диагностике органической и функциональной диспепсии, наряду с выяснением симптомов и анамнеза заболевания и анализом полученных данных, существенное значение (в сомнительных случаях) имеют результаты таких объективных методов, как эндоскопическое и рентгенологическое обследование, ультрасонография; в некоторых случаях при обследовании больных показано и проведение компьютерной томографии. Применение этих методов позволяет выявить или исключить наличие других заболеваний (в том числе и установить причину органической диспепсии).
Авторы некоторых публикаций [7, 9, 19, 24], сообщая о функциональной диспепсии, не сходятся в выделении того или иного их симптомокомплекса. Отметим две наиболее распространенные классификации функциональной диспепсии. Согласно одной из них [6], выделяются язвенноподобный, дискинетический, связанный с нарушением моторики, и неспецифический варианты; при этом рефлюксподобная диспепсия рассматривается как часть симптоматического комплекса гастроэзофагеальной рефлюксной болезни. Однако, согласно другой классификации [27], выделяются следующие варианты функциональной диспепсии: вариант, связанный с нарушением моторики, язвенноподобная диспепсия, рефлюксоподобная диспепсия и неспецифическая диспепсия.
Наши собственные наблюдения свидетельствуют о том, что подразделение функциональной диспепсии на разные типы может рассматриваться лишь как весьма условное. Только у части больных есть возможность выявить тот или иной комплекс симптомов, который можно более или менее точно связать с одним из вариантов функциональной диспепсии, особенно если придерживаться определения функциональной диспепсии, предложенного составителями Римских критериев по функциональным заболеваниям желудочно-кишечного тракта. При постановке диагноза функциональной диспепсии предлагается учитывать следующие критерии:
Как показывает практика, у большинства больных с функциональной диспепсией в период обращения больных к врачу нередко достаточно сложно определить вариант диспепсии для выбора наиболее оптимального варианта лечения. В определенной степени это связано с тем, что в период обращения к врачу пациента могут беспокоить не все симптомы, которые, по данным анамнеза заболевания, сохранялись у него 12 недель и более в течение последнего года. Лишь при наличии множества симптомов удается более или менее точно определить вариант функциональной диспепсии. Поэтому, по нашим наблюдениям, при подборе медикаментозного лечения целесообразно учитывать прежде всего основные симптомы диспепсии, причиняющие больному наибольшее беспокойство.
Терапия функциональной диспепсии. Основная цель лечения больных с функциональной диспепсией — улучшение объективного и субъективного состояния, включая устранение болей и диспепсических расстройств.
Успех лечения больных с функциональной диспепсией в значительной степени определяется следующими факторами:
Известно, что при лечении больных с функциональной диспепсией, в том числе и сочетающейся с хроническим гастритом, в нашей стране наиболее часто применяются (в зависимости от состояния больных) следующие медикаментозные препараты (или их комбинации): прокинетики (домперидон, метоклопрамид), антисекреторные препараты (ингибиторы протонного насоса, антагонисты Н2-рецепторов), невсасывающиеся антацидные препараты (висмута трикалия дицитрат (денол)), ферментные препараты (фестал, микразим, панзинорм, пензитал и др.). Иногда у больных с хроническим гастритом, ассоциируемым с Helicobacter pylori (НР), и сочетающимся с функциональной диспепсией, проводится антихеликобактерная терапия, в ходе которой в качестве базисных препаратов чаще используются висмута трикалия дицитрат (де-нол) или ингибиторы протонного насоса.
Наличие большого количества вариантов медикаментозной терапии, предлагаемых для лечения больных с функциональной диспепсией, в определенной степени свидетельствует о неудовлетворенности врачей результатами лечения пациентов с функциональной диспепсией. Вероятно, это связано не только с недостаточной изученностью патогенеза большинства симптомов диспепсии, но и патогенеза синдрома функциональной диспепсии в целом, а также с нередко возникающими при дифференциации вариантов функциональной диспепсии по комплексу тех или иных симптомов трудностями. Это объясняется тем, что интерпретация многих симптомов диспепсии больными в разных популяциях населения, включая и этнические группы, существенно различается.
В качестве прокинетиков при лечении больных с функциональной диспепсией обычно используются домперидон (мотилиум, мотониум) или метоклопрамид (церукал). Эти препараты усиливают перистальтику пищевода и желудка, а также обеспечивают нормализацию гастродуоденальной координации и опорожнения желудка, увеличение тонуса нижнего сфинктера пищевода. Применение данных средств показано при наличии у больных с функциональной диспепсией таких симптомов, как замедление опорожнения желудка (чувство раннего насыщения, возникающее во время еды или сразу после приема небольшого количества пищи), а также симптомов, ассоциируемых с повышенной чувствительностью желудка к растяжению (чувство тяжести, распирания и/или переполнения желудка, возникающие во время или непосредственно после приема пищи); при наличии изжоги (жжения). Обычная доза прокинетиков — 10 мг 3 раза в сутки за 20–30 мин до еды. В тяжелых случаях дозировку прокинетиков можно увеличить до 10 мг 4 раза в сутки (последний раз на ночь), до снижения интенсивности выраженных проявлений диспепсии, затем продолжить лечение больных препаратами в обычной дозировке.
При использовании домперидона (мотилиум, мотониум) возникает меньшая, по сравнению с метоклопрамидом, вероятность появления побочных эффектов [3]. Поэтому в случае необходимости домперидон можно использовать в лечении больных более продолжительное время, однако не менее 3 нед.
Лечение больных домперидоном позволяет устранить чувство преждевременного насыщения в 84% случаев, распирания в подложечной области — в 78%, дискомфорта после приема пищи — в 82% и тошноты — в 85% случаев. К сожалению, сроки лечения больных (это относится ко всем прокинетикам) довольно часто превышают 2–5 нед.
Для устранения выраженных боли и/или изжоги (жжения) в эпигастральной области у больных с функциональной диспепсией вполне достаточно в течение первых 7–10 дней использовать ингибиторы протонного насоса в стандартной дозировке 1 раз в день (лансопразол, пантопразол, рабепразол, эзомепразол соответственно по 30, 40, 20 и 40 мг), после этого пациентов можно переводить на лечение антагонистами Н2-рецепторов (ранитидин или фамотидин соответственно по 150 мг и 20 мг 2 раза в день). Известно, что омепразол (лосек) в дозе 20 мг позволяет в среднем снизить суточный уровень выделения соляной кислоты в желудке на 80%, ранитидин в дозе 300 мг в сутки в среднем до 60%, что в определенной степени определяет эффективность этих препаратов. Вышеуказанный курс лечения целесообразно проводить у лиц с функциональной диспепсией при язвенноподобном варианте или при наличии у больных рефлюксоподобной диспепсии.
Однако всегда ли необходимо значительно ингибировать кислотообразование в желудке для успешного лечения больных с функциональной диспепсией, в том числе сочетающейся с хроническим гастритом? Этот вопрос невольно встает перед врачами и исследователями в связи с тем, что соляная кислота в организме человека играет и определенную защитную роль; кроме того, чрезмерное снижение секреции соляной кислоты повышает вероятность увеличения микрофлоры в желудке. Известно также, что ингибиторы протонного насоса и антагонисты Н2-рецепторов более эффективны при гиперсекреции соляной кислоты. Поэтому в лечении больных функциональной диспепсией при неспецифическом варианте, а также части пациентов с нарушением моторики верхних отделов желудочно-кишечного тракта целесообразно использовать висмута трикалия дицитрат, оказывающий цитопротекторное действие на слизистую оболочку желудка. Его назначают по 120 мг 4 раза в день; при необходимости, для устранения болевых ощущений в качестве терапии «по требованию», целесообразно дополнительно принимать один из антагонистов Н2-рецепторов 1–2 раза в день в терапевтической дозировке до устранения боли и жжения в эпигастральной области.
И все же главное в терапии больных — лечение одним или несколькими препаратами, механизм действия которых позволяет устранить симптомы функциональной диспепсии, причиняющие пациентам наибольшее беспокойство. В частности, при наличии часто повторяющихся симптомов диспепсии, обычно объединяемых единым термином «дискомфорт», у больных с функциональной диспепсией следует использовать ферментные препараты (панкреатин, микрозим, фестал, пензитал, панзинорм и др.), даже при нормальной внешнесекреторной функции поджелудочной железы, в необходимых случаях сочетая их применение с антагонистами Н2-рецепторов или с прокинетиками, с висмутом трикалия дицитратом. Определенное улучшение процессов пищеварения и нормализация двигательной функции желудочно-кишечного тракта способствуют устранению симптомов функциональной диспепсии, связанных с повышенной висцеральной чувствительностью желудка к растяжению, механической и химической стимуляции, а также с нарушением моторики.
Длительность лечения больных определяется их общим состоянием, которое во многом зависит от отношения к своему здоровью и выполнения рекомендаций врачей.
Не менее важно научить пациентов соблюдать режим труда и отдыха, избегать приема тех или иных продуктов, плохо переносящихся ими; посоветовать им своевременно обращаться к врачам за медицинской помощью, если в этом появится необходимость.
Функциональная диспепсия и НР. При рассмотрении вопроса о существовании связи между функциональной диспепсией и НР, необходимо принимать во внимание три аспекта.
Взаимосвязь между НР и функциональной диспепсией остается неясной. По некоторым наблюдениям [28, 30, 31], функциональная диспепсия лишь в 28–40% случаев сочетается с хроническим гастритом, ассоциируемым с НР. Однако между клиническими симптомами, считающимися характерными для функциональной диспепсии, и наличием обсемененности НР слизистой оболочки желудка [1, 7, 19] не установлено какой-либо достоверной связи: не выявлено каких-либо специфических симптомов, характерных для НР-положительных больных с функциональной диспепсией. Да и значение НР в развитии нарушений моторики желудка является спорным.
Взгляды на целесообразность проведения эрадикации НР при функциональной диспепсии и гастроэзофагеальной рефлюксной болезни весьма противоречивы. В частности, одни исследователи [16, 17] полагают, что эрадикация НР при функциональной диспепсии, как и при гастроэзофагеальной рефлюксной болезни [20] необходима, в то время как другие [5] считают, что инфекция НР у больных с рефлюкс-эзофагитом и хроническим гастритом может иметь защитный эффект.
По наблюдениям некоторых исследователей [28, 31], инфекция НР в популяции достоверно связана с наличием синдрома диспепсии и может быть «ответственна» лишь за 5% симптомов, считающихся характерными для поражения верхних отделов желудочно-кишечного тракта: эрадикация способствует уменьшению частоты и интенсивности диспепсии, однако это не приводит к улучшению качества жизни пациентов. Эрадикационная терапия может быть экономически оправдана при функциональной диспепсии, сочетающейся с хроническим гастритом, у инфицированных НР больных, однако лица, принимающие решения, должны быть готовы оплачивать такое лечение.
С учетом отдаленных результатов лечения больных установлено, что эрадикационная терапия хронического хеликобактерного гастрита не оправдала возлагаемых на нее надежд [2, 11, 23] в устранении симптомов функциональной диспепсии. Увеличение уровня желудочной секреции, возникающее у части больных гастроэзофагеальной рефлюксной болезнью после проведенной эрадикации НР [12] представляет собой существенный фактор, провоцирующий обострение или возникновение рефлюкс-эзофагита [4, 10, 14]. Учитывая разноречивость сообщений различных исследователей, в широкой клинической практике при лечении больных с хроническим гастритом, ассоциированным с НР и сочетающимся с синдромом функциональной диспепсии или с гастроэзофагеальной рефлюксной болезнью, пока еще не следует отдавать предпочтение антихеликобактерной терапии перед антисекреторной.
Литература
Ю. В. Васильев, доктор медицинских наук, профессор
ЦНИИ гастроэнтерологии, Москва