Диагноз пня гинекология что это
Диагноз пня гинекология что это
Диагноз преждевременной яичниковой недостаточности (ПЯН) ставят при аменорее, дефиците эстрогенов и повышенном количестве ФСГ у женщин до 40 лет. Распространенность составляет около 1%. Большинство случаев преждевременной яичниковой недостаточности (ПЯН) связано с химиотерапией и лучевой терапией по поводу рака. Преждевременная яичниковая недостаточность (ПЯН) обычно необратима, хотя возможно спонтанное восстановление функций яичников. Преждевременная яичниковая недостаточность (ПЯН) — частая причина вторичной аменореи (4-18% наблюдений).
В ряде случаев этиология преждевременной яичниковой недостаточности (ПЯН) остается невыясненной. Тем не менее у больных с аменореей до 30-летнего возраста нужно исследовать кариотип на транслокацию половой хромосомы, а также наличие Y-хромосомы, потому что эти состояния связаны с повышенным риском существования злокачественных опухолей яичников. Некоторые эксперты рекомендуют подвергать хромосомному анализу всех больных с преждевременной яичниковой недостаточностью (ПЯН). Тем не менее у больных с вторичной аменореей, связанной с преждевременной яичниковой недостаточностью (ПЯН), чаще всего идентифицируют кариотип 46ХХ.
Дисгенезия гонад как причина преждевременной яичниковой недостаточности (ПЯН)
В редких случаях у больных с дисгенезией гонад происходит нормальное пубертатное развитие, а затем у них наступает вторичная аменорея, чаще в возрасте до 30 лет.
У женщин со вторичной аменореей в результате дисгенезии гонад обычно выявляют нормальный кариотип 46ХХ, хотя у некоторых могут быть обнаружены 47ХХХ или 46X0. У больных с дисгенезией гонад и нормальным кариотипом возможны другие пороки, такие как нейросенсорная глухота (синдром Перро) или синдром ломкой Х-хромосомы — наиболее частая генетическая причина нарушений развития.
Приблизительно у 16% женщин-носителей премутированного аллеля синдрома ломкой Х-хромосомы возникает преждевременная яичниковая недостаточность (ПЯН), особенно если в семейном анамнезе прослеживается преждевременная яичниковая недостаточность (ПЯН) или умственная отсталость. Когда у женщин со спорадической преждевременной яичниковой недостаточностью (ПЯН) проводят скрининго-вое исследование, 3% из них оказываются носителями генных мутаций. У некоторых обнаруживают умеренную умственную отсталость и плохую обучаемость.
Существует также связь между преждевременной яичниковой недостаточностью (ПЯН) и наследуемой аутосомно-доминантным путем патологией глазного яблока — инверсивным синдромом блефарофимоза-птоза-эпикантуса. Этот синдром сопровождается мутацией FOXL2 гена, транскрипционного фактора, расположенного на хромосоме 3. Некоторые другие аутосомные нарушения связаны с яичниковой недостаточностью, они приводят к повышению содержания ФСГ без истощения запаса ооцитов. Некоторые из них включают мутации в генах фосфоманомутазы 2 (РММ2), галактоза-1-фосфатуридитрансферазы (CALT), рецептора к ФСГ и аутоиммунорегулирующего гена (АРГ), который ответствен за полиэндокринопатию — эктодермальную дистрофию.
Аутоиммунные причины преждевременной яичниковой недостаточностью (ПЯН)
Часто причиной преждевременной яичниковой недостаточностью (ПЯН) бывают аутоиммунные заболевания. У 40% женщин с преждевременной яичниковой недостаточностью (ПЯН) есть аутоиммунная патология, чаще всего аутоиммунный тиреоидит с развитием гипотиреоза. ПЯН чаще встречается у пациенток с инсулинозависимым сахарным диабетом, myasthenia gravis и заболеваниями паращитовидных желез, чем у здоровых женщин. От 10 до 60% женщин, страдающих болезнью Аддисона, имеют ПЯН.
Поскольку у этих больных повышен риск аутоиммунных эндокринных заболеваний, они должны ежегодно проходить обследование по поводу различных аномалий, что позволяет своевременно начать лечение. Больные с преждевременной яичниковой недостаточностью (ПЯН) невыясненной этиологии должны пройти полное обследование для выявления аутоиммунных расстройств. Необходимо оценить уровень кальция, фосфор, глюкозу натощак, антитела к 21-гидроксилазе, свободный Т4, ТТГ и антитиреоидные антитела. Обследование необходимо проводить ежегодно.
Скрининг на антиовариальные антитела проводить не рекомендуется в свете низкой информативности и специфичности. Необходимо проводить скрининг пациентов на наличие патологии надпочечников при помощи определения уровня антиандреналовых антител. Если этот тест оказывается положительным, необходимы более сложные исследования, например тест стимуляции кортикотропином. Определение содержания кортизола в сыворотке крови утром натощак не информативно.
Преждевременная яичниковая недостаточность: другие причины
Хотя повышенное содержание ФСГ в сыворотке крови почти всегда связано с патологией яичников, встречаются необычные ситуации, когда повышение количества ФСГ связано не с овариальными, а с центральными проблемами. К последним относятся аденомы гипофиза, секретирующие ФСГ, или специфические дефекты ферментов, например дефицит 17-гидролазы (Р450с17) или галактоза-1-фосфат уридилтрансферазы (галактоземия).
Есть несколько сообщений об изолированном дефиците гонадотропинов. Одновременное определение количества ЛГ и ФСГ позволяет распознать это редкое состояние. В случае преждевременной яичниковой недостаточности (ПЯН) обнаруживают оба этих гормона, повышение содержания одного из них нетипично. Большинство таких нарушений связано с изменением одного гена или заменой аминокислоты. В этих случаях МРТ гипофиза позволит распознать гипофизарную аденому, секретирующую оба гормона, особенно если это связано с повышением секреции а-субъединицы. Тем не менее эти опухоли обычно не связаны с аменореей.
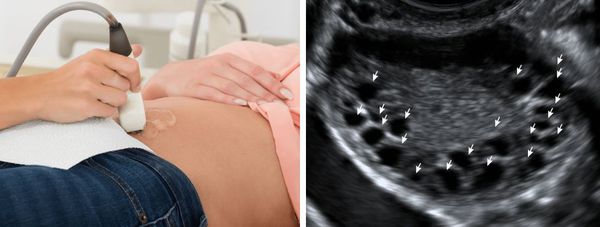
Может также происходить мутация гонадотропных рецепторов. У таких больных диагностируют синдром резистентных яичников. Обычно у этих женщин присутствует вторичная аменорея в сочетании с нормальными вторичными половыми признаками. Реакции на гонадотропины нет, а при УЗИ яичников выявляются мелкие антральные фолликулы.
Существует мутация гена, отвечающего за ФСГ-рецепторы (как у мужчин, так и у женщин) [74]. У женщин обнаруживают гипергонадотропный гипогонадизм из-за нечувствительности к ФСГ. Этот фенотип проявляется как отсутствием развития молочных желез, так и нормальными молочными железами, а также первичной или вторичной аменореей. Эти относительно необычные находки обнаружены у определенной части населения Финляндии (1% женщин — гетерозиготы).
Мутация рецептора к ЛГ у женщин с кариотипом 46,XX приводит к сочетанию нормального полового развития и аменореи. Количество ЛГ в сыворотке крови колеблется от нормального до повышенного, содержание ФСГ нормальное, эстрадиола в фолликулярную фазу — нормальное, прогестерона — снижено. Матка маленькая, состояние яичников характеризуется стойкой ановуляцией.
Диагностика преждевременной яичниковой недостаточности
Первичное обследование, как и во всех случаях аменореи, состоит из определения количества ТТГ, пролактина и ФСГ в сыворотке крови. Диагноз ПЯН ставят при повышении концентрации ФСГ, нормальном количестве пролактина и ТТГ. Показатели эстрадиола будут снижены, таким образом, тест с прогестином не будет вызывать менструацию — подобное кровотечение в ответ на отмену.
Женщинам с ПЯН необязательно проводить биопсию яичников. Цена и риск хирургического вмешательства значительны, а влияния на тактику лечения это исследование не окажет. Необходимо выполнить ТВУЗИ для определения количества фолликулов в яичнике.
Лечение преждевременной яичниковой недостаточности
Женщинам с ПЯН следует предложить заместительную терапию эстрогенами и прогестероном, чтобы сохранить их вторичные половые признаки и уменьшить риск развития остеопороза. Этого можно достичь с помощью комбинированных пероральных контрацептивов до возраста естественной менопаузы, если нет противопоказаний. У некоторых женщин, принимающих малые дозы экзогенных эстрогенов с прогестином, возможно спонтанное появление овуляции и (в редких случаях) наступает беременность.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Яичниковая недостаточность ( Овариальная недостаточность )
Яичниковая недостаточность — это функциональная несостоятельность фолликулярного аппарата, обусловленная его неразвитостью, необратимым повреждением или нечувствительностью к гонадотропинам. Проявляется бесплодием, нерегулярными менструациями или их отсутствием, признаками гипоэстрогении. Диагностируется с помощью гинекологического осмотра, анализа уровней половых гормонов, УЗИ органов малого таза, диагностической лапароскопии, цитогенетического исследования. Для лечения бесплодия применяют метод донации. В остальных случаях назначают заместительную гормонотерапию.
МКБ-10
Общие сведения
Яичниковая недостаточность является следствием нескольких заболеваний, имеющих сходную клиническую картину, но разные этиопатогенетические механизмы. Форма расстройства, связанная с дисгенезией гонад, диагностируется у 1 девочки на 10-12 тысяч новорожденных. Истощение фолликулярного аппарата и синдром его резистентности к фолликулостимулирующему гормону отмечаются у 10% пациенток, страдающих аменореей. В подростковом возрасте овариальная недостаточность обычно обусловлена генетическими факторами. У женщин репродуктивного возраста нарушение менструальной функции и фертильности может носить первичный характер или возникать вторично на фоне ранее нормальных менструальной и генеративной функций.
Причины
Секреция половых гормонов нарушается при изначально недостаточном количестве примордиальных фолликулов, их ускоренной атрезии или функциональной несостоятельности. Специалисты в сфере гинекологии выделяют несколько групп причин, которые вызывают первичное повреждение фолликулярного аппарата либо изменяют чувствительность овариальной ткани к стимулирующему действию гонадотропинов:
При трубной беременности, разрыве кисты, злокачественных опухолях яичники удаляют хирургически. Функциональная недостаточность овариального аппарата наблюдается у некоторых пациенток с хроническими воспалительными заболеваниями придатков матки — оофоритом, аднекситом. Вероятность преждевременной атрезии примордиальных фолликулов особенно высока при специфическом инфекционном процессе, вызванном микобактериями туберкулеза.
Патогенез
В основе формирования яичниковой недостаточности обычно лежит пре- и постпубертатная деструкция герминативной ткани. Механизм развития заболевания зависит от причин, вызвавших расстройство. При большинстве генетических дефектов количество фолликулов изначально низкое, обычно их хватает не более чем на 5-15 лет репродуктивной жизни. Экзогенные воздействия, аутоиммунные расстройства, инфекционно-воспалительные заболевания вызывают ускоренную атрезию клеток коркового слоя. В редких случаях из-за нарушения чувствительности рецепторного аппарата снижается или отсутствует реакция яичников на действие гонадотропных гормонов.
Вне зависимости от этиологии конечное звено заболевания является общим — прекращается овуляция, развивается гипоэстрогения. Истощенные яичники выглядят гипопластичными, имеют небольшие размеры (1,5-2,0 см х 0,5 см х 1,0-1,5 см) и массу (до 1,0-2,0 г каждый). После прекращения секреторной активности в стерильной коре отсутствуют примордиальные фолликулы, межуточная ткань атрофирована. На фоне низкой секреторной активности гонад гипофиз по принципу обратной связи образует повышенное количество гонадотропинов, поэтому такая форма овариальной недостаточности носит название гипергонадотропного гипогонадизма.
Классификация
Систематизация форм яичниковой недостаточности осуществляется с учетом причин, приведших к развитию заболевания, и степени его выраженности. Этиопатогенетический подход позволяет более точно оценить репродуктивные способности пациентки и выбрать оптимальную тактику лечения. По мнению современных акушеров-гинекологов, существует три основных клинических варианта недостаточности яичников:
При оценке выраженности овариальной недостаточности ориентируются на наличие клинических симптомов и уровень ФСГ в сыворотке крови. На скрытой стадии заболевания содержание ФСГ в норме, но женщина не может забеременеть без видимых причин. Для биохимической стадии характерно повышение базальной концентрации ФСГ при необъяснимом бесплодии. Явная недостаточность сопровождается бесплодием, нерегулярными месячными и повышенным базальным уровнем ФСГ. О раннем истощении гонад свидетельствуют аменорея, высокая концентрация ФСГ и необратимое бесплодие вследствие полной атрезии фолликулярного аппарата.
Симптомы яичниковой недостаточности
На скрытом и биохимическом этапе заболевания единственным признаком зачастую является бесплодие, необъяснимое какими-либо органическими причинами. О переходе расстройства в явную фазу свидетельствует нарушение овариально-менструального цикла – месячные становятся редкими, нерегулярными, со временем прекращаются полностью. Зачастую возникают признаки эстрогенной недостаточности — приливы, снижение полового влечения, сухость и атрофия слизистых влагалища и вульвы, остеопороз. При врожденной дисгенезии у женщин могут выявляться характерные внешние признаки наследственной патологии (дисморфическое телосложение, крыловидные шейные складки, аркообразное небо, недоразвитие вторичных половых признаков, недостаточное оволосение на лобке, в подмышках).
Осложнения
Наиболее серьезным последствием яичниковой недостаточности является бесплодие. Преждевременное угасание секреторной функции фолликулярной ткани провоцирует раннее старение организма с повышенным риском развития кардиопатологии (ишемической болезни сердца, инфаркта миокарда), болезни Паркинсона, деменции. Остеопороз, возникший вследствие эстрогенной недостаточности, сопровождается увеличением вероятности переломов. У пациенток снижается работоспособность, ухудшается качество жизни, нарушаются сексуальные отношения, могут возникать депрессивные и даже суицидальные мысли.
Диагностика
Комплексное обследование для исключения яичниковой недостаточности назначают всем больным с бесплодием неясного генеза. Основными задачами диагностического поиска являются определение функциональных возможностей яичников, оценка морфологической структуры их тканей. Наиболее ценными для постановки диагноза считаются такие методы, как:
При подозрении на дисгенезию гонад показаны консультация генетика, цитогенетические методы (кариотипирование и др.). Для определения возможных последствий эстрогенной недостаточности дополнительно назначают денситометрию, исследование липидного обмена. Первичную и вторичную овариальную недостаточность дифференцируют с гипогонадотропным гипогонадизмом, поликистозом и синдромом склерокистозных яичников, другими заболеваниями, нарушающими менструальную и репродуктивную функции. По показаниям пациентку консультируют эндокринолог, онколог, невропатолог, нейрохирург, кардиолог.
Лечение яичниковой недостаточности
Методов, позволяющих восстановить фолликулярный аппарат овариальной ткани, на сегодняшний день не предложено. Использование стимуляторов овуляции обычно неэффективно. Выбор тактики ведения пациентки определяется в первую очередь ее возрастом и репродуктивными планами. Рекомендованными схемами лечения овариальной недостаточности являются:
Хирургические методы лечения рекомендованы пациенткам, у которых патология яичниковой ткани сопряжена с генетическим дефектом в виде наличия Y-хромосомы. Проведение двухсторонней оофорэктомии позволяет снизить риск развития герминогенного рака яичников, который у таких женщин возникает чаще, чем в среднем по популяции. Операция обычно выполняется лапароскопически.
Прогноз и профилактика
В большинстве случаев возможность естественного оплодотворения у пациенток, страдающих яичниковой недостаточностью, восстановить невозможно, хотя некоторые из таких женщин беременеют даже без активного лечения. Эффективность одной попытки донации в настоящее время достигает 30%. Применение заместительной гормонотерапии позволяет существенно улучшить качество жизни при преждевременном истощении яичников, их дисгенезии и резистентности. Профилактика предполагает сведение к минимуму токсических воздействий на яичниковую ткань, своевременное лечение хронической генитальной и экстрагенитальной патологии, выбор органосохраняющих вмешательств при необходимости оперативного лечения.
Альтернативный подход к лечению женщин с преждевременной недостаточностью яичников
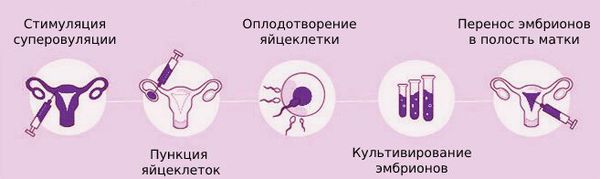
Согласно данным Росстата, частота женского бесплодия в Российской Федерации в 2018 г. достигла 273,8 на 100 тыс. женщин репродуктивного возраста (для сравнения: в 2005 г. – 146,6 на 100 тыс.) [1]. Одной из причин женского бесплодия является преждевременная недостаточность яичников (ПНЯ). В 74% случаев ПНЯ единственный шанс забеременеть – провести экстракорпоральное оплодотворение с использованием ооцитов донора [2]. В связи с этим актуальным представляется поиск новых подходов к решению данной проблемы.
Частота встречаемости ПНЯ в женской популяции составляет 1,5%, а в структуре вторичной аменореи – до 10% [3–5]. Известно несколько теорий, объясняющих причины возникновения ПНЯ: пре- и постпубертатная деструкция ооцитов, хромосомные аномалии, аутоиммунные расстройства и др. [6]. Типичный портрет пациентки: молодая девушка с наличием менопаузальных симптомов, у которой не наступает беременность на фоне вторичной аменореи [7]. К диагностическим критериям ПНЯ относят олигоменорею, аменорею в течение 4–6 месяцев, уровень фолликулостимулирующего гормона (ФСГ) в крови свыше 25 МЕ/л в двукратных исследованиях с интервалом не менее четырех недель, снижение уровня эстрадиола (Е2) и антимюллерова гормона (АМГ) в крови [8].
Патогенетическим подходом к лечению ПНЯ признана заместительная гормональная терапия [9]. Однако на данный момент эффективные схемы лечения, позволяющие улучшить прогноз в отношении восстановления фертильности, отсутствуют [8]. Альтернативным методом лечения ПНЯ считается плацентарная терапия препаратом Мэлсмон.
Мэлсмон, гидролизат плаценты человека (Melsmon pharmaceutical, Co., Ltd., Япония) – концентрат низкомолекулярных биологически активных веществ, полученных из терминальных ворсин хориона плаценты человека, в ампулах для подкожного введения. Плацентарный препарат Мэлсмон имеет регистрационное удостоверение лекарственного средства Минздрава России № ЛП-000550 [10]. Вероятно, в основе плацентарной терапии ПНЯ лежит влияние на различные звенья этого многофакторного синдрома. Препарат Мэлсмон обеспечивает коррекцию митохондриальной дисфункции, увеличивает регенераторный потенциал клеток, подавление циклооксигеназы 2 и таких медиаторов воспаления, как NO и фактор некроза опухоли альфа, обусловливая положительное влияние на инфекционно-воспалительный фактор возникновения ПНЯ и увеличение овариального резерва [11].
В казанский медицинский центр «Джаннис» обратилась пациентка Э. 22 лет с жалобами на отсутствие менструаций (аменорею) в течение года и отсутствие наступления беременности в течение четырех лет, ощущение приливов жара до десяти раз в сутки, гипергидроз, снижение либидо, вялость, повышенную утомляемость, одышку, бессонницу. Пациентка замужем четыре года, брак первый, при регулярной половой жизни в отсутствие каких-либо методов контрацепции беременность в данном браке не наступила. Муж пациентки прошел исследование состояния репродуктивного здоровья. Мужской фактор бесплодия исключен. Менструации у пациентки с 11 лет, установились сразу, продолжительность – пять дней, через 30 дней. Из анамнеза (июнь 2016 г. – ноябрь 2018 г.) известно о нарушении менструального цикла в виде скудных кровянистых выделений (олигоменорея) и их постепенном исчезновении. В ноябре 2018 г. при осмотре в зеркалах обнаружен фиброзный полип цервикального канала. Выполнена гистероскопия с раздельным диагностическим выскабливанием и удалением полипа цервикального канала. Гистологическое заключение: железистая гиперплазия эндометрия с элементами полипоза на фоне хронического эндометрита. Фиброзный полип шейки матки. Соматический анамнез не отягощен. На инфекции, передаваемые половым путем, ранее не обследовалась. Профессиональных вредностей, вредных привычек не имеет. В течение четырех месяцев, начиная с декабря 2015 г., с целью регуляции менструального цикла принимала Регулон, затем прекратила прием из-за резкого повышения индекса массы тела (после отмены препарата Регулон вес вернулся к прежним значениям).
При сборе семейного анамнеза выяснилось, что у матери менструальная функция прекратилась в 34 года. Из-за отсутствия наступления беременности семья испытывает стресс.
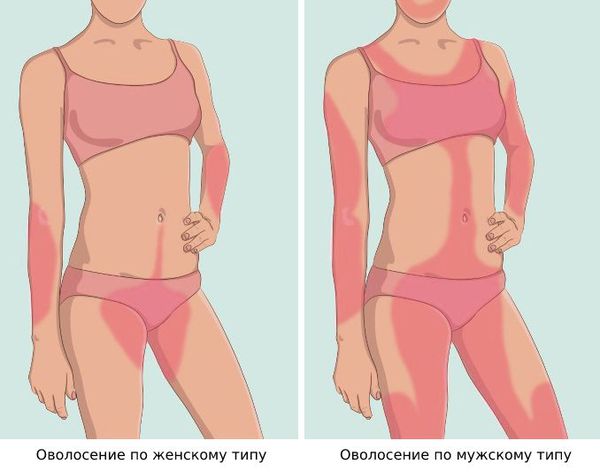
Наружные половые органы развиты правильно. Оволосение по женскому типу. При осмотре в зеркалах – влагалище узкое, нерожавшее. Шейка матки конической формы, чистая. Выделения из половых путей – бели умеренные. Бимануальное гинекологическое исследование: матка обращена кпереди, грушевидной формы с четкими контурами, безболезненная при пальпации, придатки с обеих сторон не определяются. Результаты клинико-лабораторных исследований: общий анализ крови, общий анализ мочи, биохимический анализ крови в пределах нормы.
Проведен инфекционный скрининг. В ПЦР-анализе урогенитального соскоба обнаружена ДНК Cytomegalovirus, Gardnerella vaginalis. В посеве из цервикального канала с учетом чувствительности возбудителей к антибиотикам – избыточный рост Ureaplasma spp. – 10 5 КОЕ, Mycoplasma hominis – 10 5 КОЕ. В нативном мазке из влагалища – ключевые клетки, pH – 7.0. Дважды, с интервалом не менее четырех недель [8], определена концентрация гормонов в крови: ФСГ – 40 МЕ/л, Е2 – 18 пг/мл, прогестерон – 0,69 нмоль/л, лютеинизирующий гормон (ЛГ) – 20 МЕ/л. Проведена оценка овариального резерва: АМГ – 1,06 нг/мл (уровень АМГ
Что такое дисфункция яичников? Причины возникновения, диагностику и методы лечения разберем в статье доктора Салаева Г. Д., репродуктолога со стажем в 11 лет.
Определение болезни. Причины заболевания
Дисфункция яичников — это различные нарушения гормональной функции яичников, при которых овуляция происходит редко, нерегулярно или отсутствует.
По МКБ-10 (Международной классификации болезней) дисфункцию яичников кодируют как E28. В эту группу заболеваний включают:
Распространённость
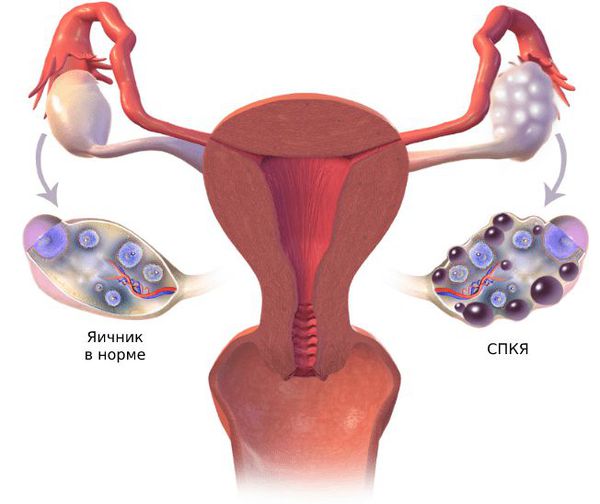
Cиндромом поликистозных яичников страдают:
Причины дисфункции яичников
Функции яичников нарушаются при заболеваниях щитовидной железы, гипофиза и гипоталамуса, стрессах и психических расстройствах, прерванной беременности, акклиматизации и приёме лекарственных препаратов, воздействующих на репродуктивную систему. Чтобы установить точную причину патологии, нужно посетить доктора и сдать анализы.
Причины синдрома поликистозных яичников:
Причины преждевременной недостаточности яичников:
Причины избытка эстрогенов:
Причины избытка андрогенов:
Симптомы дисфункции яичников
Дисфункция яичников — частая причина нарушения менструального цикла. В норме у женщины должно быть не менее восьми менструаций в год.
Признаки нарушения менструального цикла:
Эти симптомы могут быть признаками и других заболеваний, поэтому при их появлении нужно обратиться к врачу для уточнения диагноза.
Симптомы ПНЯ и СПКЯ могут быть схожи.
Основное отличие ПНЯ — это признаки снижения или прекращения работы яичников :
Признаки избытка андрогенов:
Признаки избытка эстрогенов:
Патогенез дисфункции яичников
К дисфункции яичников приводят гормональные нарушения в организме женщины.
Гормоны, ответственные за работу яичников:
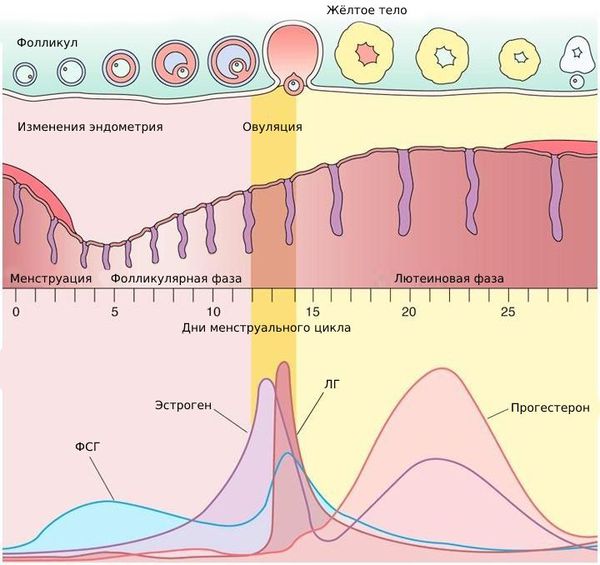
Каждой фазе менструального цикла соответствует определённый уровень этих гормонов. Если они в норме, то фолликул созревает и происходит овуляция. В дальнейшем наступает беременность, либо начинается менструация.
При дисфункции яичников процесс овуляции нарушается. Менструальный цикл сбивается и не проходит все необходимые фазы.
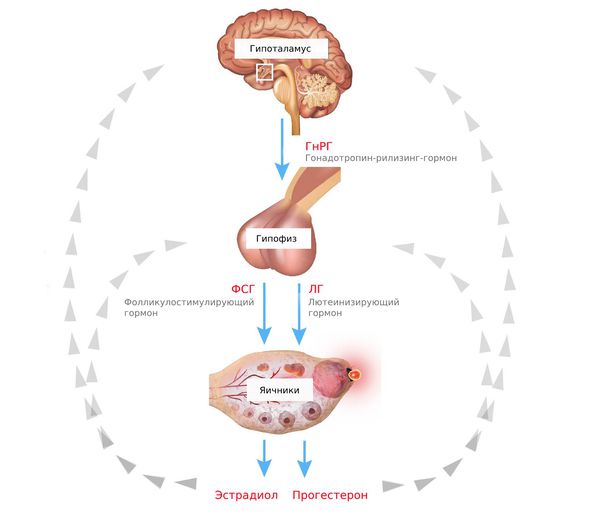
Подобные нарушения происходят при патологических изменениях в оси гипоталамус — гипофиз — яичники, которая является основой женской репродуктивной системы.
Гипоталамо-гипофизарно-яичниковая система передаёт сигналы от головного мозга главной эндокринной железе женских половых органов — яичникам — и получает от них обратную связь. Например, для СПКЯ характерна повышенная активность данной оси.
Правильная работа этой системы обеспечивает:
Классификация и стадии развития дисфункции яичников
Термин «дисфункция яичников» сборный, к нему относятся следующие состояния:
В зависимости от возраста пациентки выделяют:
Дисфункция также может быть физиологической:
Эти дисфункции не являются патологией и со временем проходят самостоятельно.
Недостаточность яичников по причине патологии:
По клиническому течению:
Признаки полового созревания: начало менструаций, рост молочных желёз, оволосение подмышечной области и лобка.
Осложнения дисфункции яичников
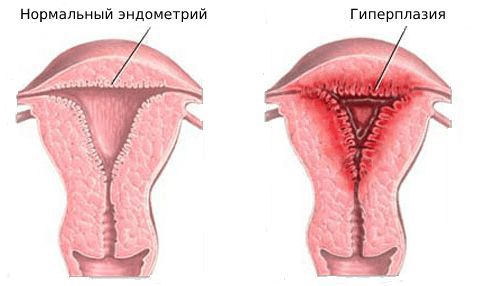
Гиперплазия эндометрия — это чрезмерное увеличения объёма и толщины внутренней оболочки матки. В отличие от рака эндометрия этот процесс является доброкачественным, но может приводить к повторяющимся кровотечениям.
Помимо нарушений со стороны репродуктивной системы, дисфункция яичников часто сопровождается:
Преждевременная недостаточность яичников связана с риском развития остеопороза и частыми переломами. Это вызвано тем, что при ПНЯ снижается уровень женских гормонов эстрогенов, замедляется обмен веществ и, как следствие, возникает дефицит минералов и витаминов.
Диагностика дисфункции яичников
Цель обследования — установить истинную причину дисфункции яичников.
Алгоритм диагностики состоит из трёх этапов:
У всех пациенток с нарушением менструального цикла и симптомами дефицита женских половых гормонов необходимо исключить ПНЯ.
Диагностика синдрома истощения яичников
Признаки синдрома истощения яичников:
Диагностика синдрома поликистозных яичников
Методы диагностики СПКЯ:
Основной признак гиперандрогении — чрезмерный рост тёмных, жёстких и длинных волос на подбородке, верхней части груди, спине и животе. Акне и выпадение волос на голове не являются самостоятельными критериями СПКЯ, но их учитывают при сочетании с другими симптомами.
Нарушение овуляции можно заподозрить при продолжительности цикла менее 21 дня или более 35 дней.
Диагностика гиперэстрогении
Симптомы миомы матки разнообразны:
Эндометриоз проявляется мажущими кровянистыми выделениями коричневого цвета, которые начинаются за несколько дней до менструации. Задолго до её начала возникают сильные тянущие боли внизу живота.
Для выявления гиперэстрогении потребуются анализы крови на эстрадиол, ФСГ, свободный эстриол и прогестерон. Их результаты оценивает врач-эндокринолог или гинеколог-эндокринолог.
Лечение дисфункции яичников
Цели лечения дисфункции яичников:
Лечение гормональными контрацептивами
Если женщина не планирует беременность, то первая линия терапии при СПКЯ — комбинированные гормональные контрацептивы: оральные (КОК), пластыри и вагинальные кольца. Препараты снижают выработку яичниками мужских половых гормонов. Поэтому их применение особенно актуально для женщин с нарушениями менструального цикла, избыточным оволосением и акне. Гормональные контрацептивы являются препаратами выбора для коррекции проявлений СПКЯ, однако официально для этого они не зарегистрированы.
Лечение метформином
Лечение акне
Изотретиноин способен нарушать нормальный ход развития плода и вызывать у него пороки, поэтому при его приёме необходима контрацепция.
Критерии эффективности лечения:
После лечения женщинам, которые не заинтересованы в беременности, рекомендуются методы контрацепции. Их подбирают индивидуально с акушером-гинекологом.
Дисфункция яичников и планирование беременности
Если женщина планирует беременность, то основная цель лечения — восстановить овуляцию и менструальный цикл. Этого добиваются, применяя индукцию овуляции, — медикаментозную стимуляцию созревания яйцеклетки.
При неэффективности или невозможности использовать кломифена цитрат искусственная стимуляция проводится гонадотропинами (как правило, ФСГ) или рекомендуется хирургическое лечение — лапароскопия. Гонадотропины также применяются шесть циклов.
Показания к лапароскопии у женщин с бесплодием:
Если овуляция отсутствует через 12 недель после лапароскопии, то рекомендуется принимать кломифена цитрат. При его неэффективности в течение трёх месяцев можно использовать гонадотропины. Если вышеперечисленные методы не привели к беременности, а также при сопутствующих патологиях или необходимости преимплантационной генетической диагностики, применяют экстракорпоральное оплодотворение (ЭКО).
Дисфункция яичников и ЭКО
Преимплантационная генетическая диагностика позволяет выявить генетические заболевания эмбриона перед его переносом в слизистую оболочку матки. Проводится только в рамках программы ЭКО. Однако в рутинной практике метод не применяется — показаний для молодых пациенток со СПКЯ в программе ЭКО для такой диагностики нет.
При ЭКО частота наступления беременности на лечебный цикл у женщин со СПКЯ сопоставима с таковой у пациенток без этого заболевания.
Снижение веса
Для снижения веса при ожирении, избыточной массе тела и для профилактики сердечно-сосудистых заболеваний и сахарного диабета 2-го типа рекомендовано заниматься физическими упражнениями и соблюдать диету.
Изменение образа жизни для пациенток с ожирением позволит отсрочить развитие сахарного диабета.
При регулярных тренировках с частотой сердечных сокращений (ЧСС) более 80 % от максимальной у пациенток со СПКЯ повышается чувствительность к инсулину.
Максимальная ЧСС = 220 − возраст женщины
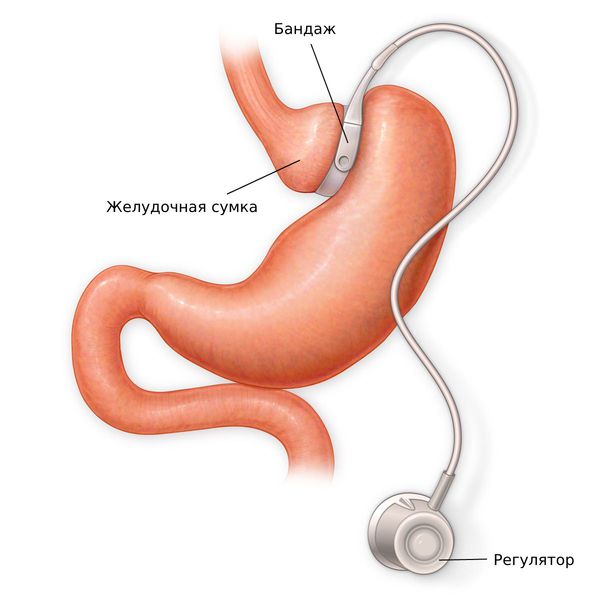
Виды бариатрических операций:
Лечение заместительной гормональной терапией
Недостаточность яичников вне зависимости от симптомов дефицита эстрогена — показание для непрерывного приёма заместительной гормональной терапии (ЗГТ). Препараты используются до менопаузы, после чего дозу пересматривают.
Для этого применяют следующие препараты:
Методы, которые с доказанной эффективностью восстановят функции яичников и способность к зачатию при ПНЯ, не разработаны. Несмотря на многообещающие результаты экспериментальных исследований, единственным надёжным способом забеременеть для таких пациенток пока остаётся ЭКО с донорскими яйцеклетками.
Прогноз. Профилактика
Прогноз при дисфункции яичников благоприятный. Однако ПНЯ негативно влияет не только на репродуктивную сферу, но и на качество жизни, общую заболеваемость и смертность женщин.
Снижение веса и регулярные физические упражнения помогут уменьшить тяжесть СПКЯ.
Специфических методов профилактики избытка женских половых гормонов и андрогенов не существует. Рациональное и сбалансированное питание, физическая активность и отказ от курения помогут избежать развития сопутствующих болезней.