Что такое время плазмолиза
Что такое время плазмолиза
Работа 1. Плазмолиз и деплазмолиз. Формы плазмолиза
Плазмолиз – процесс отделения протопласта от оболочки клетки, погруженной в гипертонический раствор, то есть раствор, концентрация солей которого больше таковой клеточного сока.
В зависимости от разницы концентраций внутреннего и внешнего растворов и длительности процесса проявляются разные формы плазмолиза 1 : уголковый, вогнутый, судорожный, выпуклый (рис. 1, А). Уголковый плазмолиз проявляется в форме отхождения протопласта от клеточной оболочки только по ее углам. При вогнутом плазмолизе протопласт остается в соприкосновении с клеточной оболочкой в некоторых местах; резко выраженной его формой является судорожный плазмолиз. Самая глубокая стадия – выпуклый плазмолиз – наступает, когда протопласт отходит от оболочки полностью и принимает вид комочка с выпуклой поверхностью. Часто на последней стадии видны тончайшие нити протопласта («нити Гехта»), соединяющие последний со стенками клетки (рис. 1, Б).
Деплазмолиз – процесс, обратный плазмолизу, проявляющийся в восстановлении нормального состояния клетки при перенесении ее в чистую воду. Если раствор, вызывающий плазмолиз, не ядовит, то явление плазмолиза и деплазмолиза можно наблюдать несколько раз.
В настоящее время явление плазмолиза широко используется в экспериментальной цитологии и физиологии растений для определения осмотического потенциала, вязкости цитоплазмы, клеточной проницаемости и многих других вопросов.
Материалы и оборудование. Луковица с пигментированными чешуями, 0,7 М раствор нитрата кальция, 0,5 М раствор хлорида кальция, 1,0 М раствор сахарозы, дистиллированная вода, предметные стекла, покровные стекла, стеклянные трубочки, фильтровальная бумага, набор для препарования, спиртовка, микроскоп «Биолам 70-Р».
Ход работы. Приготовьте водный препарат нижнего эпидермиса синего лука, накройте покровным стеклом и рассмотрите под микроскопом на малом увеличении. Сделайте схематический рисунок наблюдаемой картины. Удалите с помощью фильтровальной бумаги воду и замените ее на имеющийся в наличии гипертонический раствор (0,7 М Ca(NO3)2, 0,5 М CaCl2 или 1,0 М C12H22O11). Сразу после нанесения раствора на стекло начните наблюдения. Дождитесь появления всех этапов плазмолиза (уголковый, вогнутый, выпуклый). Заполните таблицу 1 по результатам опыта.
Скорость проявления различных форм плазмолиза
Тема 1 Влияние анионов и катионов на форму и время плазмолиза
Цель: определить время наступления фаз плазмолиза.
Теоретические сведения
Плазмолиз – отставание цитоплазмы от стенок клетки, помещенной в раствор с большей концентрацией, чем концентрация клеточного сока (гипертонический раствор). В ходе плазмолиза очертания поверхности меняются: сначала она сокращается, а после полной потери тургора протопласт отстает от клеточной стенки по углам (уголковый плазмолиз), затем во многих местах (вогнутый плазмолиз) и, наконец, протопласт округляется (выпуклый плазмолиз).
Временем плазмолиза называется период, который проходит с момента погружения ткани растения в раствор плазмолитика до наступления выпуклого плазмолиза. Этот показатель может характеризовать вязкость цитоплазмы: чем больше время плазмолиза, тем выше вязкость цитоплазмы.
Катионы и анионы солей оказывают специфическое и многообразное действие на цитоплазму. Одним из заметных внешних проявлений этого действия являются изменения в степени набухания и вязкости цитоплазмы, для наблюдения за которыми используют время плазмолиза.
Ход работы:Срез эпидермиса с выпуклой поверхности чешуи цветного лука помещают в каплю раствора испытуемой соли, накрывают покровным стеклом и сейчас же приступают к рассматриванию под микроскопом. Следят за сменой форм плазмолиза. Определяют время плазмолиза в каждой соли. Результаты опыта записывают по форме:
| Вариант | Соль | Концентрация раствора | Время погружения ткани в раствор | Время наступления выпуклого плазмолиза | Время плазмолиза (мин.) |
| Ca(NO3)2 | 0.7 | ||||
| KNO3 | 1.0 | ||||
| KCNS | 1.0 |
На основании полученных результатов делают выводы о влиянии катионов и анионов на вязкость цитоплазмы.
Литература:1, с.19
Контрольные вопросы:
1 Известно, что через клеточные мембраны проникают как вода, так и многие растворенные вещества. Почему тем не менее можно говорить о полупроницаемости мембран, хоть и не идеальной?
2 Какая мембрана обладает более низкой проницаемостью для растворенных веществ – плазмолемма или тонопласт?
Тема 2 Определение осмотического давления клеточного сока плазмолитическим методом
Цель:определить изотоническую концентрацию и вычислить осмотическое давление клеточного сока по уравнению Вант-Гоффа
Теоретические сведения
Клеточный сок – водный раствор различных органических и неорганических веществ. Потенциальное осмотическое давление зависит от числа частиц, находящихся в этом растворе, т.е. от концентрации и степени диссоциации растворенных молекул. Потенциальное осмотическое давление выражает максимальную способность всасывать воду. Величина этого показателя указывает на возможность произрастания растения на почвах различной водоудерживающей силы. Повышение осмотического давления клеточного сока при засухе является критерием обезвоживания растений и необходимости полива.
Данный метод основан на подборе такой концентрации наружного раствора, которая вызывает начальный (уголковый) плазмолиз в клетках исследуемой ткани. В этом случае, осмотическое давление раствора примерно равно осмотическому давлению клеточного сока. Такой раствор называется изотоническим.
Ход работы:В бюксы готовят по 10мл. 0,7М; 0,6М; 0,5М; 0,4М; 0,3М; 0,2М, растворов сахарозы путем разбавления 1M раствора дистиллированной водой. Растворы тщательно перемешивают. Бюксы закрывают крышками, чтобы предотвратить испарение, и ставят в ряд убывающей концентрации растворов.
Лезвием безопасной бритвы делают тонкие срезы с выпуклой поверхности чешуи лука размером примерно 25 мм 2 из среднего хорошо окрашенного участка.
В каждый бюкс, начиная с высокой концентрации, с интервалом в 3 мин. опускают по 2-3 среза. Через 30 мин. после погружения срезов в первый бюкс исследуют их под микроскопом. Затем, через каждые 3 мин. наблюдают под микроскопом срезы из последующих бюксов. Этим достигается равная продолжительность пребывания срезов в растворах плазмолитиков. Рассматривать срезы под микроскопом следует в капле раствора из того бюкса, откуда был взят срез.
Определяют степень плазмолиза клетки в каждом растворе и находят изотоническую концентрацию как среднее арифметическое между концентрацией, при которой плазмолиз только начинается, и при которой уже вызывает плазмолиз.
Результаты опыта записывают по форме таблицы
| Концентрация растворов сахарозы, М | На 10 мл раствора | Продолжительность пребывания срезов в растворе | Степень плазмолиза | Изотоническая концентрация, М | Потенциальное осмотическое давление, кПа |
| IМ сахарозы | воды, мл | время погружения | время наблюдения | ||
| 0,7 | |||||
| 0,6 | |||||
| 0,5 | |||||
| 0,4 | |||||
| 0,3 | |||||
| 0,2 |
Величину потенциального осмотического давления (в кПа) рассчитывают по формуле:
П = R*T*c*i*101,3;
где R – газовая постоянная, равная 0,0821л атм./град моль;
Т – абсолютная температура (273 о С + комнатная);
с – изотоническая концентрация в молях;
i – изотонический коэффициент Вант-Гоффа;
101,3 – множитель для перевода атмосфер в килопаскали.
Коэффициент Вант-Гоффа характеризует ионизацию растворов и для неэлектролитов (сахароза) равен 1.
Оборудование: луковица синего лука; 1 М раствор сахарозы, скальпель, лезвие бритвы, препаровальная игла, микроскоп, предметные и покровные стекла; карандаш по стеклу; фильтровальная бумага, пробирки (бюксы).
Литература: 1, с. 16-18.
Контрольные вопросы:
1 Что такое плазмолиз и каковы его причины?
2 Как происходит деплазмолиз?
3 Способны ли плазмолизироваться мертвые клетки?
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.
Что такое время плазмолиза
Известно, что одним из продуктов реакции медного купороса и желтой кровяной соли является полупроницаемая мембрана ферроцианида меди (II), которая хорошо пропускает молекулы воды и не пропускает молекулы CuSO4. Такая избирательная проницаемость мембраны способствует протеканию процесса осмоса, характерного, в том числе и для жизнедеятельности растительной клетки [4, c.306]. А сам эксперимент, проведенный в XIX веке Морицем Траубе, продемонстрировал, что в неживой природе неорганических веществ можно найти такие химические соединения, которые при взаимодействии образуют совершенное подобие растительной клеточки, способной вбирать в себя одни вещества из окружающей среды и выделять другие. По теории Траубе, рост полученных им искусственных клеточек происходит вследствие внутреннего гидростатического давления (тургор), которое играет важную роль в жизни растений. Таким образом, клеточки Траубе принято считать моделям живой клетки [9].
Еще в 1750г. русский ученный М.В. Ломоносов получал с помощью желтой кровяной соли удивительные по окраске малорастворимые в воде соединения, которые иногда называют «ферроцианидными солями Ломоносова», или «ферроцианидные кустарники Ломоносова». Эти изумительные растения, похожие на нитевидные водоросли формируются благодаря образованию на поверхности кристалликов желтой кровяной соли полупроницаемой пленки [1, c.126-127].
2. Теоретическая часть
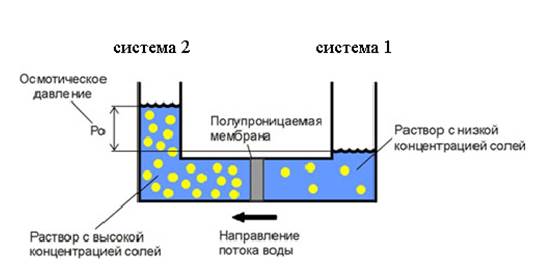
Явление осмоса наблюдается при наличии двух систем с различной концентрацией веществ, где подвижность растворителя больше подвижности растворённых веществ. Важным частным случаем осмоса является осмос через полупроницаемую мембрану, когда они сообщаются с помощью полупроницаемой мембраны. В этом случае по законам термодинамики выравнивание концентраций происходит за счет вещества, для которого мембрана проницаема.
Полупроницаемыми называют мембраны, которые имеют достаточно высокую проницаемость не для всех, а лишь для некоторых веществ, в частности, для растворителя [13, с.228]. (Подвижность растворённых веществ в мембране относительно мала). Как правило, это связано с размерами и подвижностью молекул, например, молекула воды меньше большинства молекул растворённых веществ. Если такая мембрана разделяет раствор и чистый растворитель, то концентрация растворителя в растворе оказывается менее высокой, поскольку там часть его молекул замещена на молекулы растворённого вещества. Вследствие этого переходы частиц растворителя из отдела, содержащего чистый растворитель, в раствор, будут происходить чаще, чем в противоположном направлении. Соответственно, объём раствора будет увеличиваться (а концентрация вещества уменьшаться), тогда как объём чистого растворителя будет, соответственно, уменьшаться (рис.1).
При рассмотрении двух систем с различной концентрацией по сторонам полупроницаемой мембраны выравнивание концентраций в системе 1 и 2 возможно только за счет перемещения воды. В системе 1 концентрация воды выше, поэтому поток воды направлен от системы 1 к системе 2. По достижении равновесия реальный поток будет равен нулю [12, с.188]
Рис. 1 Схема формирования осмотического давления
В случаях, когда мембрана проницаема не только для растворителя, но и для некоторых растворённых веществ, перенос последних из раствора в растворитель позволяет осуществить диализ, применяемый как способ очистки полимеров и коллоидных систем от низкомолекулярных примесей, например электролитов [15, c.38-56].
Осмос играет важную роль во многих биологических процессах. Мембрана, окружающая нормальную клетку крови, проницаема лишь для молекул воды, кислорода, некоторых из растворённых в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворённом состоянии внутри клетки, она непроницаема. Поэтому белки, столь важные для биологических процессов, остаются внутри клетки.
Осмос участвует в переносе питательных веществ в стволах высоких деревьев, где капиллярный перенос не способен выполнить эту функцию [3,с. 117].
Клетки растений используют осмос также для увеличения объёма вакуоли, чтобы она распирала стенки клетки (тургорное давление). Клетки растений делают это путём запасания сахарозы. Увеличивая или уменьшая концентрацию сахарозы в цитоплазме, клетки могут регулировать осмос [6, с.66]. За счёт этого повышается упругость растения в целом. С изменениями тургорного давления связаны многие движения растений (например, движения усов гороха и других лазающих растений).
Таким образом, осмос играет важную роль в жизни растительной клетки.
Б) Растительная клетка как осмотическая система
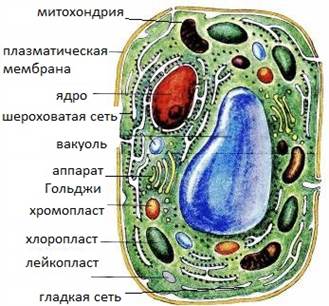
Рис.2 Растительная клетка
Растительную клетку можно рассматривать как осмотическую систему. Клеточная стенка обладает определенной эластичностью и может растягиваться. В вакуоли накапливаются растворимые в воде вещества (сахара, органические кислоты, соли), которые обладают осмотической активностью. Клеточный сок вакуоли является высококонцентрированным раствором. Тонопласт (от греч. tonos – натяжение, напряжение и plastos – оформленный, вылепленный) – мембрана, ограничивающая вакуоль растительной клетки [12, с.138].
Тонопласт и клеточная мембрана выполняют в данной системе функцию полупроницаемой мембраны, поскольку эти структуры избирательно проницаемы, и вода проходит через них значительно легче, чем вещества, растворенные в клеточном соке и цитоплазме [17, c.98].
Чтобы попасть в вакуоль, вода должна пройти через клеточную стенку, плазмалемму, цитоплазму и тонопласт. Клеточная стенка хорошо проницаема для воды [8, c.65]. Плазмалемма и тонопласт обладают избирательной проницаемостью, являются полупроницаемой мембраной, а вакуоль с клеточным соком – концентрированным раствором. Поэтому, если клетку поместить в воду, то вода по законам осмоса начнет поступать внутрь клетки.
Тургорное давление – внутреннее давление, которое развивается в растительной клетке, когда в неё в результате осмоса входит вода, и цитоплазма прижимается к клеточной стенке; это давление препятствует дальнейшему проникновению воды в клетку [6, с.66].
Эластическое растяжение ткани благодаря тургорному давлению ее клеток придает твердость неодревесневшим частям растений. Завядающие побеги становятся дряблыми, так как при потере воды тургорное давление падает. Тургорное давление противодействует притоку воды в клетку. Давление, с которым вода осмотически притекает в клетку, равно, таким образом, разности осмотического давления и тургорного давления.
В связи с этим, если клетка попадает в окружающую среду, где концентрация осмотически активных веществ (электролиты, неэлектролиты, белки) будет меньше по сравнению с концентрацией внутри клетки (или клетка помещена в воду), вода по законам осмоса должна поступать внутрь клетки.
Наблюдения за явлениями плазмолиза и тургора позволяют ученым изучать многие свойства клетки. Явление плазмолиза показывает, что клетка жива и протоплазма сохранила полупроницаемость. По скорости и форме плазмолиза можно судить о вязкости протоплазмы. Также явление плазмолиза позволяет определить величину осмотического давления (плазмолитический метод) [7, с. 135].
Осмотическое давление различно у разных жизненных форм. У древесных пород оно выше, чем у кустарников, а у кустарников выше, чем у травянистых растений. Разные экологические группы различаются по величине осмотического давления. Особенное значение имеет снабжение растений водой. У растений пустынь осмотическое давление больше, чем у степных растений. У степных — больше, чем у луговых. Еще меньше осмотическое давление у растений болотных и водных местообитаний. У светолюбивых растений осмотическое давление больше, чем у теневыносливых. Растение в определенной степени регулирует величину осмотического давления. Ферментативное превращение сложных нерастворимых веществ в растворимые (крахмала в сахара, белков в аминокислоты) приводит к возрастанию концентрации клеточного сока и повышению осмотического давления.
Однако, говоря о поступлении воды в клетку, надо учитывать, что наряду с осмотическим давлением в клетках существует давление набухания. Давление набухания связано со способностью гидрофильных коллоидов притягивать к себе молекулы воды. Сила, с которой коллоиды притягивают воду, и представляет собой давление набухания. Большое значение давление набухания имеет для молодых меристематических клеток, в которых отсутствуют вакуоли и которые заполнены коллоидным веществом [2, с.407].
В) Мориц Траубе, изучение тургорного давления
По окончании гимназии занимался в Берлине естественными науками и специально химией под руководством Е. Митчерлиха, Г. Розе и Раммельсбурга. Из Берлина Траубе перешел в Гиссен, где занимался в лаборатории Либиха. В 1846 г. Траубе. снова вернулся в Берлин, и через род получил степень доктора философии за химическую диссертацию «De nonnullis Chromii connubiis». Чтобы приобрести практические сведения. Траубе поступил на одну берлинскую красильню, но вскоре вернулся в Ратибор.
После смерти отца, он продолжал его дело (виноторговля) и досуги посвящал любимым занятиям теоретической химией. Его работы, сделанные в маленьком Ратиборе, вдали от общения с учеными, поразительны, отличаясь замечательной ясностью, логичностью мышления и новизной идей.
С 1851 по 1894 г. Траубе опубликованы 42 монографии, в которых он высказал совершенно новые взгляды на процессы брожения, нашедшие блестящее подтверждение в работах последних десятилетий. Процессы брожения вызываются, по мнению Траубе, не самими организмами брожения (дрожжами), но теми ферментами, которые эти организмы вырабатывают и выделяют в окружающую среду.
Громадное влияние на общую физиологию оказало открытие Траубе, касающееся образования растительных клеток. До того существовало представление, что в образовании, питании и росте клеток играют главную роль исключительно жизненные процессы.
Опыты Траубе показали, что можно найти такие неорганические химические соединения, которые при взаимодействии образуют совершенное подобие растительной клеточки, способной вбирать в себя одни вещества из окружающей среды и выделять другие. По теории Траубе, рост клеточек происходит вследствие внутреннего гидростатического давления (тургор).
Во внимание к трудам Траубе университет в Галле преподнес ему в день празднования своего 300-летнего юбилея в 1874 г., диплом на степень Dr. med. et chir. Не занимая никогда профессорского места, числясь корреспондентом Берлинской академии наук в течение всей своей жизни, Траубе не прерывал занятий наукой и умер среди начатых работ [5].
3. Практическая часть
А) Эксперимент с медным купоросом и желтой кровяной солью
Данный эксперимент имеет недостаток – в нём используются редкий, токсичный реактив – желтая кровяная соль [10, c.90]. Поэтому этот эксперимент ученики не смогут при желании повторить дома.
Используемые реактивы и оборудование:
В химическом стакане приготовим 5% раствор CuSO4. Для этого растворим при помешивании 15 г соли в 285 мл дистиллированной воды при комнатной температуре. Наблюдаем появление голубого мутного раствора CuSO4 в воде. Для подавления гидролиза сульфата меди по катиону в водном растворе, добавляем в стакан несколько крупинок лимонной кислоты. Наблюдаем, что раствор стал прозрачным. Это очень удобно для наблюдения процессов формирования клеточек Траубе.
После этого пинцетом поместим небольшой кристаллик желтой кровяной соли на дно стакана. Наблюдаем рост клеточки Траубе.
Рис.4. Рост клеток Траубе в растворе медного купороса.
Объяснение наблюдаемых процессов:
2 CuSO4 + K4[Fe(CN)6] ®Cu2[Fe(CN)6] + 2 K2SO4
Концентрация желтой кровяной соли внутри клетки больше, чем концентрация сульфата меди снаружи. В результате вода проникает в клетку, тем самым увеличивая ее до тех пор, пока концентрации желтой кровяной соли и сульфата меди не уравняются. За счет давления мембрана из гексацианоферрата(II) меди постоянно разрывается. На месте разрыва опять взаимодействуют сульфат меди и желтая кровяная соль, и пленка образуется снова. Поэтому клеточка Траубе растет неравномерно.
Б) Эксперимент с хлоридом железа (III) и силикатным клеем
Данный эксперимент еще называется «Силикатный сад» и имеет преимущество перед предыдущим в плане большей доступности реактивов. Так силикатный клей можно приобрести в канцелярском магазине, а реактив FeCl3 в магазине для радиолюбителей (он используется при пайке радиодеталей). Поэтому этот эксперимент ученики смогут при желании повторить у себя дома неограниченное количество раз, наблюдая, как на скорость и размер «водорослей» влияет разная концентрация силикатного клея в воде и размеры кристаллов хлорида железа (III).
Реактивы и оборудование:
Смешиваем силикатный клей и воду в соотношении 1:1. Насыпаем в полученный раствор немного соли FeCl3. Наблюдаем, как из кристалликов соли постепенно вырастают красивые «водоросли».
Рис.5. Рост клеток Траубе в силикатном растворе.
Объяснение наблюдаемых процессов:
Силикаты многих металлов плохо растворить в воде. Клей содержит относительно хорошо растворимые силикаты калия и натрия. В реакции обмена образуются силикаты железа, которые в водном растворе сразу же подвергаются гидролизу с образованием нерастворимого гидроксида железа (III)
2FeCl3 +3Na2SiO3 ® Fe2(SiO3)3 + 6NaCl
Fe2(SiO3)3 + 6H2O ® 2Fe(OH)3¯ + 3H2SiO3
Клеточная мембрана живой клетки обладает свойством полупроницаемости. Это явление демонстрируется в опыте с искусственной клеткой Траубе.
Изучена сущность осмотических процессов и проведены эксперименты по воздействию гипертонических, гипотонических и изотонических растворов на живые клетки с применением модельной клеточки Траубе.
Сделано заключение о том, что получение клеточки Траубе с применением силикатного водного раствора и хлорида железа (III) более доступно и безопасно для школьников, чем способ с использованием медного купороса и желтой кровяной соли при проведении подобного эксперимента в домашних условиях.
Плазмолиз
Плазмолиз (от др.-греч. πλάσμα — вылепленное, оформленное и λύσις — разложение, распад), отделение протопласта от клеточной стенки в гипертоническом растворе.
Плазмолизу предшествует потеря тургора.
Плазмолиз возможен в клетках, имеющих плотную клеточную стенку (у растений, грибов, крупных бактерий [1] ). Клетки животных, не имеющие жесткой оболочки, при попадании в гипертоническую среду сжимаются, при этом отслоения клеточного содержимого от оболочки не происходит. Характер плазмолиза зависит от ряда факторов:
Различают уголковый плазмолиз, при котором отрыв протопласта от стенок клетки происходит на отдельных участках, выпуклый плазмолиз, когда отслоение захватывает значительные участки плазмалеммы, и вогнутый, полный плазмолиз, при котором связи между соседними клетками разрушаются практически полностью. Выпуклый плазмолиз часто обратим; в гипотоническом растворе клетки вновь набирают потерянную воду, и происходит деплазмолиз. Вогнутый плазмолиз обычно необратим и ведет к гибели клеток.
Выделяют также судорожный плазмолиз, подобный выпуклому, но отличающийся от него тем, что сохраняются цитоплазматические нити, соединяющие сжавшуюся цитоплазму с клеточной стенкой, и колпачковый плазмолиз, характерный для удлиненных клеток.
Содержание
Методы оценки
Есть 2 способа сравнительной оценки плазмолиза в тканях:
В первом методе, который создал Хуго Де Фриз, ткани погружаются в растворы KNO3, сахарозы или других осмотически активных веществ разной концентрации, и определяется концентрация, при которой плазмолизируется 50 % клеток. Плазмометрический метод заключается в измерении после плазмолиза относительных объёмов клетки и протопласта и вычислении по концентрации раствора осмотического давления клетки.
История исследований
Наблюдая за плазмолизом, голландский ботаник Хуго Де Фриз в 1877 году впервые измерил осмотическое давление в клетках растений.
Примечания
Ссылки
Полезное
Смотреть что такое «Плазмолиз» в других словарях:
плазмолиз — плазмолиз … Орфографический словарь-справочник
плазмолиз — сущ., кол во синонимов: 1 • отделение (129) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
ПЛАЗМОЛИЗ — ПЛАЗМОЛИЗ, сморщивание протопласта, от хождение его от клеточной целлюлезной оболочки, наблюдающееся при погружении растительной клетки, окруженной твердой стенкой, в гипертонический раствор какого либо вещества. Если клетку затем перенести в… … Большая медицинская энциклопедия
плазмолиз — Отделение пристеночного слоя цитоплазмы от твердой оболочки растительной клетки в гипертоническом по отношению к клеточному соку растворе; при возвращении нормальных осмотических условий тургор клетки обычно восстанавливается (при резком П.… … Справочник технического переводчика
плазмолиз — plasmolysis плазмолиз. Oтделение пристеночного слоя цитоплазмы от твердой оболочки растительной клетки в гипертоническом по отношению к клеточному соку растворе; при возвращении нормальных осмотических условий тургор клетки обычно… … Молекулярная биология и генетика. Толковый словарь.
ПЛАЗМОЛИЗ — (plasmolysis) протекающий в организме бактерий и растений процесс, который характеризуется отслаиванием протоплазмы от плотной клеточной стенки при помещении клетки в гипертонический раствор. Плазмолиз протекает благодаря удалению из клетки воды… … Толковый словарь по медицине
плазмолиз — (plasmolysis; плазмо + греч. lysis распад, растворение; син. плазмолизис) 1) потеря воды клеткой в гипертоническом растворе, сопровождающаяся отслоением протоплазмы от клеточной оболочки; 2) стадия цитолиза, заключающаяся в разжижении протоплазмы … Большой медицинский словарь