Что такое впр цнс
Врожденные пороки ЦНС
Нормальное внутриутробное формирование плода может быть нарушено генетическими дефектами, инфекционными заболеваниями типа краснухи, ВИЧ, цитомегаловируса, интоксикацией алкоголем, наркотиками, некоторыми лекарственными средствами, воздействием вредного излучения и т.д. Негативное воздействие подобных эндогенных и экзогенных факторов особенно опасно в течение первого триместра беременности, поскольку плацента находится в состоянии формирования и не может полноценно выполнять свою защитную функцию.
Формирование нервной системы эмбриона начинаются с первых 10 дней, когда начинает дифференцироваться нервная ткань. Нервная трубка (ЦНС) и спинномозговые нервы формируются на 4-5-й неделе, мозговые пузыри – на 4-5-й неделе, кора большого мозга – на 6-8-й неделе, конечный мозг – на 7-8-й. Полностью мозговые структуры формируются только в конце внутриутробного развития. В связи с такими особенностями поражение органов нервной системы может произойти на любом этапе созревания плода.
В зависимости от срока воздействия негативных факторов у плода могут возникнуть различные дефекты развития нервной системы – как центральной, так и периферической, с аномалиями головного мозга, спинного мозга, позвоночника и черепа.
Виды пороков развития нервной системы
Врожденные пороки развития ЦНС занимают второе место после пороков развития опорно-двигательного аппарата. По статистике, из двух тысяч зарегистрированных новорожденных трое рождаются с врожденными аномалиями нервной системы.
Среди врожденных пороков ЦНС можно выделить часто встречающиеся в генетической и гинекологической практике группы с аномалиями различных участков центральной нервной системы.
Пороки развития головного мозга
К врожденным аномалиям внутриутробного формирования головного мозга, которые приводят к гибели плода или инвалидности новорожденного, относятся:
Сочетанные аномалии развития головного мозга и черепа
Взаимосвязанность формирования черепной коробки и развития мозга приводят к различным сочетанным дефектам:
Пороки развития позвоночника и спинного мозга
Среди врожденных аномалий нервной системы человека значительное место занимают патологии, вызванные пороками развития позвоночного столба и спинного мозга. Чаще всего причиной этих пороков становятся нарушения закрытия заднего конца нервной трубки, которое происходит на 4-й неделе формирования плода. Общее для всех этих аномалий – незаращение дуги позвонков, или spina bifida, что становится причиной спинномозговых грыж с различным содержимым грыжевого выпячивания:
Это далеко не полный список пороков развития ЦНС, которые приводят к мертворождению, гибели новорожденного в первые месяцы жизни или тяжелым уродствам.
Генетическая диагностика нарушений ЦНС в НИАРМЕДИК
В генетических отделениях многопрофильной медицинской сети НИАРМЕДИК проводится эффективное генетическое обследование в рамках подготовки к зачатию и пренатальный скрининг – в разные периоды беременности, которые позволяют с большой точностью выявить пороки в развитии органов и систем плода.
Показаниями для консультации у врача-генетика являются:
Центральные и районные генетические отделения и лаборатории сети предоставляют пациентам пройти полный цикл аппаратного обследования и лабораторного молекулярно-генетического исследования.
Виды пренатального скрининга в НИАРМЕДИК
На первую медико-генетическую консультацию к врачу-генетику рекомендуется приходить парой, поскольку проблемы аномалий развития ЦНС могут присутствовать в семьях мужчины и женщины или в роду обоих супругов. На основании тщательного сбора анамнеза и предварительного диагноза врач назначает дородовую диагностику будущей мамы и плода.
Обследование беременной относится к непрямым методам, куда кроме уже упомянутой медико-генетической консультации входят сбор и изучение акушерского и гинекологического анамнезов, бактериологические и серологические исследования в Центре лабораторной диагностики НИАРМЕДИК.
Пациентка проходит биохимические скрининговые тесты, которые определяют содержание эстриола, фетопротеина, хорионического гонадотропина и других белков, и гормонов в организме беременной, которые способствуют определению группы риска по порокам развития плода, но 100 % гарантии их наличия не дают.
Исследование плода проводится инвазивными и неинвазивными методами. Основной неинвазивный метод обследования – ультразвуковая или эхографическая диагностика.
УЗИ-диагностика центральной нервной системы и спинного мозга плода проводится в каждом триместре беременности. Конкретные сроки обследования связаны со сроками проявления различных патологий ЦНС при формировании органов и систем. По итогам эхографической диагностики врач-генетик оценивает:
Для изучения состояния сосудов головного мозга плода применяются технологии цветового допплеровского картирования (ЦДК).
Такое обследование плода в сочетании с результатами биохимических скрининговых тестов женщины повышают точность диагностики при наличии пороков до 90%, поскольку в сети клиник НИАРМЕДИК применяются инновационные ультразвуковые сканеры экспертного класса и трансвагинальная эхография с трехмерным и четырехмерным режимами изображения.
Для подтверждения диагноза применяются инвазивные методики генетического исследования околоплодных вод (амниоцентез), пуповинной крови (кордоцентез), ворсин хориона.
Забор амниотической жидкости (околоплодных вод) и пуповинной крови производится специальной иглой под видеоконтролем. Прокол при амниоцентезе проводится на 8-14 неделе беременности через брюшную стенку, при кордоцентезе – на 22-24 неделе, когда кровеносные сосуды достаточно развиты для инъекции. В этом случае забор крови берется через брюшную стенку или шейку матки.
Биопсия ворсин хориона (наружной оболочки эмбриона) проводится биопсийной иглой через брюшную стенку или с помощью гибкого зонда – через шейку матки на 10-12 неделе.
В пуповинной крови и околоплодных водах содержатся клетки плода, а клетки ворсинок наружной оболочки зародыша аналогичны его собственным клеткам. Генетическое исследование этих клеток дает возможность диагностировать пороки ЦНС с уровнем точности, достигающим 99%.
Записаться на прием к врачу-генетику многопрофильной сети клиник НИАРМЕДИК можно, позвонив по единому номеру телефона контакт-центра или отправив заявку на запись через обратную форму связи на сайте.
Что такое впр цнс
Возможности активного лечения мальформаций мозга ограничены. Вызывающие гидроцефалию пороки развития эффективно купируются с помощью вентрикуло-перитонеального шунтирования или других шунтирующих операций. Тем не менее, и в этих случаях после успешной операции могут сохраняться нарушения развития нервной системы из-за сопровождающей гидроцефалию диффузной патологии. За последние десятилетия наметился существенный прогресс в медикаментозном лечении эпилепсии.
Хирургическое вмешательство, особенно при эпилептогенных дисплазиях, в некоторых случаях стало практически возможным и будет совершенствоваться, но еще недостаточно используется. Однако для многих пациентов основным методом лечения остаются реабилитация и физиотерапия. Во многих случаях требуется специальное обучение, а также необходима создание организационной базы для самых тяжелых больных.
Предупреждение мальформаций ЦНС — одно из главных направлений детской неврологии на ближайшие годы. Современный уровень знаний позволяет проводить первичную профилактику дефектов нервной трубки назначением фолиевой кислоты. Кроме первичной профилактики, основными доступными профилактическими мерами являются генетическое консультирование и пренатальная диагностика.
Генетическое консультирование необходимо для точной диагностики определенных энцефалопатий и установления различных типов наследования (Lie et al., 1994). Основные достижения в нейровизуализации (D’Incerti, 2003; Garel, 2004; Gressens и Luton, 2004), особенно MPT плода, позволили увидеть самые важные синдромные мальформации, такие как полимикроги-рия и некоторые «малые» пороки развития, которые очень сложно или невозможно было диагностировать прежде. В идеале для эффективности генетического консультирования диагноз мальформации ЦНС должен быть не только точным, но и ранним.
Генетика самых распространенных мальформаций ЦНС обычно не соответствует простым менделевским закономерностям. В таблице ниже перечислены некоторые главные генетические пороки развития ЦНС и типы наследования. Тем не менее, все большее число мальформаций, прежде считавшихся спорадическими, оказываются иногда генетически определенными и несколько синдромов точно определены как негенетические. Так обстоит дело в большинстве несиндромных случаев агенезии мозолистого тела, при синдроме Айкарди, синдроме Денди-Уолкера и при кортикальных дисплазиях.
Желательно выявление других синдромов подобного типа. К сожалению, намного чаще синдромные мальформации имеют либо генетическое, либо экологическое происхождение и возможность разграничения этих механизмов пока не найдена. Хромосомное и МРТ обследование родителей, особенно матерей, целесообразно при некоторых обстоятельствах.
Пренатальная диагностика тяжелых аномалий мозга осуществима в основном при помощи ультрасонографии (Американская академия педиатрии, 1994, Aubry et al., 2003, Barnewolt и Estroff, 2004). Усовершенствование методов обеспечивает раннюю и точную диагностику. В большинстве центров сейчас возможно проведение МРТ плода, что позволяет более точно определить патологические особенности мальформаций (Garel, 2004, Golja et al., 2004, Gressens и Luton, 2004). Исследование показано при неясном диагнозе после ультрасонографии или необходимости большей анатомической точности.
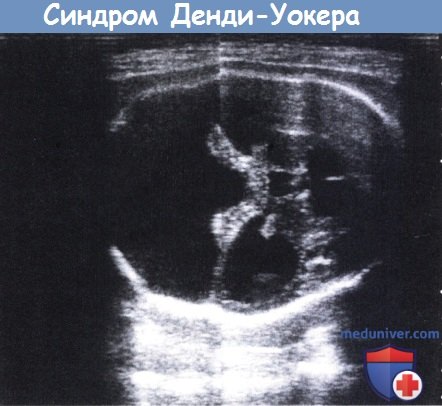
Пренатальная диагностика методом ультразвукового сканирования на 33 неделе беременности.
Хорошо видно отсутствие червя мозжечка и выраженное расширение задней черепной ямки (левая часть рисунка).
С усовершенствованием методов при многих состояниях стала возможной ранняя диагностика, но при других остается относительно поздней, в результате чего возможен поздний неблагоприятный исход случаев метаболических заболеваний. Кроме того, достоверность ультрасонографии в значительной степени зависит от опыта специалиста. В связи с некоторыми аномалиями, такими как синдром Денди-Уолкера или агенезия мозолистого тела, возможны серьезные этические проблемы, поскольку они в значительной части случаев могут не сопровождаться дисфункцией нейроразвития.
Для хромосомного анализа может потребоваться амниоцентез или биопсия ворсин хориона при spina bifida и некоторых метаболических расстройствах. Эти методы сопровождаются риском фетальной потери приблизительно в 0,5-1% при амниоцентезе, выполненном под контролем ультразвука (Seeds, 2004), и в 3% при биопсии хориона (Caughey et al., 2006). Риск ранения плода очень незначителен, но существует (Mancini et al., 2001, Seeds et al., 2004).
Некоторые пороки развития ЦНС могут сопровождаться заболеваниями обмена веществ. Отдельные из них можно предупредить с помощью контроля за метаболическими расстройствами у матери (например, фенилкетонурия или диабет) или путем профилактики токсического действия определенных препаратов или других токсических веществ, таких как алкоголь, которые можно выявить пренатально. Особые врожденные нарушения обмена веществ являются причиной мальформаций ЦНС (Nissenkorn et al., 2001, Raoul et al., 2003).
Неоднократно выявлялись некетотическая гиперглицинемия, митохондриальные и пероксисомальные расстройства. Bamforth et al. (1988) обнаружили 8 случаев агенезии мозолистого тела среди 50 пациентов с наследственными заболеваниями обмена веществ. Недавно были описаны некоторые аномалии метаболизма холестерина (Haas et al., 2001). Полиморфизм гена, кодирующего метилентетрагидрофолатредуктазу, может быть фактором риска для spina bifida (van der Put et al., 1995).
Нарушение обмена веществ экологического происхождения, либо в связи с заболеваниями матери, либо в результате действия токсических веществ на протяжении беременности, является важной причиной развития пороков развития плода. Материнский сахарный диабет (Anderson et al., 2005) является одним из основных метаболических расстройств, способных существенно повысить частоту отдельных пороков развития ЦНС, особенно голопрозэнцефалии. Более того, четкая взаимосвязь высокого уровня гликозилированного гемоглобина А1 на ранних сроках беременности с появлением тяжелых дефектов потомства, подтверждает гипотезу, что мальформации у детей от матерей, страдающих диабетом, возникают рано в течение первых семи недель гестации.
Такие данные свидетельствуют о том, что необходим строгий контроль за течением материнского диабета.
Фенилкетонурия у матерей является другой причиной аномалий развития ЦНС.
Важным фактором является материнский алкоголизм. Влияние на плод, включая мальформации ЦНС, были всесторонне рассмотрены в ряде опубликованных исследований, употребления любого количества алкоголя во время беременности лучше избегать, так как «безопасный» уровень не определен. Зарегистрированы случаи с агенезией мозолистого тела и голопрозэнцефалией (Ronen и Andrews, 1991).
Мальформации в результате употребления кокаина были вызваны экспериментально на мышах (Nassogne et al., 1998). Для людей ситуация не однозначна, хотя хорошо известно воздействие на плод материнской наркомании с нарушением роста головы и поведения.
Тщательное наблюдение за беременностью очень важно, с особым вниманием к случаям с высокими факторами риска, такими как материнский возраст более 35 лет, многоплодная беременность, многоводие или маловодие, и матерям с известными нарушениями или тем, у кого прежде рождались дети с пороками развития. Плоды с меньшим весом к сроку гестации также имеют повышенный риск. Khoury et al. (1988) обнаружили 8% пороков развития у маленьких к сроку гестации детей в сравнении с 3,3% у детей с соответствующим весом к сроку гестации.
Обнаружение периферических мальформаций при ультрасонографии, особенно кистозных гигром, также является показателем высокого риска, а воротниковые пространства обладают очень важной информацией для диагностики синдрома Дауна и других аномалий развития.
Важно информировать будущих родителей о том, что вне зависимости от метода и тщательности наблюдения многие мальформации мозга могут быть упущены.
Редактор: Искандер Милевски. Дата публикации: 30.11.2018
Исследование плода и плаценты при врожденных пороках развития, несовместимых с жизнью
Целью исследования было выявить структуру врожденных пороков развития плода, несовместимых с жизнью, приведших к индуцированному прерыванию беременности по медицинским показаниям, структурные изменения в последе при наличии пороков развития. Проведено ран
The aim of the study was to reveal the structure of fatal congenital malformations of the fetus, leading to the induced interruption of pregnancy due to medical indications, structural changes in the afterbirth in the presence of malformations. The randomized comparative study was conducted in 2 stages (retrospective and prospective).
Врожденные пороки развития (ВПР) плода считают важнейшей медицинской и социальной проблемой, поскольку они занимают ведущее место в структуре причин перинатальной, неонатальной и младенческой заболеваемости, смертности и инвалидности [1]. Также актуальной является проблема прерывания беременности в поздние сроки по медицинским показаниям со стороны плода, так как на ее долю приходится около 20% от общего числа абортов, а количество осложнений возрастает в 3–4 раза при прерывании беременности во втором триместре по сравнению с первым [2]. Согласно данным ВОЗ, ВПР отмечают у 4–6% детей. В России ежегодно более 50 000 детей рождаются с ВПР, число пациентов с ВПР превышает 1,5 млн человек. При наличии у плода ВПР, несовместимых с жизнью, или сочетанных пороков с неблагоприятным прогнозом для жизни и здоровья, при ВПР, приводящих к стойкой потере функций вследствие тяжести и объема поражения при отсутствии методов эффективного лечения, женщине предоставляется информация о возможности искусственного прерывания беременности по медицинским показаниям [3]. При отказе женщины прервать беременность из-за наличия ВПР, несовместимых с жизнью, или иных сочетанных пороков беременность ведется в соответствии с разделом I настоящего порядка. Высокие затраты на лечение, уход и реабилитацию детей с ВПР обусловливают необходимость разработки и совершенствования не только методов контроля, диагностики и профилактики ВПР у детей, но и изучения патоморфологии плода и последа [4].
В последние десятилетия интенсивно изучаются многочисленные антенатальные факторы, приводящие к повреждению нервной системы плода — внутриутробные инфекции, генетические дефекты, проблемы резус-конфликта, воздействие на плод лекарственных веществ и целый ряд других факторов. Нередко причинами врожденных пороков развития плода и последа являются инфекционные причины: инфекционные фетопатии формируются с 16-й недели, когда происходит генерализация инфекции у плода, вследствие чего могут возникать такие пороки развития, как фиброэластоз эндокарда, поликистоз легких, микро- и гидроцефалия (ранние фетопатии) [5].
Большое количество работ посвящено методам прерывания беременности в позднем сроке по медицинским показаниям со стороны плода — врожденным порокам развития плода, реабилитации женщин после элиминации плода [6–11]. В то же время недостаточно описаны результаты патологоанатомического исследования плода и плаценты при врожденных пороках, несовместимых с жизнью. Наше исследование посвящено прерыванию беременности во втором триместре по медицинским показаниям со стороны плода. Данная публикация посвящена вопросам патологоанатомического исследования плода и последа.
Целью данного исследования было выявить структуру врожденных пороков развития плода, несовместимых с жизнью, приведших к прерыванию беременности по медицинским показаниям, их сочетания со структурными изменениями в последе.
Материалы и методы исследования
Исследование одобрено локальным этическим комитетом ФГБОУ ВО ОмГМУ МЗ РФ, Омск (№ 63 от 09.10.2014 г.) и выполнено на базе БУЗОО ГКПЦ, Омск. Прерывание беременности во II триместре по медицинским показаниям проводилось согласно Распоряжению Министерства здравоохранения Омской области № 308-р от 17.09.2013 г. в указанном учреждении, где был создан центр по прерыванию беременности второго триместра и женщине выдавалось заключение перинатального консилиума специалистами (акушер-гинеколог, перинатолог, неонатолог и др.). Гистологическое исследование элиминированных плодов и плацент проведено согласно рекомендациям А. П. Милованова и осуществлялось в патологоанатомическом отделении БУЗОО ОДКБ, Омск.
Основным показанием к прерыванию беременности на всех этапах являлись ВПР плода, несовместимые с жизнью. При наличии у плода ВПР, несовместимого с жизнью, или наличии сочетанных пороков с неблагоприятным прогнозом для жизни и здоровья, при ВПР, приводящих к стойкой потере функций вследствие тяжести и объема поражения при отсутствии методов эффективного лечения, предоставлялась информация о возможности искусственного прерывания беременности по медицинским показаниям. Искусственное прерывание беременности проводилось при наличии информированного добровольного согласия женщины.
На первом ретроспективном этапе (до внедрения в практику регламентирующих документов [3, 12]) проведен анализ гистологического исследования плацент после прерывания беременности у 150 женщин, которые в зависимости от метода прерывания были разделены на две группы: группу А составили 75 женщин, которым проведено прерывание беременности в поздние сроки методом трансвагинального трансцервикального амниоцентеза: амниоинфузия 10% раствором хлорида натрия. Группу Б составили 75 женщин, которым с целью прерывания беременности в поздние сроки для возбуждения и стимуляции родовой деятельности использовали гель динопростон для эндоцервикального введения. Более подробно методы прерывания беременности, их эффективность и исходы описаны в наших предыдущих публикациях [13–15]. Критериями включения пациенток в группы А и Б были следующие: срок беременности 18–21 неделя 6 дней, возможность родоразрешения через естественные родовые пути и отсутствие противопоказаний к применению гипертонического раствора хлорида натрия (10% NaCl) и простагландинов. Пациентки обеих групп были идентичны по возрасту, особенностям менструальной функции, наличию экстрагенитальных и гинекологических заболеваний, паритету. Все пациентки были консультированы в медико-генетическом отделе.
На втором этапе под проспективным наблюдением было 195 беременных, разделенных на две группы. Основную группу составили 98 женщин, которым проведено прерывание беременности в поздние сроки следующим комбинированным методом: мифепристон перорально и введение ламинарий в цервикальный канал. В группу сравнения были включены 97 женщин, прерывание беременности которым проводилось по схеме ВОЗ. Критерии включения в группы: пациентки, которым дано заключение консилиума врачей для прерывания беременности по медицинским показаниям со стороны плода в сроки гестации 18–21 неделя согласно приказам МЗСР РФ № 736 от 03 декабря 2007 г. [16] и № 572н от 01.11.2012 [3].
На проспективном этапе исследования материалом для изучения послужили результаты патоморфологического исследования плодов (аутопсийного материала) и последов (макроскопическое и микроскопическое). В работе использованы антропометрические, органометрические, гистологические методы. С целью уточнения гестационного возраста плода и дополнительных скрытых аномалий развития в соответствии с имеющимися стандартами использовали антропометрические и органометрические исследования [17–20]. Гистологические исследования органов плода, плодных оболочек, пуповины и плаценты проводили на парафиновых срезах, изготовленных по общепринятой методике и окрашенных гематоксилином и эозином, а также избирательно пикрофуксином по методу Ван Гизона. Для гистологического исследования предварительно материал фиксировали в 10% нейтральном формалине, после промывки и стандартной проводки заливали в парафин. Парафиновые срезы толщиной 3–5 мкм окрашивали гематоксилином и эозином. Элементы соединительной ткани определяли пикрофуксином по методу Ван-Гизона. Методы гистологического исследования выполнялись по прописям, изложенным в классических руководствах по гистологической технике и гистохимии. Обследование элиминированных плодов включало тщательную визуальную оценку имеющихся стигм эмбриогенеза, врожденных пороков. Для гистологического исследования отбирали фрагменты органов с целью изучения их гистоархитектоники [17].
Использовался способ статистической обработки результатов по критерию t таблиц Стьюдента, позволяющий вычислить степень достоверности различий при небольшом числе наблюдений. Перед каждым вычислением достоверности различий между количественными признаками, а также для выбора критерия корреляции оценивали нормальность их распределения по критерию Колмогорова–Смирнова. В случае ненормального распределения количественных признаков или неравенстве дисперсий применялся U-критерий Манна–Уитни. Для факторов, имеющих биноминальное распределение, дополнительно были рассчитаны 95% доверительные интервалы.
Результаты исследования
Пациентки всех групп были идентичны по возрасту, особенностям менструальной функции, наличию экстрагенитальных и гинекологических заболеваний, паритету. Эффективность прерывания беременности в поздние сроки методом амниоцентеза составила 93,3%, при применении простагландинов — 92%, на проспективном этапе не имела достоверных различий и составила 99,0% в основной группе и 96,9% — в группе сравнения.
В структуре выявленных ВПР плода на первом месте в основной группе были врожденные пороки сердечно-сосудистой системы (34 наблюдения — 34,7%), на втором — пороки центральной нервной системы (ЦНС) (29 наблюдений — 29,6%), на третьем — множественные пороки развития (13–13,3%), на четвертом — пороки мочевыводящей системы (9–9,2%) (табл. 1). В остальных наблюдениях выявлены ВПР опорно-двигательного аппарата (7–7,1%) и другие (6–6,1%): кожи и мышц, желудочно-кишечного тракта, легких, шеи и лица, прочие. В группе сравнения на первом месте также были врожденные пороки сердечно-сосудистой системы (32 наблюдения — 33,0%), на втором — пороки ЦНС (30 наблюдений — 30,9%), на третьем — множественные пороки развития (15–15,5%), на четвертом — пороки мочевыводящей системы (10–10,3%). В остальных наблюдениях выявлены ВПР опорно-двигательного аппарата (8–8,2%) и другие (2–2,1%): кожи и мышц, желудочно-кишечного тракта, легких, шеи и лица, прочие.
Среди пороков сердечно-сосудистой системы в обеих группах чаще наблюдались транспозиция магистральных сосудов, дефекты межжелудочковой и межпредсердной перегородок, общий артериовенозный канал, тетрада Фалло, сочетанные пороки сердца, аномалии Эбштейна, гипоплазия левого отдела, прочие врожденные пороки сердечно-сосудистой системы.
В структуре пороков ЦНС чаще наблюдалась гидроцефалия, анэнцефалия, синдром Арнольда–Киари и Денди–Уокера, микроцефалия, агенезия мозолистого тела, акрания, spina bifida (спинномозговая грыжа). Гидроцефалия — заболевание, характеризующееся избыточным накоплением цереброспинальной жидкости в желудочках и подоболочечных пространствах головного мозга, сопровождающееся их расширением и атрофией мозгового вещества.
В ходе ретроспективной оценки исследования последов в группе А в подавляющем большинстве наблюдений (78,7%) определялись серозно-гнойный и гнойно-некротический децидуит и лишь в небольшом проценте случаев (21,3%) наблюдался серозный децидуит. Также в этой группе отмечалось наличие дисциркуляторных нарушений (выраженный отек стромы ворсин, тромбоз межворсинчатого пространства, ретроплацентарные гематомы). В группе Б серозный париетальный децидуит определялся в большинстве случаев (54,7%), воспалительные изменения не определялись в 38,7% наблюдений, серозно-гнойный париетальный децидуит обнаружен в 6,6% случаев.
На ретроспективном этапе при исследовании последа в большей степени были обнаружены патологическое строение и пороки развития пуповины, чем в плаценте. Так, на первом месте среди признаков патологического строения пуповины была тощая пуповина: 19 наблюдений в основной группе (19,4%) и 21 (21,6%) в группе сравнения (табл. 2). На втором месте определялись ложные узлы пуповины: 16 (16,3%) и 17 (17,5%) соответственно исследуемым группам, на третьем месте — истинные узлы пуповины: 14 (14,2%) и 15 (15,5%). Нередко в структуре патологических вариантов строения пуповины было оболочечное прикрепление пуповины: 12 (12,2%) и 9 (9,3%) соответственно. Реже были выявлены гипо- и гиперизвитая пуповина: 8 (8,2%) и 7 (7,2%) соответственно исследуемым группам; единственная артерия пуповины: 6 (6,1%) и 4 (4,1%); гематома пуповины: 1 (1,0%) в основной группе и 2 (2,1%) в группе сравнения. Всего при исследовании нарушения строения пуповины были выявлены в 76 случаях основной группы и в 75 — группы сравнения, в целом в исследовании — в 77,4% наблюдениях.
При гистологическом исследовании плаценты отмечалась относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения (23 наблюдения — 23,5% в основной группе и 29–30,0% в группе сравнения). Серозный париетальный децидуит определялся в 17,3% наблюдений основной группы и 16,5% группы сравнения. Такие скудные изменения в плаценте, выявленные при исследовании, свидетельствуют о том, что ВПР плода, несовместимые с жизнью, чаще сочетаются с патологией строения пуповины, чем с нарушениями строения и пороками развития плаценты. Также относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения указывают на то, что прерывание беременности проводилось современным медикаментозным способом, который имитирует спонтанную сократительную деятельность матки и не вызывает грубых изменений в плаценте.
Таким образом, в структуре выявленных ВПР плода, несовместимых с жизнью, в исследуемых группах на первом месте были врожденные пороки сердечно-сосудистой системы, на втором — пороки ЦНС, на третьем — множественные пороки развития, на четвертом — пороки мочевыводящей системы. В остальных наблюдениях выявлены ВПР опорно-двигательного аппарата и другие: желудочно-кишечного тракта, дыхательной системы, шеи и лица, прочие.
При гистологическом исследовании плаценты ретроспективного этапа (до внедрения в акушерскую практику современных методов производства позднего индуцированного аборта) при проведении амниоинфузии гипертоническим раствором в подавляющем большинстве определялись серозно-гнойный и гнойно-некротический мембранит, при применении динопростона чаще наблюдался серозный париетальный децидуит. После внедрения в работу акушерско-гинекологической службы регламентирующего Приказа 572н при гистологическом исследовании плаценты у пациенток второго этапа обеих групп отмечалась относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения.
При исследовании последа чаще встречались пороки развития пуповины, чем плаценты. На первом месте среди признаков патологического строения пуповины была тощая пуповина, на втором месте — ложные узлы пуповины, на третьем — истинные узлы. Реже определялось оболочечное прикрепление пуповины. Значительно реже были выявлены гипо- и гиперизвитая пуповина, единственная пупочная артерия; гематома пуповины. При гистологическом исследовании плаценты отмечалась относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения. Скудные изменения в плаценте (в сравнении с изменениями в пуповине), выявленные при исследовании, свидетельствуют о том, что врожденные пороки развития плода, несовместимые с жизнью, чаще сочетаются с патологией строения пуповины, чем с плацентарными пороками. Также относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения указывают на то, что прерывание беременности проводилось современным медикаментозным способом, который имитирует спонтанную сократительную деятельность матки и не вызывает грубых изменений в плаценте.
Литература
* ФГБОУ ВО ОмГМУ МЗ РФ, Омск
** БУЗОО ОДКБ, Омск
_575.gif)