Что такое вдкн у женщин
Врожденная дисфункция коры надпочечников
На сегодняшний день проблема диагностики данной патологии в большинстве развитых стран мира решается с помощью проведения неонатального скрининга на дефицит белка 21-гидроксилазы, который основан на определении уровня 17-гидроксипрогестерона в крови, взятой из пятки новорожденного. Данное исследование проводится с целью максимально раннего выявления врожденной дисфункции коры надпочечников, что позволяет приступить к началу заместительной гормональной терапии до возникновения симптомов надпочечниковой недостаточности.
К факторам, повышающим риск развития врожденной дисфункции коры надпочечников, относится наличие данной патологии у одного из родителей, либо если родители являются носителями гена, обусловливающего дефект транспортных белков, необходимых для синтеза кортизола корой надпочечников. Если подобный ген есть у обоих родителей, в четверти случаев есть риск проявления патологии у ребенка.
Механизм развития врожденной дисфункции коры надпочечников
Симптомы врожденной дисфункции надпочечников
Клиническая картина врожденной дисфункции коры надпочечников, вызванной дефектом фермента 21-гидроксилазы зависит от степени его выраженности и проявляется тремя формами:
— простая вирильная форма;
Сольтеряющая форма врожденной дисфункции коры надпочечников является наиболее часто встречаемой (встречается в трех случаях из четырех), и развивается в результате полной блокады белка 21-гидроксилазы, что влечет за собой нарушение продукции глюкокортикоидов и минералокортикоидов, в том числе кортизола и альдостерона. Начавшись ещё в период внутриутробного развития, врожденная дисфункция коры надпочечников проявляется практически сразу после рождения симптомами надпочечниковой недостаточности и избытка андрогенов.
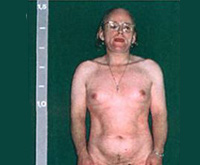
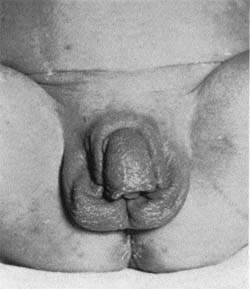
Новорожденные девочки страдают при этом женским гермафродитизмом, который проявляется формированием их половых органов по мужскому типу, а именно, увеличением клитора, сходством его с половым членом и сращением половых губ наподобие мошонки. Внутренние половые органы при этом не изменяют своей анатомической формы. Однако, из-за избытка андрогенов, при отсутствии лечебных мероприятий, у девочек не наступят менструации.
У новорожденных мальчиков врожденная дисфункция коры надпочечников проявляется в виде увеличения размера полового члена и усиленной пигментации мошонки, в результате которой цвет её темнеет. Если не проводить своевременную коррекцию гиперандрогении, заболевание склонно к стремительному прогрессированию, что приводит к быстрому закрытию ростовых зон костей, в результате чего дети остаются низкорослыми. Кроме того у мальчиков в возрасте 2-3 лет наблюдается раннее огрубление голоса, чрезмерное развитие мускулатуры и рост волос в паховой зоне.
Сниженная концентрация кортизола и альдостерона при врожденной дисфункции коры надпочечников приводят к надпочечниковой недостаточности, которая клинически проявляется в виде вялого сосания, рвоты, обезвоживания, снижения активности и потемнением кожных покровов.
Простая вирильная форма врожденной дисфункции коры надпочечников развивается при частичном сохранении ферментативной активности 21-гидроксилазы, поэтому симптомы надпочечниковой недостаточности не наблюдаются, а трансформация половых органов сходна с таковой при сольтеряющей форме.
Постпубертатная форма врожденной дисфункции коры надпочечников развивается при незначительном дефекте фермента 21-гидроксилазы, что приводит к умеренному снижению уровня кортизола и альдостерона и незначительному повышению концентрации адренокортикотропного гормона. Именно этим и обусловлен тот факт, что у младенцев не наблюдаются симптомы надпочечниковой недостаточности и нарушения строения наружных половых органов. Заболевание может быть обнаружено при обращении пациенток с проблемой бесплодия или менструальной дисфункцией, а также с избыточным оволосением по мужскому типу. В некоторых случаях генетический дефект фермента настолько незначителен, что на протяжении жизни может клинически никак не проявляться.
Диагностика врожденной дисфункции коры надпочечников
Наряду с анализом анамнестических данных, позволяющих выявить наличие подобной патологии в семейном анамнезе, объективным осмотром, основным критерием для постановки диагноза являются данные лабораторных исследований. Определение уровня 17-гидроксипрогестерона (предшественник кортизола) и уровня андрогенов является одним из основных диагностических критериев врожденной дисфункции коры надпочечников, вызванной дефектом фермента 21-гидроксилазы.
Неонатальный скрининг, проводимый на 4-5 сутки после рождения ребенка и предполагающий исследование 17-гидроксипрогестерона в пяточной крови младенца, позволяет выявить врожденную дисфункцию коры надпочечников в самые ранние сроки.
Лечение врожденной дисфункции коры надпочечников
Если активность ренина в плазме крови повышена, что свидетельствует о сниженном уровне альдостерона, требуется назначение минералокортикоидов. Наиболее распространено использование флудрокортизона, доза которого должна подбираться с учетом данных лабораторного исследования активности ренина, и составляет примерно 0,05-0,15 мг/сутки. Изредка требуется введение солевых растворов (хлорида натрия), если происходит насыщение минералокортикоидами.
Такие формы врожденной дисфункции коры надпочечников, которые протекают с выраженным нарушением продукции андрогенов, требуют, начиная с подросткового возраста, назначения заместительной гормональной терапии половыми стероидами с учетом выбранного пола. Если диагностика заболевания проведена с опозданием и половые органы у женщины развиты по мужскому типу, прибегают к хирургическому вмешательству, подразумевающему пластику наружных половых органов.
Прогноз заболевания напрямую связан с тем, насколько своевременно установлен диагноз врожденной дисфункции коры надпочечников и верно ли выбрана схема проводимой коррекции.
Консультации пациентов с заболеваниями надпочечников проводят:
 |
 |
 |
 |
Консультации проводятся в амбулаторных филиалах центра:
— Петроградский филиал (Санкт-Петербург, Кронверкский пр., д. 31, 200 метров от станции метро «Горьковская», телефон для записи (812) 498-10-30, с 7.30 до 20.00, ежедневно);
— Приморский филиал (Санкт-Петербург, ул. Савушкина, д. 124, корп. 1, 250 метров направо от станции метро «Беговая», телефон для записи (812) 565-11-12 с 7.00 до 21.00 в будни и с 7.00 до 19.00 в выходные).
Для консультации просим привозить все имеющиеся у Вас результаты обследований.
ВНИМАНИЮ ПАЦИЕНТОВ!
В настоящее время в Северо-Западном центре эндокринологии проводится бесплатное оперативное лечение пациентов с новообразованиями надпочечников. Лечение проводится в рамках программы ОМС (обязательного медицинского страхования) или программы СМП (специализированная медицинская помощь).
Вопросы по госпитализации можно задать ответственному администратору Клешниной Валентине Петровне по телефону +7 900 6291427 (в будни, с 9 до 17 часов).
Пакет необходимых обследований должен в себя включать следующий перечень (в случае отсутствия результатов перечисленных исследований их требуется выполнить в любом случае):
Должны быть определены следующие лабораторные показатели:
Для проведения перечисленных обследований нет необходимости ложиться в стационар, их можно выполнить по месту жительства или в ближайшей лаборатории.
Пациентам из Санкт-Петербурга желательно до поступления в клинику обратиться для очной консультации (запись по телефону (812) 565-11-12, Приморский филиал центра, адрес: ул. Савушкина, д. 124, к.1, запись по телефону (812) 498-1030, Петроградский филиал центра, адрес: Кронверкский пр., д.31).
Преждевременное половое созревание
Кортикостерома
Анализы в СПб
Одним из важнейших этапов диагностического процесса является выполнение лабораторных анализов. Чаще всего пациентам приходится выполнять анализ крови и анализ мочи, однако нередко объектом лабораторного исследования являются и другие биологические материалы.
Консультация эндокринолога
Специалисты Северо-Западного центра эндокринологии проводят диагностику и лечение заболеваний органов эндокринной системы. Эндокринологи центра в своей работе базируются на рекомендациях Европейской ассоциации эндокринологов и Американской ассоциации клинических эндокринологов. Современные диагностические и лечебные технологии обеспечивают оптимальный результат лечения.
Анализ на АКТГ
Анализ на АКТГ применяется для диагностики заболеваний, связанных с нарушением работы коры надпочечников, а также в ходе наблюдения после оперативного удаления опухолей
Консультация гинеколога-эндокринолога
Гинеколог-эндокринолог – один из наиболее востребованных специалистов Северо-Западного центра эндокринологии. Консультации гинеколога в Санкт-Петербурге являются одними из наиболее востребованных, а консультации гинеколога-эндокринолога – особенно. Подавляющее большинство заболеваний, приводящих женщин на консультацию к гинекологу, имеют причины своих проблем в нарушенной функционировании эндокринной системы. Именно поэтому многие пациентки, обращающиеся за помощью в эндокринологический центр, нуждаются именно в консультации гинеколога-эндокринолога, а в ряде случаев – еще и в консультации терапевта-эндокринолога
Анализ на альдостерон
Альдостерон – гормон, вырабатываемый корой надпочечников. Его основная функция – регуляция содержания солей натрия и калия в крови
УЗИ надпочечников
Консультация уролога-андролога
Андрология — область медицины, изучающая мужчин, мужскую анатомию и физиологию, заболевания мужской половой сферы и методы их лечения. На данный момент специализации по андрологии в России не существует, поэтому специалисты, желающие заниматься этой областью медицины, должны получать базовое образование по урологии с последующей дополнительной специализацией по эндокринологии
Консультация детского эндокринолога
Очень часто на прием к специалистам Северо-Западного центра эндокринологии обращаются пациенты, не достигшие 18 лет. Для них в центре работают специальные врачи – детские эндокринологи
Отзывы
Истории пациентов
Видеоотзывы: опыт обращения в Северо-Западный центр эндокринологии
Адреногенитальный синдром — наследственное заболевание надпочечников, при котором вследствие функциональной несостоятельности ферментов нарушается стероидогенез. Проявляется вирилизацией гениталий, маскулиноподобным телосложением, недоразвитием груди, гирсутизмом, акне, аменореей или олигоменореей, бесплодием. В ходе диагностики определяют уровни 17-гидроксипрогестерона, 17-кетостероидов, андростендиона, АКТГ, проводят УЗИ яичников. Пациенткам назначают заместительную гормонотерапию глюкокортикоидами и минералокортикоидами, эстрогены в комбинации с андрогенами или прогестинами нового поколения. При необходимости выполняют пластику половых органов.
МКБ-10
Общие сведения
Адреногенитальный синдром, или врожденная дисфункция (гиперплазия) коры надпочечников, — наиболее частое из наследуемых заболеваний. Распространенность патологии отличается у представителей разных национальностей. Классические варианты АГС у лиц европеоидной расы встречаются с частотой 1:14 000 младенцев, в то время как у эскимосов Аляски этот показатель составляет 1:282.
Существенно выше заболеваемость у евреев. Так, неклассическую форму адреногенитального расстройства выявляют у 19% лиц еврейской национальности группы ашкенази. Патология передается по аутосомно-рецессивному типу. Вероятность рождения ребенка с таким синдромом при носительстве патологического гена у обоих родителей достигает 25%, в браке носителя и больного — 75%. Если один из родителей имеет полноценные ДНК, клинические проявления синдрома у детей не развиваются. При наличии АДС у отца и матери ребенок также будет болен.
Причины
У больных с наследуемой гиперплазией надпочечников генетический дефект проявляется несостоятельностью ферментных систем, участвующих в секреции стероидных гормонов. В 90-95% случаев патология возникает при повреждении гена, который отвечает за синтез 21-гидроксилазы — фермента, влияющего на образование кортизола. В остальных клинических случаях вследствие дефекта ДНК нарушается производство других ферментов, обеспечивающих стероидогенез, — StAR/20,22-десмолазы, 3-β-гидрокси-стероиддегидрогеназы, 17-α-гидроксилазы/17,20-лиазы, 11-β-гидроксилазы, P450-оксидоредуктазы и синтетазы альдостерона.
У пациентов с признаками вирилизирующего синдрома вместо активного гена CYP21-B в коротком плече 6-й аутосомы расположен функционально несостоятельный псевдоген CYP21-A. Структура этих участков ДНК-цепи во многом гомологична, что повышает вероятность конверсии генов в мейозе с перемещением участка нормального гена на псевдоген или делецию CYP21-B.
По-видимому, именно этими механизмами объясняется существование скрытых форм болезни, дебютирующих в пубертате или постпубертатном периоде. В таких случаях клинические признаки патологии становятся заметными после нагрузок, истощающих кору надпочечников: тяжелых болезней, травм, отравлений, радиационных воздействий, длительного периода интенсивной работы, психологически напряженных ситуаций и т. д.
Патогенез
В основе механизма развития наиболее распространенного варианта адреногенитального синдрома с дефектом CYP21-B-гена лежит принцип обратной связи. Ее начальным звеном становится дефицит стероидов — кортизола и альдостерона. Несостоятельность процессов гидроксилирования сопровождается неполным переходом 17-гидроксипрогестерона и прогестерона в 11-дезоксикортизол и дезоксикортикостерон. В результате снижается секреция кортизола, а для компенсации этого процесса в гипофизе усиливается синтез АКТГ — гормона, вызывающего компенсаторную гиперплазию коры надпочечников для стимуляции выработки кортикостероидов.
Параллельно возрастает синтез андрогенов и появляются видимые признаки их влияния на чувствительные ткани и органы. При умеренном снижении активности фермента минералокортикоидная недостаточность не развивается, поскольку потребность организма в альдостероне почти в 200 раз ниже по сравнению с кортизолом. Только глубокий дефект гена вызывает тяжелую клиническую симптоматику, которая проявляется с раннего возраста. Патогенез развития заболевания при нарушении структуры других участков ДНК аналогичен, однако пусковым моментом являются нарушения в других звеньях стероидогенеза.
Классификация
Систематизация различных форм вирилизирующей гиперплазии надпочечников основана на особенностях клинической картины заболевания, выраженности генетического дефекта и времени проявления первых патологических признаков. Тяжесть расстройства напрямую связана со степенью повреждения ДНК. Специалисты в сфере эндокринологии различают следующие виды адреногенитального синдрома:
Сольтеряющий и простой вирильный виды адреногенитальных расстройств относят к категории антенатальной патологии, формирующейся внутриутробно и проявляющейся с момента рождения. При дефекте строения других генов наблюдаются более редкие варианты заболевания: гипертензивные — классический (врожденный) и неклассический (поздний), гипертермический, липидный, с ведущими проявлениями гирсутизма.
Симптомы
Сольтеряющий и простой вирильный
При антенатальных формах заболевания основным клиническим симптомом является видимая вирилизация гениталий. У новорожденных девочек обнаруживаются признаки женского псевдогермафродитизма. Клитор большой по размерам или имеет пенисообразную форму, преддверие влагалища углублено, сформирован урогенитальный синус, большие и малые половые губы увеличены, промежность высокая. Внутренние половые органы развиты нормально.
У младенцев-мальчиков увеличен половой член и гиперпигментирована мошонка. Кроме того, при сольтеряющем адреногенитальном расстройстве выражена симптоматика надпочечниковой недостаточности с тяжелыми, зачастую несовместимыми с жизнью соматическими нарушениями (понос, рвота, судороги, обезвоживание и др.), которые проявляются с 2-3-недельного возраста. У девочек с простым вирильным АГС по мере взросления признаки вирилизации усиливаются, формируется диспластическое телосложение.
Из-за ускорения процессов окостенения пациентки отличаются невысоким ростом, широкими плечами, узким тазом, короткими конечностями. Трубчатые кости массивные. Половое созревание начинается рано (до 7 лет) и протекает с развитием вторичных мужских половых признаков. Отмечается увеличение клитора, снижение тембра голоса, нарастание мышечной силы, формирование типичной для мужчин формы перстневидного хряща щитовидной железы. Грудь не растет, менархе отсутствует.
Неклассический
Менее специфичны клинические симптомы при неклассических формах вирилизирующего синдрома, возникшие в пубертате и после стрессовых нагрузок (выкидыша на ранних сроках беременности, медицинского аборта, операции и др.). Обычно пациентки вспоминают, что у них еще в младшем школьном возрасте появилось небольшое оволосение в подмышечных впадинах и на лобке. В последующем развились признаки гирсутизма с ростом стержневых волос над верхней губой, по белой линии живота, в области грудины, в сосково-ареолярной зоне.
Женщины с АГС предъявляют жалобы на стойкую угревую сыпь, пористость и повышенную жирность кожи. Менархе наступает поздно — к 15-16 годам. Менструальный цикл неустойчив, интервалы между менструациями достигают 35-45 дней и более. Кровянистые выделения во время месячных скудные. Молочные железы небольшие. Клитор несколько увеличен. Такие девушки и женщины могут иметь высокий рост, узкий таз, широкие плечи.
По наблюдениям специалистов в сфере акушерства и гинекологии, чем позже развиваются адреногенитальные расстройства, тем менее заметны внешние признаки, характерные для мужчин, и тем чаще ведущим симптомом становится нарушение месячного цикла. При более редких генетических дефектах пациентки могут жаловаться на повышение артериального давления или, наоборот, гипотонию с низкой работоспособностью и частыми головными болями, гиперпигментацию кожи с минимальными симптомами вирилизации.
Осложнения
Основным осложнением адреногенитального синдрома, по поводу которого пациентки обращаются к акушерам-гинекологам, является стойкое бесплодие. Чем раньше проявилось заболевание, тем меньше вероятность забеременеть. При значительной ферментной недостаточности и клинических проявлениях простого вирилизирующего синдрома беременность вообще не наступает.
У забеременевших пациенток с пубертатными и постпубертатными формами заболевания возникают самопроизвольные выкидыши на раннем сроке. В родах возможна функциональная истмико-цервикальная недостаточность. Такие женщины более склонны к возникновению психоэмоциональных расстройств — склонности к депрессии, суицидальному поведению, проявлениям агрессии.
Диагностика
Постановка диагноза при антенатальных типах АГС с характерными изменениями половых органов не представляет сложности и проводится сразу после родов. В сомнительных случаях применяют кариотипирование для подтверждения женского кариотипа (46ХХ), молекулярно-генетические тесты. Большее значение диагностический поиск приобретает при позднем клиническом дебюте или скрытом течении с минимальными внешними проявлениями вирилизации. В подобных ситуациях для выявления адреногенитального синдрома используют следующие лабораторные и инструментальные методы:
Для сольтеряющего варианта АГС также характерна повышенная концентрация ренина в плазме крови. Дифференциальная диагностика адреногенитальных расстройств, возникших в пубертатном и детородном возрасте, проводится с синдромом поликистозных яичников, овариальными андробластомами, андростеромами надпочечников, вирильным синдромом гипоталамического происхождения и конституциональным гирсутизмом. В сложных случаях к диагностике привлекают эндокринологов, урологов, врачей-генетиков.
Лечение адреногенитального синдрома
Основным способом коррекции вирильной дисфункции надпочечников является заместительная гормональная терапия, восполняющая дефицит глюкокортикоидов. Если у женщины со скрытым АГС нет репродуктивных планов, кожные проявления гиперандрогении незначительны и месячные ритмичны, гормоны не применяют. В остальных случаях выбор схемы лечения зависит от формы эндокринной патологии, ведущей симптоматики и степени ее выраженности. Зачастую назначение глюкокортикоидных препаратов дополняют другими медикаментозными и хирургическими методами, подобранными в соответствии с конкретной терапевтической целью:
Определенные сложности в ведении пациентки возникают в тех случаях, когда заболевание не диагностировано в акушерском стационаре, и девочка с выраженной вирилизацией гениталий регистрируется и воспитывается как мальчик. При решении о восстановлении женской половой идентичности хирургическую пластику и гормонотерапию дополняют психотерапевтической поддержкой. Решение о сохранении гражданского мужского пола и удалении матки с придатками принимается в исключительных случаях по настоянию больных, однако такой подход считается ошибочным.
Прогноз и профилактика
Прогноз при своевременном обнаружении адреногенитального синдрома и адекватно подобранной терапии благоприятный. Даже у пациенток со значительной вирилизацией гениталий после пластической операции возможна нормальная половая жизнь и естественные роды. Заместительная гормонотерапия при любой форме АГС способствует быстрой феминизации — развитию грудных желез, появлению месячных, нормализации овариального цикла, восстановлению генеративной функции. Профилактика заболевания осуществляется на этапе планирования беременности.
Если в роду наблюдались случаи подобной патологии, показана консультация генетика. Проведение пробы с АКТГ обоим супругам позволяет диагностировать гетерозиготное носительство или скрытые формы адреногенитального расстройства. При беременности синдром может быть обнаружен по результатам генетического анализа клеток хорионических ворсин или содержимого околоплодных вод, полученных методом амниоцентеза. Неонатальный скрининг, проводимый на 5-е сутки после родов, направлен на выявление повышенной концентрации 17-гидропрогестерона для быстрого выбора терапевтической тактики.
Врожденная дисфункция коры надпочечников
Адреногенитальный синдром Hадпочечники секретируют кортикостероиды, которые по биологическим свойствам можно разделить на 4 группы: глюкокортикоиды, минералокортикоиды, андрогены и эстрогены. Синтез кортизола в надпочечниках плода под вли
 |
| Адреногенитальный синдром |
Hадпочечники секретируют кортикостероиды, которые по биологическим свойствам можно разделить на 4 группы: глюкокортикоиды, минералокортикоиды, андрогены и эстрогены.
Синтез кортизола в надпочечниках плода под влиянием адренокортикотропного гормона (АКТГ) начинается рано, в связи с этим дефект ферментных систем приводит к вирилизации до рождения ребенка. Так как к этому сроку формирование внутренних половых органов заканчивается, вирилизация затрагивает наружные половые органы.
Из различных ферментных дефектов недостаточность 21-гидроксилазы встречается наиболее часто и протекает в виде двух клинических форм: вирильного и сольтеряющего синдромов.
Вирильная форма связана с частичной недостаточностью 21-гидроксилазы. Как правило, при этом наблюдается компенсация функции коры надпочечников в результате повышенной секреции АКТГ, то есть уровень кортизола определяется на нижней границе нормы. Компенсаторное выделение АКТГ приводит к образованию значительного количества андрогенов, прогестерона, 17-гидроксипрогестерона, которые угнетают сользадерживающую активность на уровне канальцев почек, что ведет к значительному увеличению продукции альдостерона. У девочек с вирильной формой с рождения имеются признаки ложного гермафродитизма. Клитор гипертрофирован, напоминает по строению половой член, имеющий единое мочеполовое отверстие — урогенитальный синус, открывающийся у корня клитора, мошонкообразные большие половые губы.
| Врожденная дисфункция коры надпочечников является наследственным заболеванием, характеризующимся нарушением синтеза кортикостероидов, в основном кортизола, в результате дефицита ферментных систем коры надпочечников с одновременной избыточной продукцией андрогенов в надпочечниках |
У мальчиков с рождения отмечается увеличение полового члена, кожа мошонки морщинистая, выражена пигментация шва полового члена, кожи мошонки, передней линии живота, ареолы сосков.
В постнатальном периоде продолжается избыточная секреция андрогенов, усиливаются явления вирилизации. Дети быстрее растут, имеют развитую мускулатуру. Вначале больные обгоняют в росте сверстников, в дальнейшем же, после 9-10 лет, в связи с закрытием зон роста остаются низкорослыми. В возрасте 2–4 лет появляется преждевременное оволосение на лобке, подмышках, туловище, лице. У некоторых мальчиков значительно увеличивается половой член и появляются эрекции. Телосложение девочек мускулинного типа. В пубертатный период менструации не наступают, молочные железы не развиваются, так как повышенная секреция андрогенов надпочечниками по принципу обратной связи тормозит образование и выделение гонадотропинов. У мальчиков по этой причине угнетается развитие яичек — они остаются маленькими.
При сольтеряющей форме дефицит 21-гидроксилазы более глубокий, поэтому наряду с дефицитом образования кортизола происходит резкое снижение биосинтеза альдостерона. Если при вирильной форме потеря натрия, обусловленная избыточной продукцией прогестерона, 17-гидроксипрогестерона, компенсируется избыточной секрецией альдостерона, то при сольтеряющей форме снижено образование альдостерона. Результатом такого комбинированного действия является развитие клинической картины по типу острой надпочечниковой недостаточности.
| Заболевание наследуется по аутосомно-рецессивному типу и проявляется в гомозиготном состоянии. Распространенность составляет в среднем 1:4000-5000, а гетерозиготное носительство — 1:35-40 человек |
У новорожденных при этом синдроме резко выражены симптомы вирилизации, особенно у детей женского пола — полное заращение половой щели и появление мошоночноподобного образования. На 5–10-й день наступает быстрое ухудшение состояния, связанное с частой рвотой, жидким стулом. Развивается дегидратация, ребенок становится вялым, снижается масса тела. В сыворотке крови нарастает уровень кальция и снижается содержание натрия и хлора.
Гипертоническая форма дисфункции коры надпочечников, связанная с дефицитом 11b-гидроксилазы, встречается реже. В клинической картине, помимо признаков андрогенизации в раннем возрасте, характерно повышение артериального давления. При этой патологии отсутствует гиперплазия юкстагломерулярного аппарата почки и уровень ренина в плазме не повышен.
Дифференциальный диагноз врожденной дисфункции коры надпочечников у девочек первых лет жизни следует проводить с дисгенезией гонад, анорхизмом, истинным гермафродитизмом; у мальчиков — с преждевременным половым развитием различного генеза, в том числе с опухолью яичка, с андрогенпродуцирующей опухолью надпочечника (андростерома). Сольтеряющую форму у новорожденных дифференцируют с пилороспазмом и пилоростенозом.
У девочек старшего возраста при подозрении на врожденную дисфункцию коры надпочечников требуется исключить такие заболевания, как андрогенпродуцирующая опухоль яичника, стромальный текоматоз, поликистоз яичников.
Наиболее приемлемым средством заместительной терапии является преднизолон, который в течение длительного срока сохраняет достаточную концентрацию и обладает некоторым минералокортикоидным действием. Суточная доза его подбирается индивидуально и колеблется в зависимости от возраста: от 1,5–3 мг (для детей младше 3 лет) до 5 мг для детей старшего возраста. Реже применяют преднизолон, кортизон, дексаметазон. Соответственно суточному физиологическому ритму 17-гидроксипрогестерона принимать преднизолон рекомендуется рано утром, в 6-7 часов (причем в это время следует принять 2/3–1/2 дозы) и поздно вечером (23–24 часа). Глюкокортикоиды больные должны получать постоянно, так как отмена препарата ведет к декомпенсации заболевания.
При лечении больных с сольтеряющей формой врожденной дисфункции коры надпочечников к кортикостероидам добавляют минералкортикоиды. Это либо масляный раствор дезоксикортикостерона ацетата (ДОКА), либо таблетированный препарат кортинеф (0,1 мг), который в 5–10 раз активнее первого. Препараты назначаются в течение 1–2 недель ежедневно (ДОКА по 1–2 мл, кортинеф по 1 таб.) с последующим постепенным снижением дозы до оптимальной. Возможно поддерживающую терапию проводить через каждые 1–2 дня. У некоторых больных дефицит минералкортикоидов можно компенсировать добавлением в пищу поваренной соли. Обязательный контроль за весом, артериальным давлением, калием, натрием, ЭКГ.
Начальные дозы кортикостероидов должны быть в два раза выше физиологических.
При адекватном лечении у детей уменьшается мышечная гипертрофия, перераспределяется подкожножировая клетчатка, половое оволосение не прогрессирует. Если лечение начинают до закрытия ядер окостенения, то увеличивается темп роста. В случаях же поздней терапии эти дети так и остаются низкорослыми.
Гипертоническая форма заболевания лечится аналогично вирильной.
При присоединении интеркуррентных заболеваний дозу глюкокортикоидов увеличивают в 1,5–2 раза.
В случае развития острого криза недостаточности коры надпочечников показано внутривенное капельное введение жидкости (физиологический раствор и 5%-ный раствор глюкозы 100-200 мл/кг массы тела в сутки) в 4 приема, ДОКА 2–3 мг/кг массы тела в сутки. В последующие дни доза глюкокортикоидов быстро снижается и больной переводится на пероральный прием преднизолона.
Важное место в лечении врожденной дисфункции коры надпочечников занимает психотерапия, особенно в случае необходимости перемены пола ребенка.
Большинство девочек с этим заболеванием нуждается в проведении феминизирующей пластики наружных гениталий, удалении клитора и формировании малых половых губ после вскрытия урогенитального синуса. Коррекцию наружных гениталий рекомендуется проводить через год после назначения кортикостероидной терапии.