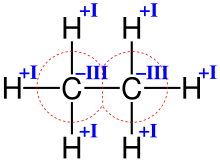
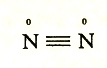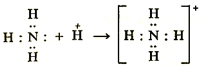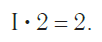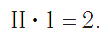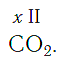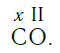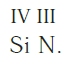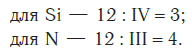Что такое валентность своими словами
Валентность
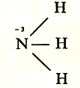
Вале́нтность (от лат. valēns «имеющий силу») — способность атомов химических элементов образовывать определённое число химических связей с атомами других элементов.
Содержание
История возникновения понятия «валентность»
Этимологию термина валентность возможно отследить начиная с 1425 года, когда его начали использовать в научных текстах в значении «экстракт», «препарат». Использование в рамках современного определения зафиксировано в 1884 году (нем. Valenz ). [1] В 1789 году Уильям Хиггинс опубликовал работу, в которой высказал предположение о существовании связей между мельчайшими частицами вещества. [2]
Уже три года спустя, в сентябре 1861 г. А. М. Бутлеров внёс в теорию валентности важнейшие дополнения. Он провёл чёткое различие между свободным атомом и атомом, вступившим в соединение с другим, когда его сродство «связывается и переходит в новую форму». Бутлеров ввёл представление о полноте использования сил сродства и о «напряжении сродства», то есть энергетической неэквивалентности связей, которая обусловлена взаимным влиянием атомов в молекуле. В результате этого взаимного влияния атомы в зависимости от их структурного окружения приобретают различное «химическое значение». Теория Бутлерова позволила дать объяснение многим экспериментальным фактам, касавшимся изомерии органических соединений и их реакционной способности.
Огромным достоинством теории валентности явилась возможность наглядного изображения молекулы. В 1860-х гг. появились первые молекулярные модели. Уже в 1864 г. А. Браун предложил использовать структурные формулы в виде окружностей с помещёнными в них символами элементов, соединённых линиями, обозначающими химическую связь между атомами; количество линий соответствовало валентности атома. В 1865 г. А. фон Гофман продемонстрировал первые шаростержневые модели, в которых роль атомов играли крокетные шары. В 1866 г. в учебнике Кекуле появились рисунки стереохимических моделей, в которых атом углерода имел тетраэдрическую конфигурацию.
Современные представления о валентности
С момента возникновения теории химической связи понятие «валентность» претерпело существенную эволюцию. В настоящее время оно не имеет строгого научного толкования, поэтому практически полностью вытеснено из научной лексики и используется, преимущественно, в методических целях.
Особенно это справедливо для молекул с делокализованными химическими связями, например в азотной кислоте степень окисления азота равна +5, тогда как азот не может иметь валентность выше 4. Известное из многих школьных учебников правило — «Максимальная валентность элемента численно равна номеру группы в Периодической таблице» — относится исключительно к степени окисления. Понятия «постоянной валентности» и «переменной валентности» также преимущественно относятся к степени окисления.
Семиполярные и донорно-акцепторные (дативные) связи по своей сути являются «двойными» связями, поскольку при их образовании происходят оба процесса: перенос электрона (образование ионной связи) и обобществление электронов (образование ковалентной связи).
О валентности для «чайников»
Под валентностью понимают способность атома к образованию химической связи. Численно валентность равна количеству электронных пар, которыми атом связывается с другим атомом или атомами.
Количество возможных связей, которые может образовать атом в процессе химической реакции, равно количеству его неспаренных электронов.
ВАЖНО! При определении валентности не имеет значение полярность образующейся связи, поэтому, валентность, в отличие от степени окисления, не имеет знака.
Дальнейшее изложение материала ведется с условием того, что читатель знаком с электронной структурой атомов и степенью окисления.
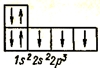
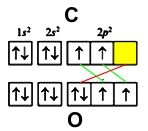
Атом азота имеет три неспаренных электрона, следовательно, его валентность равна 3. Остальные четыре атома азота, располагаются на первом уровне (2), и еще два на 2s-подуровне.
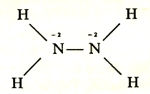
Разберем структурные формулы трех веществ: молекулы азота N2, гидразина N2H4, аммиака NH3. Напомним, что в структурных формулах электронная пара ковалентной связи отображается в виде черточки.
В молекуле азота атомы связываются друг с другом тремя парами неспаренных электронов, таким образом, в этом соединении азот имеет валентность 3,но степень окисления 0.
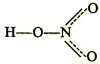
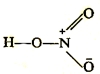
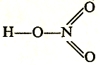
В молекуле азотной кислоты HNO3 оба атома кислорода, связанные только с атомом азота, находятся на одинаковом расстоянии и делят между собой поровну четвертую связь атома азота.
Неверно изображать молекулу азотной кислоты следующей структурной формулой:
Атом азота в принципе не может образовать пять ковалентных связей, поскольку, для этого понадобится 10 электронов, но у атома азота на внешнем (втором) энергетическом уровне не может находиться более 8 электронов, поэтому, азот в принципе не может иметь валентность V. Но, степень окисления азота в молекуле азотной кислоты = +5.
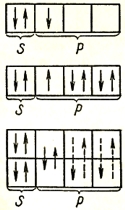
В заключение изложения материала, разберем химическую связь в молекуле угарного газа, имеющего очень прочную химическую связь, что объясняется наличием тройной связи в молекуле CO.
В молекуле оксида углерода (II) атомы кислорода и углерода соединены тройной связью.
В молекуле угарного газа атом углерода принимает валентность 3, но степень окисления +2. По этой причине, для оксида углерода CO(II) характерны реакции присоединения, в которых он играет роль восстановителя:
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Значение слова «валентность»
[От лат. valens, valentis — имеющий силу]
Источник (печатная версия): Словарь русского языка: В 4-х т. / РАН, Ин-т лингвистич. исследований; Под ред. А. П. Евгеньевой. — 4-е изд., стер. — М.: Рус. яз.; Полиграфресурсы, 1999; (электронная версия): Фундаментальная электронная библиотека
ВАЛЕ’НТНОСТЬ, и, мн. нет, ж. [от латин. valens — имеющий ценность, значение] (хим.). То же, что атомность.
Источник: «Толковый словарь русского языка» под редакцией Д. Н. Ушакова (1935-1940); (электронная версия): Фундаментальная электронная библиотека
вале́нтность
1. хим. способность атома химического элемента образовывать связь с другими атомами, а также число этих связей в конкретном соединении ◆ Во всех соединениях галогены проявляют валентность I. ◆ Понятия валентности и степени окисления различны — так, например, в молекуле O2 каждый из атомов кислорода имеет степень окисления 0, но при этом проявляет валентность I.
2. лингв. способность слова вступать в синтаксические — смысловые и грамматические — связи с другими словами
Делаем Карту слов лучше вместе

Спасибо! Я стал чуточку лучше понимать мир эмоций.
Вопрос: торговка — это что-то нейтральное, положительное или отрицательное?
Ассоциации к слову «валентность»
Синонимы к слову «валентность»
Предложения со словом «валентность»
Сочетаемость слова «валентность»
Понятия со словом «валентность»
Отправить комментарий
Дополнительно
Предложения со словом «валентность»
При переходе от некаузативной конструкции к каузативной валентность глагола повышается на единицу, а в семантической структуре предложения появляется ситуация с семантикой побуждения, воздействия и т. п.
То есть у высказывания, выражающего событие, должна быть логическая валентность, или истинностное значение, то есть оно должно быть либо истинным, либо ложным.
Напомним, что валентность углерода в органических молекулах всегда равна четырём.
Урок 6. Валентность
В уроке 6 «Валентность» из курса «Химия для чайников» дадим определение валентности, научимся ее определять; рассмотрим элементы с постоянной и переменной валентностью, кроме того научимся составлять химические формулы по валентности. Напоминаю, что в прошлом уроке «Химическая формула» мы дали определение химическим формулам и их индексам, а также выяснили различия химических формул веществ молекулярного и немолекулярного строения.
Вы уже знаете, что в химических соединениях атомы разных элементов находятся в определенных числовых соотношениях. От чего зависят эти соотношения?
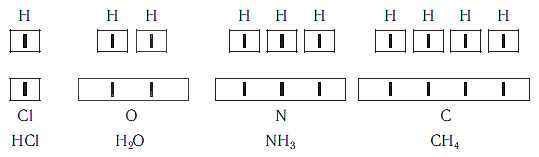
Рассмотрим химические формулы нескольких соединений водорода с атомами других элементов:
Нетрудно заметить, что атом хлора связан с одним атомом водорода, атом кислорода — с двумя, атом азота — с тремя, а атом углерода — с четырьмя атомами водорода. В то же время в молекуле углекислого газа СО2 атом углерода связан с двумя атомами кислорода. Из этих примеров видно, что атомы обладают разной способностью соединяться с другими атомами. Такая способность атомов выражается с помощью численной характеристики, называемой валентностью.
Валентность — численная характеристика способности атомов данного элемента соединяться с другими атомами.
Поскольку один атом водорода может соединиться только с одним атомом другого элемента, валентность атома водорода принята равной единице. Иначе говорят, что атом водорода обладает одной единицей валентности, т. е. он одновалентен.
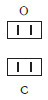
Валентность атома какого-либо другого элемента равна числу соединившихся с ним атомов водорода. Поэтому в молекуле HCl у атома хлора валентность равна единице, а в молекуле H2O у атома кислорода валентность равна двум. По той же причине в молекуле NH3 валентность атома азота равна трем, а в молекуле CH4 валентность атома углерода равна четырем. Если условно обозначить единицу валентности черточкой |, вышесказанное можно изобразить схематически:
Следовательно, валентность атома любого элемента есть число, которое показывает, со сколькими атомами одновалентного элемента связан данный атом в химическом соединении.
Численные значения валентности обозначают римскими цифрами над символами химических элементов:
Определение валентности
Однако водород образует соединения далеко не со всеми элементами, а вот кислородные соединения есть почти у всех элементов. И во всех таких соединениях атомы кислорода проявляют валентность, равную двум. Зная это, можно определять валентности атомов других элементов в их бинарных соединениях с кислородом. (Бинарными называются соединения, состоящие из атомов двух химических элементов.)
Чтобы это сделать, необходимо соблюдать простое правило: в химической формуле вещества суммарные числа единиц валентности атомов каждого элемента должны быть одинаковыми.
Так, в молекуле воды H2O общее число единиц валентности двух атомов водорода равно произведению валентности одного атома на соответствующий числовой индекс в формуле:
Так же определяют число единиц валентности атома кислорода:
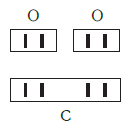
По величине валентности атомов одного элемента можно определить валентность атомов другого элемента. Например, определим валентность атома углерода в молекуле углекислого газа СО2:
Существует и другое соединение углерода с кислородом — угарный газ СО, в молекуле которого атом углерода соединен только с одним атомом кислорода:
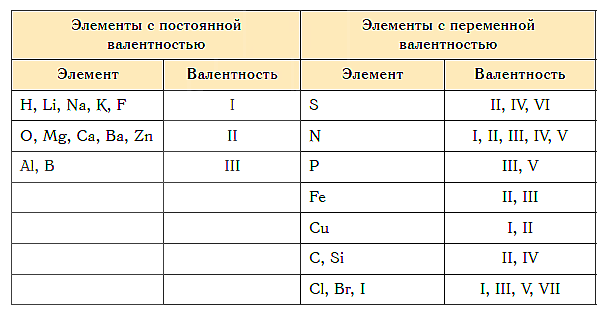
Постоянная и переменная валентность
Как видим, углерод соединяется с разным числом атомов кислорода, т. е. имеет переменную валентность. У большинства элементов валентность — величина переменная. Только у водорода, кислорода и еще нескольких элементов она постоянна (см. таблицу).
Составление химических формул по валентности
Зная валентность элементов, можно составлять формулы их бинарных соединений. Например, необходимо записать формулу кислородного соединения хлора, в котором валентность хлора равна семи. Порядок действий здесь таков.
Записываем рядом символы элементов в следующем виде:
Затем находим НОК валентностей обоих элементов. Оно равно 12 ( IV·III ).
Определяем индексы каждого элемента:
Записываем формулу соединения: Si3N4.
В дальнейшем при составлении формул веществ не обязательно указывать цифрами значения валентностей, а необходимые несложные вычисления можно выполнять в уме.
Краткие выводы урока:
Надеюсь урок 6 «Валентность» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Валентность
Полезное
Смотреть что такое «Валентность» в других словарях:
ВАЛЕНТНОСТЬ — ВАЛЕНТНОСТЬ, мера «соединительной способности» химического элемента, равная числу индивидуальных ХИМИЧЕСКИХ СВЯЗЕЙ, которые может образовать один АТОМ. Валентность атома определяется числом ЭЛЕКТРОНОВ на самом верхнем (валентном) уровне (внешней… … Научно-технический энциклопедический словарь
ВАЛЕНТНОСТЬ — (от лат. valere иметь значение), или атомность, число атомов водорода или эквивалентных ему атомов или радикалов, к рое может присоединить данный атом или радикал. В. является одной из основ распределения элементов в периодической системе Д. И.… … Большая медицинская энциклопедия
Валентность — * валентнасць * valence термин происходит от лат. имеющий силу. 1. В химии это способность атомов химических элементов образовывать определенное число химических связей с атомами др. элементов. В свете строения атома В. это способность атомов… … Генетика. Энциклопедический словарь
ВАЛЕНТНОСТЬ — (от лат. valentia сила) в физике число, показывающее, со сколькими атомами водорода может соединяться данный атом или замещать их. В психологии валентность есть идущее из Англии обозначение для побуждающей способности. Философский… … Философская энциклопедия
валентность — атомность Словарь русских синонимов. валентность сущ., кол во синонимов: 1 • атомность (1) Словарь синонимов ASIS. В.Н. Тришин … Словарь синонимов
ВАЛЕНТНОСТЬ — (от лат. valentia – крепкий, прочный, влиятельный). Способность слова к грамматическому сочетанию с другими словами в предложении (например, у глаголов валентность определяет способность сочетаться с подлежащим, прямым или косвенным дополнением) … Новый словарь методических терминов и понятий (теория и практика обучения языкам)
ВАЛЕНТНОСТЬ — (от латинского valentia сила), способность атома химического элемента присоединять или замещать определенное число других атомов или атомных групп с образованием химической связи … Современная энциклопедия
ВАЛЕНТНОСТЬ — (от лат. valentia сила) способность атома химического элемента (или атомной группы) образовывать определенное число химических связей с другими атомами (или атомными группами). Вместо валентности часто пользуются более узкими понятиями, напр.… … Большой Энциклопедический словарь
ВАЛЕНТНОСТЬ — ВАЛЕНТНОСТЬ, валентности, мн. нет, жен. (от лат. valens имеющий ценность, значение) (хим.). То же, что атомность. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
ВАЛЕНТНОСТЬ — ВАЛЕНТНОСТЬ, и, жен. (спец.). Способность атома (или атомной группы) образовывать химические связи с другими атомами (или атомными группами). | прил. валентный, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
ВАЛЕНТНОСТЬ — (от лат. valentia сила), способность атомов элементов к образованию химических связей; количественно характеризуется числом. В. можно рассматривать как способность атома отдавать или присоединять определ. число эл нов внеш. электронных оболочек… … Физическая энциклопедия