Что такое гидроксильный показатель
Водородный и гидроксильный показатели: рН и рОН



1) нейтральная среда :
Чтобы избежать неудобств, связанных с применением чисел с отрицательными показателями степени, концентрацию водородных ионов принято выражать через водородный показатель и обозначать символом рН.
Водородным показателем рН называют десятичный логарифм концентрации водородных ионов, взятый с обратным знаком:
где [Н + ] – концентрация ионов водорода, моль/л.
Понятие «водородный показатель» было введено датским химиком Серенсеном в 1909 г.: буква «р» – начальная буква датского слова potenz – математическая степень, буква Н – символ водорода.
С помощью рН реакция растворов характеризуется так:
нейтральная рН=7, кислая рН 7.
С помощью рОН реакция растворов характеризуется так:
нейтральная рОН=7, кислая рОН>7, щелочная рОН
Понятие водородного и гидроксильного показателей
Равновесной концентрацией ионов водорода или гидроксила можно количественно охарактеризовать степень кислотности или щёлочности любого раствора. Чаще принято характеризовать растворы концентрацией ионов водорода:
Для удобства проведения расчётов – избавление от отрицательных степеней – в значениях концентраций ионов водорода и гидроксила предложено применять вместо подлинных значений концентраций [Н + ] и [ОН – ] их отрицательные логарифмы.
При увеличении концентрации водородных ионов величина рН уменьшается, при увеличении концентрации гидроксил-ионов величина рН увеличивается, т.е. в кислой среде рН 7.
Индикаторы – вещества, изменяющие свою окраску при взаимодействии с одним из реагирующих веществ реакции. Под интервалом (областью перехода) индикатора понимают промежуток значений рН, в котором происходит заметное изменение окраски индикатора. В таблице приведены интервалы некоторых индикаторов.
| Индикатор |  Область перехода ∆ Область перехода ∆ |  Цвет индикатора в средах кислой щелочной Цвет индикатора в средах кислой щелочной |
| Метиловый оранжевый | 3,2 – 4,4 | красный жёлтый |
| Лакмус | 5 – 8 | красный синий |
| Фенолфталеин | 8,2 – 10,0 |  бесцветный малиновый бесцветный малиновый |
| Метиловый красный | 4,2 – 6,2 | красный жёлтый |
Буферные растворы
Растворы, сохраняющие практически неизменными величины рН при разбавлении, либо при добавлении к ним небольших количеств кислот или щелочей называются буферными. Буферные растворы именуются часто буферными смесями, так как по составу они представляют смеси электролитов с одноимёнными ионами:
1. Слабой кислоты и одноимённой её соли. Например, ацетатный буфер:
СН3СООН и СН3СООNa.
2. Слабого основания и соли с одноимёнными катионами. Например, аммиачный буфер: NH4OH и NH4Cl.
3. Гидросолей многоосновных кислот с одноимёнными катионами. Например, NaН2РО4 и Na2НРО4.
4. Составы буферных смесей разнообразны и могут быть ещё более сложными.
Регулирующий механизм рН буферных растворов основан на смещении устанавливающихся в них равновесий. Например, в аммиачном буфере имеются следующие равновесные процессы: NH4OH D NH4 + + OH –
Расчётные формулы для вычисления рН буферных растворов представлены в таблице 3 приложения.
Гидролиз солей
Гидролизом называется ионообменное взаимодействие соли с водой, в результате которого образуются малодиссоциирующие соединения (ионы или молекулы). Продуктами гидролиза могут быть слабая кислота (или кислотные остатки) и слабое основание (или основные остатки).
При рассмотрении солей как продуктов взаимодействия кислоты с основанием в зависимости от силы их можно выделить 4 типа солей, образованных:
1) сильной кислотой и сильным основанием;
2) сильным основанием и слабой кислотой;
3) слабым основанием и сильной кислотой;
4) слабым основанием и слабой кислотой.
В зависимости от типов солей возможны 4 случая их гидролиза:
1. Соли, образованные сильным основанием и сильной кислотой (например, K2SO4, NaNO3, KCl, NaCl) гидролизу не подвергаются, так как при взаимодействии их с водой слабые электролиты не образуются. В таких растворах равновесие в процессе диссоциации воды не нарушается, реакция среды остаётся нейтральной.
Катионы натрия с водой не взаимодействуют.
Na2CO3 + Н2О D NaНCO3 +NaОН.
Анионы NO3 – сильной кислоты с водой не взаимодействуют. Катион Fe 3+ является катионом слабого основания Fe(ОН)3, основной остаток FeOH +2 взаимодействует с молекулами воды с образованием малодиссоциирующего продукта – основного остатка FeOH +2 :
Fe(NO3)3 + Н2О D (FeOH)( NO3)2 + НNO3.
Итак, при растворении в воде солей, образованных слабым основанием и
4. Если соль образована слабым основанием и слабой кислотой, происходит гидролиз её по катиону слабого основания и по аниону слабой кислоты – полный необратимый гидролиз до конечных продуктов гидролиза. Например, если сульфид алюминия Аl2S3, полученный сжиганием алюминия в порошке серы, бросить в воду, то моментально произойдёт бурная реакция гидролиза
Аl2S3: Аl2S3 + 6Н2О = 2Al(OH)3 + 3H2S.
В результате образуется осадок Al(OH)3 и выделится сероводород. Этот гидролиз необратим, поэтому реакцией обмена в растворе Аl2S3 получить нельзя. Вместо него образуются продукты гидролиза.
Уравнения необратимого гидролиза составляют только в молекулярной форме.
Расчётные формулы для вычисления рН растворов гидролизующихся солей представлены в таблице 3 приложения.
Дата добавления: 2016-09-06 ; просмотров: 4165 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
IV.Водородный и гидроксильный показатели растворов



Расчет pH и pOH растворов сильных кислот.
Cильные кислоты в растворе диссоциируют полностью:
c(B) – молярная концентрация кислоты, моль/л;
α – степень диссоциации;
Кислотность среды водного раствора сильной кислоты характеризуют водородным показателем рН:
Водородный и гидроксильный показатели взаимосвязаны:
Пример 11.ОпределитеpOH 0,1н раствора Н2SO4, степень электролитической диссоциации которой равна 90%.
Решение. Н2SO4 – сильный электролит, процесс диссоциации описывается уравнением: H2SO4 = 2H + + SO4 2- ; NH + = 2;
1. Определим молярную концентрацию кислоты:
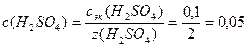
3.Определим рН раствора кислоты:
4. pOH = 14 – pH = 14 – 1,05= 12,95
Пример 12. Определите концентрацию гидроксид-ионов 5%-ного раствора HCl, степень электролитической диссоциации HCl равна 80%, плотность раствора 1,03 г/мл.
1. Определим молярную концентрацию HCl:
Примем m(р-ра)=100г, тогда m(HCl)= 5г,
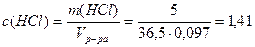
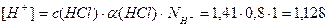
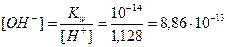
Пример 13. В 3л раствора содержится 0,015 моль HCl и 0,075 моль H2SO4, a(HCl)=1, a(H2SO4)=1. Определите pOH раствора.
Решение.Раствор содержит две сильные кислоты, уравнения их диссоциации:
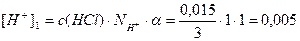
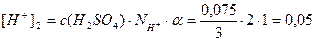
[H + ] = [H + ]1 + [H + ]2 = 0,005 + 0,05 = 0,055 моль/л;
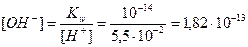
Пример 14.Рассчитайте pH раствора, полученного при смешивании 50 мл 0,1М HCl, 15мл 0,1M NaOH и 935мл H2O.
Решение. При смешивании щелочи и кислоты в растворе происходит реакция нейтрализации:
NaOH + HCl = NaCl + H2O
Реакция среды раствора будет определяться избытком
кислоты или щелочи, оставшейся после реакции.
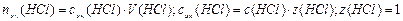
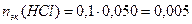
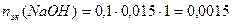
3. Взаимодействующие в ходе реакции вещества подчиняются закону эквивалентов: nэк(HCl) = nэк(NaOH). Следовательно, после реакции в растворе останется избыток HCl в количестве:
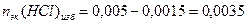
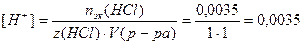
Ионное произведение воды. Водородный показатель
Теоретическое введение
Примеры решения задач
Задачи для самостоятельного решения
Теоретическое введение
Равновесие процесса диссоциации воды:
Н2О ↔ Н + + ОН —
описывается константой Кw, которая носит название “ионное произведение воды”. Ионное произведение воды равно:
Кw = [Н + ] [ОН — ] (1)
Для разбавленных водных растворов ионное произведение воды не зависит от состава раствора и постоянно при данной температуре. Так, Кw=10 — 14 для воды, миллимолярных растворов К2SO4, H2SO4 и KOH при Т=298 К. Строго говоря, постоянство Кw справедливо в случае, когда аналитические концентрации ионов заменены их активностями (лишь для малых концентраций Н + и ОН — значения концентрации и активности практически совпадают).
Процесс диссоциации Н2О идет с поглощением теплоты, поэтому при повышении температуры в интервале от 0 до 100 о С величина Кw увеличивается.
Для практических целей удобно пользоваться не концентрацией ионов водорода, а её водородным показателем – отрицательным десятичным логарифмом – рН. Величина рН равна:
рН = — lg[H + ]. (2)
Как выше отмечалось, более строгим является уравнение рН = – lg aН+, где aН+ – активность ионов водорода. Однако для практических целей при расчете рН разбавленных растворов обычно используется уравнение (2).
рН + рОН = 14, (3)
Для нейтральных растворов рН = 7, для кислых растворов рН 7. В аналитической практике редко приходится работать с растворами, рН которых выходит из интервала 0 ÷14. Тем не менее, в сильнощелочной среде рН может быть немного больше 14, а в очень кислой среде может принимать отрицательные значения.
Примеры решения задач
Задача 1. Вычислите рН 0,001М растворов HСl и КОН.
Решение. HСl и КОН являются сильными электролитами и в разбавленных растворах практически полностью диссоциируют на ионы. В растворе НСl: [Н + ] = 0,001 моль/л.
рН = –lg [H + ] = –lg 0,001 = 3
В растворе КОН: [ОН – ] = 0,001 моль/л. рОН = –lg [ОH — ] = –lg 0,001 = 3. рН=14 – 3 = 11.
Задача 2. Рассчитайте рН раствора КОН, 350 мл которого содержат 0,0035 моль КОН.
Решение.
КОН → К + + ОН —
рОН = –lg [ОH — ] = –lg 0,01 = 2.
рОН + рН = 14. рН = 14 – 2 = 12
или [Н + ] = 10 –14 /[ОН – ] = 10 –14 /0,01 = 10 –12 моль/л.
Задача 3. Вычислите молярную концентрацию раствора Ba(OH)2, если рН раствора составляет 12 при 298 К.
Решение.
Ba(OH)2 → Ва 2+ + 2ОН –
-lg [ОH – ] = 2, откуда [ОH – ] = 0,01 М.
Решение.
NH3 H2O ⇔ NH4 + + OH — или упрощенно: NH4ОH ⇔ NH4 + + OH —
рН = –lg [H + ] = –lg 2,4·10 –11 = 10,6.
Решение.
Присутствие в растворе CH3CОOH сильного электролита СН3СООNa приводит к сдвигу равновесия диссоциации уксусной кислоты влево в силу действия принципа Ле Шателье. В результате степень диссоциации уксусной кислоты уменьшается.
n(СН3СООNa) = 6:82 = 0,073 моль.
(считаем, что объем раствора после добавления 6 г СН3СООNa не изменился).
Ацетат–ионы в растворе образуются как за счет диссоциации уксусной кислоты:
так и за счет диссоциации СН3СООNa:
СН3СООNa → СН3СОО — + Na +
Поскольку СН3СООNa в растворе диссоциирует полностью, то концентрацией ацетат-ионов, образующихся при диссоциации уксусной кислоты можно пренебречь, так как она мала по сравнению с величиной 0,073 моль/л. Принимаем, что:
[H + ] = 1,75·10 –5 · 0,01 / 0,073 = 2,4·10 –6 моль/л.
Задачи для самостоятельного решения
1. Определите величину рН 0,0001 М раствора HCl.