Что такое гидроген пероксид
Пероксид водорода
| Пероксид водорода | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Пероксид водорода |
| Химическая формула | H2O2 |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Отн. молек. масса | 34,01 а. е. м. |
| Молярная масса | 34,01 г/моль |
| Плотность | 1.4 г/см³ |
| Термические свойства | |
| Температура плавления | −0,432 °C |
| Температура кипения | 150,2 °C |
| Энтальпия образования (ст. усл.) | -136.11 кДж/моль |
| Химические свойства | |
| pKa | 11.65 |
| Растворимость в воде | неограниченная |
| Классификация | |
| Рег. номер CAS | 7722-84-1 |
| SMILES | OO |
| Регистрационный номер EC | 231-765-0 |
Перокси́д водоро́да (перекись водорода), H2O2 — простейший представитель пероксидов. Бесцветная жидкость с «металлическим» вкусом, неограниченно растворимая в воде, спирте и эфире. Концентрированные водные растворы взрывоопасны. Пероксид водорода является хорошим растворителем. Из воды выделяется в виде неустойчивого кристаллогидрата H2O2•2H2O.
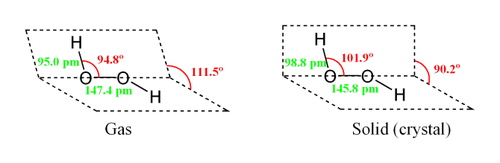
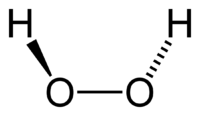
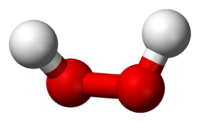
Молекула пероксида водорода имеет следующее строение:
Вследствие несимметричности молекула H2O2 сильно полярна (μ = 0,7·10 −29 Кл·м). Относительно высокая вязкость жидкого пероксида водорода обусловлена развитой системой водородных связей. Поскольку атомы кислорода имеют неподелённые электронные пары, молекула H2O2 также способна образовывать донорно-акцепторные связи.
Содержание
Химические свойства
Оба атома кислорода находятся в промежуточной степени окисления −1, что и обуславливает способность пероксидов выступать как в роли окислителей, так и восстановителей. Наиболее характерны для них окислительные свойства:

При взаимодействии с сильными окислителями пероксид водорода выступает в роли восстановителя, окисляясь до кислорода:
Молекула пероксида водорода сильно полярна, что приводит к возникновению водородных связей между молекулами. Связь O—O непрочна, поэтому H2O2 — неустойчивое соединение, легко разлагается. Так же этому может поспособствовать присутствие ионов переходных металлов. В разбавленных растворах пероксид водорода тоже не устойчив и самопроизвольно диспропорционирует на H2O и O2.Реакция диспропорционирования катализируется ионами переходных металлов, некоторыми белками:
Однако очень чистый пероксид водорода устойчив.
Пероксид водорода проявляет слабые кислотные свойства (К = 1,4·10 −12 ), и поэтому диссоциирует по двум ступеням:
При действии концентрированного раствора Н2O2 на некоторые гидроксиды в ряде случаев можно выделить пероксиды металлов, которые можно рассматривать как соли пероксида водорода (Li2O2, MgO2 и др.):

Пероксид водорода может проявлять как окислительные, так и восстановительные свойства. Например, при взаимодействии с оксидом серебра он является восстановителем:
В реакции с нитритом калия соединение служит окислителем:
Пероксидная группа [—O—O—] входит в состав многих веществ. Такие вещества называют пероксидами, или пероксидными соединениями. К ним относятся пероксиды металлов (Na2O2, BaO2 и др.). Кислоты, содержащие пероксидную группу, называют пероксокислотами, например, пероксомонофосфорная H3PO5 и пероксидисерная H2S2O8 кислоты.
Окислительно-восстановительные свойства
Пероксид водорода обладает окислительными, а также восстановительными свойствами. Он окисляет нитриты в нитраты, выделяет иод из иодидов металлов, расщепляет ненасыщенные соединения по месту двойных связей. Пероксид водорода восстанавливает соли золота и серебра, а также кислород при реакции с водным раствором перманганата калия в кислой среде.
При восстановлении Н2O2 образуется Н2O или ОН-, например:
При действии сильных окислителей H2O2 проявляет восстановительные свойства, выделяя свободный кислород:
Реакцию KMnO4 с Н2O2 используют в химическом анализе для определения содержания Н2O2:
Окисление органических соединений пероксидом водорода (например, сульфидов и тиолов) целесообразно проводить в среде уксусной кислоты.
Биологические свойства
Перекись водорода относится к реактивным формам кислорода и при повышенном образовании в клетке вызывает оксидативный стресс. Некоторые ферменты, например глюкозоксидаза, образуют в ходе окислительно-восстановительной реакции пероксид водорода, который может играть защитную роль в качестве бактерицидного агента. В клетках млекопитающих нет ферментов, которые бы восстанавливали кислород до перекиси водорода. Однако, несколько ферментных систем (ксантиноксидаза, НАД(Ф)H-оксидаза, циклоксигеназа и др.) продуцируют супероксид, который спонтанно или под действием супероксиддисмутазы превращается в перекись водорода.
Получение
Пероксид водорода получают в промышленности при реакции с участием органических веществ, в частности, каталитическим окислением изопропилового спирта:
Ценным побочным продуктом этой реакции является ацетон.
В промышленных масштабах пероксид водорода получают электролизом серной кислоты, в ходе которого образуется надсерная кислота, и последующим разложением последней до пероксида и серной кислоты.
В лабораторных условиях для получения пероксида водорода используют реакцию:
Концентрирование и очистку пероксида водорода проводят осторожной перегонкой.
Применение
Благодаря своим сильным окислительным свойствам пероксид водорода нашёл широкое применение в быту и в промышленности, где используется, например, как отбеливатель на текстильном производстве и при изготовлении бумаги. Применяется как ракетное топливо — в качестве окислителя или как однокомпонентное (с разложением на катализаторе). Используется в аналитической химии, в качестве пенообразователя при производстве пористых материалов, в производстве дезинфицирующих и отбеливающих средств. В промышленности пероксид водорода также находит свое применение в качестве катализатора, гидрирующего агента, как эпоксидирующий агент при эпоксидировании олефинов.
Хотя разбавленные растворы перекиси водорода применяется для небольших поверхностных ран, исследования показали что этот метод обеспечивая антисептический эффект и очищение и удлиняет время заживления. [1] [2] Обладая хорошими очищающими свойствами, перекись водорода на самом деле не ускоряет заживление ран. Достаточно высокие концентрации, обеспечивающие антисептический эффект, могут также удлинять время заживления из-за повреждения прилегающих к ране клеток. [3] Более того, перекись водорода может мешать заживлению и способствовать образованию рубцов из-за разрушения новообразующихся клеток кожи. [4] Однако, в качестве средства для очистки глубоких ран сложного профиля, гнойных затеков, флегмон, и других гнойных ран санация которых затруднена, перикись водорода остается препаратом выбора. Так как она обладает не только антисептическим эффектом, но и продуцирует большое количество пены, при взаимодействии с ферментом пероксидазой. Что в свою очередь позволяет размягчить и отделить от тканей некротизированные участки, сгустки крови, гноя, которые буду легко смыты последующим введением в полость раны антисептического раствора. Без предварительной обработки перекисью водорода, антисептический раствор не сможет удалить данные патологические образования, что приведет значительному увеличению времени заживления раны, и ухудшит состояние больного.
В пищевой промышленности растворы пероксида водорода применяются для дезинфекции технологических поверхностей оборудования, непосредственно соприкасающихся с продукцией. Кроме того, на предприятиях по производству молочной продукции, соков, растворы перекиси водорода используются для дезинфекции упаковки (технология «Тетра Пак»). Для технических целей пероксид водорода применяют в производстве электронной техники.
В быту применяется также для выведения пятен MnO2, получившихся при взаимодействии перманганата калия «марганцовки» с предметами (ввиду его окислительных свойств).
Пероксид водорода в аквариумистике
3%-ный раствор пероксида водорода используется в аквариумистике для оживления задохнувшейся рыбы, а также для очистки аквариумов и борьбы с нежелательной флорой и фауной в аквариуме (гидры, планарии, паразиты, водоросли, бактерии и др.)
Формы выпуска
Выпускается в виде водных растворов, стандартная концентрация 1-6 %, 30, 38, 50, 60, 85, 90 и 98 %. 30 % водный раствор пероксида водорода, стабилизированный добавлением фосфатов натрия, называется пергидролем.
Опасность применения
Несмотря на то, что пероксид водорода не токсичен, его концентрированные растворы при попадании на кожу, слизистые оболочки и в дыхательные пути вызывают ожоги. В больших концентрациях недостаточно чистый пероксид водорода может быть взрывоопасен. Опасен при приёме внутрь концентрированных растворов. Вызывает выраженные деструктивные изменения, сходные с действиями щелочей. Летальная доза 30%-го раствора пероксида водорода (пергидроля) — 50—100 мл. [7]
Пероксид водорода
Из Википедии — свободной энциклопедии
наименование
(при 20 °C)

Перокси́д водоро́да (пе́рекись водоро́да), H2O2 — простейший представитель пероксидов. Бесцветная тяжёлая полярная жидкость с «металлическим» вкусом, неограниченно растворимая в воде, спирте и эфире. Концентрированные водные растворы взрывоопасны. Пероксид водорода является хорошим растворителем. Из воды выделяется в виде неустойчивого кристаллогидрата H2O2∙2H2O.
Молекула пероксида водорода имеет следующее строение:
Вследствие несимметричности молекула H2O2 сильно полярна (μ = 0,7⋅10 −29 Кл·м). Относительно высокая вязкость жидкого пероксида водорода обусловлена развитой системой водородных связей. Поскольку атомы кислорода имеют неподелённые электронные пары, молекула H2O2 также способна образовывать донорно-акцепторные связи.
Перекись водорода : инструкция по применению
Описание
Бесцветная прозрачная жидкость.
Состав
Флакон 40 мл содержит:
действующее вещество: перекись водорода – 1,2 г;
вспомогательные вещества: натрия бензоат, вода очищенная.
Флакон 100 мл содержит:
действующее вещество: перекись водорода – 3 г;
вспомогательные вещества: натрия бензоат, вода очищенная.
Флакон 200 мл содержит:
действующее вещество: перекись водорода – 6 г;
вспомогательные вещества: натрия бензоат, вода очищенная.
Флакон 400 мл содержит:
действующее вещество: перекись водорода – 12 г;
вспомогательные вещества: натрия бензоат, вода очищенная.
Фармакотерапевтическая группа
Прочие антисептические и дезинфицирующие средства.
Фармакологическое действие
Антисептическое средство из группы оксидантов. При контакте перекиси водорода с поврежденной кожей или слизистыми оболочками высвобождается активный кислород, который обладает противомикробным, дезодорирующим, депигментирующим свойством, при этом происходит механическое очищение и инактивация органических веществ (протеины, кровь, гной). Антисептическое действие не является стерилизующим, при его применении происходит лишь временное уменьшение количества микроорганизмов. Обильное пенообразование способствует тромбообразованию и остановке кровотечений из мелких сосудов.
Показания к применению
Дезинфектант для обработки небольших порезов, ран (в том числе гнойных), изъязвлений кожи, ожогов.
Для остановки незначительных кровотечений (поверхностных, носовых).
Для полоскания полости рта и горла (при стоматите, ангине).
При гинекологических заболеваниях с целью дезинфекции.
Способ применения и дозы
Для наружного применения используют раствор 30 мг/мл; для полоскания полости рта и горла, нанесения на слизистые оболочки – раствор 2,5 мг/мл (раствор 30 мг/мл разводят водой в соотношении 1:11). Неразбавленный раствор не применяют для обработки слизистых оболочек. Поврежденные участки кожи или слизистой оболочки обрабатывают ватным или марлевым тампоном, смоченным раствором лекарственного средства. Тампоны следует держать пинцетом. Возможно струйное орошение раневой поверхности.
Побочное действие
При обработке раны возможно возникновение чувства жжения.
При длительном применении для полосканий возможна гипертрофия сосочков языка, потеря чувствительности.
Возможно проявление местных аллергических реакций при индивидуальной непереносимости лекарственного средства.
В случае возникновения побочных реакций, в т.ч. не указанных в данной инструкции, необходимо обратиться к врачу.
Противопоказания
Повышенная чувствительность к компонентам лекарственного средства.
Не используется в закрытых полостях тела и хирургических ранах из-за опасности газовой эмболии, как следствия поступления свободного кислорода в циркуляцию.
Не используется для дезинфекции хирургических инструментов (частей эндоскопов) и клизм.
Передозировка
Случайное попадание внутрь может стать причиной болезненности в глотке, желудочных сокращений и рвоты. Внезапное поступление свободного кислорода в желудочно-кишечный тракт может вызвать острое раздувание желудка и внутреннее кровотечение. Разрешается пить воду. Поступление больших объемов перекиси может привести к газовой эмболии, являющейся следствием высвобождения кислорода в желудок.
Меры предосторожности
Только для наружного применения. Не рекомендуется использовать лекарственное средство под окклюзионные повязки. Следует избегать попадания в глаза. Не применять для орошения закрытых полостей и проникающих ран во избежание высвобождения свободного кислорода в циркуляцию и возникновения газовой эмболии.
Не стабилен в щелочной среде, в присутствии щелочей металлов, сложных радикалов некоторых оксидантов, а также на свету и в тепле. Осветляет ткань.
Обработка раны раствором перекиси водорода не гарантирует защиту от заражения столбняком и др. раневой инфекцией.
Применение в педиатрической практике.
Для полоскания полости рта и горла применяется у детей с 12 лет. Применение у детей младшего возраста допускается только по показаниям врача.
Применение в гериатрической практике.
Нет достоверных данных.
Применение у лиц с нарушением функции печени и почек.
Нет достоверных данных.
Применение во время беременности и в период лактации
Нет достоверных данных. Перед применением лекарственного средства во время беременности и в период лактации необходимо проконсультироваться с врачом.
Перекись водорода (Hydrogen peroxide)
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Перекись водорода
Раствор для наружного и местного применения 3% прозрачный, бесцветный, без запаха.
| 100 мл | |
| водорода перекись | 7.5-11 г |
Вспомогательные вещества: натрия бензоат, вода очищенная.
Фармакологическое действие
Антисептическое средство из группы оксидантов. Обладает также гемостатическим эффектом. При контакте перекиси водорода с поврежденной кожей и слизистыми оболочками высвобождается активный кислород, при этом происходит механическое очищение и инактивация органических веществ (протеины, кровь, гной). Антисептическое действие перекиси водорода не является стерилизующим, при его применении происходит лишь временное уменьшение количества микроорганизмов.
Показания активных веществ препарата Перекись водорода
Воспалительные заболевания слизистых оболочек, гнойные раны, капиллярное кровотечение из поверхностных ран, носовые кровотечения. Для дезинфекции и дезодорирования: стоматит, тонзиллит, гинекологические заболевания.
Открыть список кодов МКБ-10
| Код МКБ-10 | Показание |
| J03 | Острый тонзиллит |
| J35.0 | Хронический тонзиллит |
| K05 | Гингивит и болезни пародонта |
| K12 | Стоматит и родственные поражения |
| N76 | Другие воспалительные болезни влагалища и вульвы |
| R04.0 | Носовое кровотечение |
| R58 | Кровотечение, не классифицированное в других рубриках |
| T14.0 | Поверхностная травма неуточненной области тела (в т.ч. ссадина, кровоподтек, ушиб, гематома, укус неядовитого насекомого) |
| T79.3 | Посттравматическая раневая инфекция, не классифицированная в других рубриках |
Режим дозирования
Побочное действие
Противопоказания к применению
Применение при беременности и кормлении грудью
Возможно применение при беременности и в период грудного вскармливания по показаниям, в рекомендуемых дозах.
Особые указания
Не применяют для орошения полостей.
Не рекомендуют использовать средство под окклюзионные повязки.
Перекись водорода (Hydrogen peroxide) ОПИСАНИЕ
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Перекись водорода
Раствор для наружного и местного применения 3% прозрачный, бесцветный, без запаха.
| 100 мл | |
| водорода перекись | 7.5-11 г |
Вспомогательные вещества: натрия бензоат, вода очищенная.
Фармакологическое действие
Антисептическое средство из группы оксидантов. Обладает также гемостатическим эффектом. При контакте перекиси водорода с поврежденной кожей и слизистыми оболочками высвобождается активный кислород, при этом происходит механическое очищение и инактивация органических веществ (протеины, кровь, гной). Антисептическое действие перекиси водорода не является стерилизующим, при его применении происходит лишь временное уменьшение количества микроорганизмов.
Показания активных веществ препарата Перекись водорода
Воспалительные заболевания слизистых оболочек, гнойные раны, капиллярное кровотечение из поверхностных ран, носовые кровотечения. Для дезинфекции и дезодорирования: стоматит, тонзиллит, гинекологические заболевания.
Открыть список кодов МКБ-10
| Код МКБ-10 | Показание |
| J03 | Острый тонзиллит |
| J35.0 | Хронический тонзиллит |
| K05 | Гингивит и болезни пародонта |
| K12 | Стоматит и родственные поражения |
| N76 | Другие воспалительные болезни влагалища и вульвы |
| R04.0 | Носовое кровотечение |
| R58 | Кровотечение, не классифицированное в других рубриках |
| T14.0 | Поверхностная травма неуточненной области тела (в т.ч. ссадина, кровоподтек, ушиб, гематома, укус неядовитого насекомого) |
| T79.3 | Посттравматическая раневая инфекция, не классифицированная в других рубриках |
Режим дозирования
Побочное действие
Противопоказания к применению
Применение при беременности и кормлении грудью
Возможно применение при беременности и в период грудного вскармливания по показаниям, в рекомендуемых дозах.
Особые указания
Не применяют для орошения полостей.
Не рекомендуют использовать средство под окклюзионные повязки.