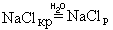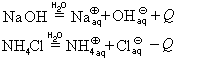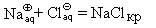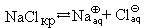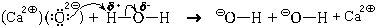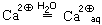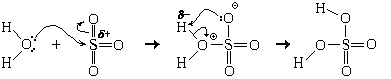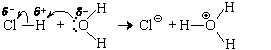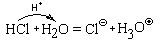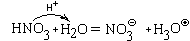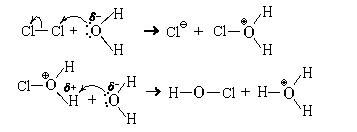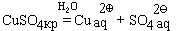Что такое гидратная оболочка
Что такое гидратная оболочка
• Соли, растворенные в воде, диссоциируют на гидратированные ионы
• Гидрофобные свойства липидного бислоя создают барьер при движении гидратированных ионов через мембрану
• Ионные каналы катализируют процесс частичной дегидратации ионов. Это обеспечивает их быстрый и селективный транспорт через мембраны
• Процесс дегидратации ионов является энергозависимым. Напротив, при их гидратации происходит высвобождение энергии
Поскольку липидный бислой мембраны обладает гидрофобными свойствами, заряженные ионы самостоятельно через нее не проходят. Для транспорта через мембрану ионы должны пройти через специальные трансмембранные белки: ионные каналы и переносчики. В этом разделе мы рассмотрим некоторые физические свойства ионов в растворе и их влияние на процесс транспорта.
Ионы в растворе находятся в гидратированном состоянии, т. е. окружены молекулами воды. Ионы, заряженные положительно или отрицательно, притягивают молекулы-диполи воды, частичный отрицательный заряд которых создается атомом кислорода, а частичный положительный — атомами водорода.
Гидратация ионов, например, обусловливает быстрое растворение кристаллов NaCl в воде. Этот процесс выгоден с энергетической точки зрения, поскольку молекулы воды присоединяются к свободным ионам Na+ и Cl-.
Молекулы воды образуют вокруг ионов слой, называемый гидратной оболочкой. За счет этого заряд иона, находящегося в растворе, частично нейтрализуется. Таким образом, бислой мембраны служит эффективным барьером, не пропускающим гидратированные ионы.
Поскольку гидратация ионов является энергетически выгодным процессом, для удаления гидратной оболочки и проникновения иона в гидрофобное окружение липидного бислоя необходимо довольно большое количество энергии. В процессе трансмембранного транспорта ионные каналы помогают преодолеть этот энергетический барьер.
Форма гидратной оболочки зависит от размера и заряда ионов. Диполи воды ориентируются по отношению к катионам и анионам в соответствии с их зарядом и размерами. По сравнению с крупными ионами, более мелкие, имеющие такой же заряд, характеризуются большей степенью его локализованности, что приводит к более высокой плотности заряда на мелких ионах.
Более высокая плотность заряда создает более сильное электрическое поле, которое притягивает больше молекул воды, и, таким образом, толщина гидратной оболочки увеличивается. Поэтому у меньшего по размеру иона гидратная оболочка больше, чем у более крупного иона, обладающего тем же зарядом. Следовательно, при проникновении через поры канала мелкие ионы характеризуются большим эффективным радиусом.
Какую роль играет степень гидратации в процессах ионного транспорта? Ионные каналы создают окружение, которое напоминает заполненные водой поры и, таким образом, по мере транспорта ионов по каналу облегчается их частичная дегидратация.
Продвигаясь по каналу, ион образует слабые электростатические связи с заряженными остатками аминокислот, которые имитируют гидратную оболочку. Тем самым процесс транспорта становится энергетически выгодным и в то же время приобретает селективность. Селективность ионного канала зависит от его способности катализировать энергетически выгодный процесс частичной дегидратации определенных ионов. Это достигается за счет специфических размеров канала и наличия специфических сайтов связывания ионов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
ОСАЖДЕНИЕ НАТИВНЫХ БЕЛКОВ



СПОСОБЫ ОСАЖДЕНИЯ БЕЛКОВ
Свойства воды гидратной оболочки
ФАКТОРЫ СТАБИЛИЗАЦИИ БЕЛКА В РАСТВОРЕ.
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА БЕЛКОВ. РАСТВОРИМОСТЬ БЕЛКОВ В ВОДЕ.
а) Температура кипения выше 100 0 С.
б) Температура замерзания ниже 0 О С.
в) В воде гидратной оболочки не растворяются различные соли и другие гидрофильные вещества.
г) Окружая каждую молекулу белка, гидратная оболочка не дает этим белковым молекулам сблизиться, соединиться и выпасть в осадок.
Делятся на две группы:
1) Способы осаждения нативного белка
2) Способы осаждения денатурированного белка
Чтобы осадить белок из раствора, надо лишить его обоих факторов стабилизации: и заряда, и гидратной оболочки.
Наиболее типичным примером осаждения нативного белка является ВЫСАЛИВАНИЕ.
При высаливании сохраняется нативность белковых молекул. Если осадить белки с помощью высаливания, а затем уменьшить концентрацию солей, например, методом диализа, то белок опять растворится.
Осаждения белков без потери ими нативности можно достичь также с помощью водоотнимающих средств.
б) ПРИМЕНЕНИЕ ВОДООТНИМАЮЩИХ СРЕДСТВ. Такими средствами являются растворители, которые смешиваются с водой в любых соотношениях. Чаще всего это ацетон, этиловый спирт. Эти вещества отнимают гидратные оболочки белков, и белки выпадают в осадок, если они лишены заряда. Но, в отличие от высаливания, осадок сразу (немедленно!) должен быть отделен от растворителя. Если растворитель и белок будут длительно находиться в контакте, то могут произойти необратимые изменения структуры белковой молекулы (денатурация).
Что такое гидратная оболочка
§ 9. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА БЕЛКОВ
Белки – это очень крупные молекулы, по своим размерам они могут уступать только отдельным представителям нуклеиновых кислот и полисахаридам. В таблице 4 представлены молекулярные характеристики некоторые белков.
Молекулярные характеристики некоторых белков
Относитель-ная молекулярная масса
Число аминокислотных остатков
Зная относительную молекулярную массу белка, можно приблизительно оценить, какое число аминокислотных остатков входит в его состав. Средняя относительная молекулярная масса аминокислот, образующих полипептидную цепь, равна 128. При образовании пептидной связи происходит отщепление молекулы воды, следовательно, средняя относительная масса аминокислотного остатка составит 128 – 18 = 110. Используя эти данные, можно подсчитать, что белок с относительной молекулярной массой 100000 будет состоять приблизительно из 909 аминокислотных остатков.
Электрические свойства белковых молекул
Электрические свойства белков определяются присутствием на их поверхности положительно и отрицательно заряженных аминокислотных остатков. Наличие заряженных группировок белка определяет суммарный заряд белковой молекулы. Если в белках преобладают отрицательно заряженные аминокислоты, то его молекула в нейтральном растворе будет иметь отрицательный заряд, если преобладают положительно заряженные – молекула будет иметь положительный заряд. Суммарный заряд белковой молекулы зависит и от кислотности (рН) среды. При увеличении концентрации ионов водорода (увеличении кислотности) происходит подавление диссоциации карбоксильных групп:
и в то же время увеличивается число протонированных амино-групп;
Таким образом, при увеличении кислотности среды происходит уменьшение на поверхности молекулы белка числа отрицательно заряженных и увеличение числа положительно заряженных групп. Совсем другая картина наблюдается при снижении концентрации ионов водорода и увеличении концентрации гидроксид-ионов. Число диссоциированных карбоксильных групп возрастает
и снижается число протонированных аминогрупп
Итак, изменяя кислотность среды, можно изменить и заряд молекулы белка. При увеличении кислотности среды в молекуле белка снижается число отрицательно заряженных группировок и увеличивается число положительно заряженных, молекула постепенно теряет отрицательный и приобретает положительный заряд. При снижении кислотности раствора наблюдается противоположная картина. Очевидно, что при определенных значениях рН молекула будет электронейтральной, т.е. число положительно заряженных групп будет равно числу отрицательно заряженных групп, и суммарный заряд молекулы будет равен нулю (рис. 14).
Значение рН, при котором суммарный заряд белка равен нулю, называется изоэлектрической точкой и обозначается pI.
Рис. 14. В состоянии изоэлектрической точки суммарный заряд молекулы белка равен нулю
Изоэлектрическая точка для большинства белков находится в области рН от 4,5 до 6,5. Однако есть и исключения. Ниже приведены изоэлектрические точки некоторых белков:
При значениях рН ниже изоэлектрической точки белок несет суммарный положительный заряд, выше – суммарный отрицательный.
Растворимость белков
Рис. 15. Образование гидратной оболочки вокруг молекулы белка.
На растворимость белка влияет наличие нейтральных солей (Na2SO4, (NH4)2SO4 и др.) в растворе. При малых концентрациях солей растворимость белка увеличивается (рис. 16), так как в таких условиях увеличивается степень диссоциации полярных групп и экранируются заряженные группы белковых молекул, тем самым снижается белок-белковое взаимодействие, способствующее образованию агрегатов и выпадению белка в осадок. При высоких концентрациях солей растворимость белка снижается (рис. 16) вследствие разрушения гидратной оболочки, приводящего к агрегации молекул белка.
Рис. 16. Зависимость растворимости белка от концентрации соли
Существуют белки, которые растворяются только в растворах солей и не растворяются в чистой воде, такие белки называют глобулины. Существуют и другие белки – альбумины, они в отличие от глобулинов хорошо растворимы в чистой воде.
Растворимость белков зависит и от рН растворов. Как мы уже отмечали, минимальной растворимостью обладают белки в изоэлектрической точке, что объясняется отсутствием электростатического отталкивания между молекулами белка.
При определенных условиях белки могут образовывать гели. При образовании геля молекулы белка формируют густую сеть, внутреннее пространство которой заполнено растворителем. Гели образуют, например, желатина (этот белок используют для приготовления желе) и белки молока при приготовлении простокваши.
На растворимость белка оказывает влияние и температура. При действии высокой температуры многие белки выпадают в осадок вследствие нарушения их структуры, но об этом более подробно поговорим в следующем разделе.
Денатурация белка
Рис. 17. Денатурация белка
При денатурации гидрофобные радикалы аминокислот, находящиеся в нативных белках в глубине молекулы, оказываются на поверхности, в результате создаются условия для агрегации. Агрегаты белковых молекул выпадают в осадок. Денатурация сопровождается потерей биологической функции белка.
Денатурация белка может быть вызвана не только повышенной температурой, но и другими факторами. Кислоты и щелочи способны вызвать денатурацию белка: в результате их действия происходит перезарядка ионогенных групп, что приводит к разрыву ионных и водородных связей. Мочевина разрушает водородные связи, следствием этого является потеря белками своей нативной структуры. Денатурирующими агентами являются органические растворители и ионы тяжелых металлов: органические растворители разрушают гидрофобные связи, а ионы тяжелых металлов образуют нерастворимые комплексы с белками.
Наряду с денатурацией существует и обратный процесс – ренатурация. При снятии денатурирующего фактора возможно восстановление исходной нативной структуры. Например, при медленном охлаждении до комнатной температуры раствора восстанавливается нативная структура и биологическая функция трипсина.
Белки могут денатурировать и в клетке при протекании нормальных процессов жизнедеятельности. Совершенно очевидно, что утрата нативной структуры и функции белков – крайне нежелательное событие. В связи с этим следует упомянуть об особых белках – шаперонах. Эти белки способны узнавать частично денатурированные белки и, связываясь с ними, восстанавливать их нативную конформацию. Шапероны также узнают белки, процесс денатурации которых зашел далеко, и транспортируют их в лизосомы, где происходит их расщепление (деградация). Шапероны играют важную роль и в процессе формирования третичной и четвертичной структур во время синтеза белка.
Интересно знать! В настоящее время часто упоминается такое заболевание, как коровье бешенство. Эту болезнь вызывают прионы. Они могут вызывать у животных и человека и другие заболевания, носящие нейродегенеративный характер. Прионы – это инфекционные агенты белковой природы. Прион, попадая в клетку, вызывает изменение конформации своего клеточного аналога, который сам становится прионом. Так возникает заболевание. Прионный белок отличается от клеточного по вторичной структуре. Прионная форма белка имеет в основном b-складчатую структуру, а клеточная – a-спиральную.
Что такое гидратная оболочка
11.1. Физическое растворение
При попадании какого-либо вещества в воду оно может:
а) раствориться в воде, то есть перемешаться с ней на атомно-молекулярном уровне;
б) вступить с водой в химическую реакцию;
в) не раствориться и не прореагировать.
От чего же зависит результат взаимодействия вещества с водой? Естественно, от характеристик вещества и от характеристик воды.
Начнем с растворения и рассмотрим, какие характеристики воды и взаимодействующих с ней веществ имеют наибольшее значение в этих процессах.
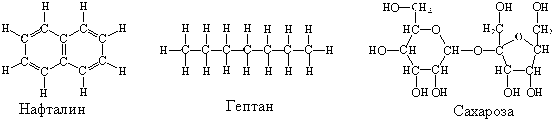
Поместим в две пробирки по небольшой порции нафталина С10Н8. Нальем в одну из пробирок воду, а в другую – гептан С7Н16 (можно вместо чистого гептана использовать бензин). Нафталин в гептане растворится, а в воде – нет. Проверим, действительно ли нафталин растворился в гептане или прореагировал с ним. Для этого поместим несколько капель раствора на стекло и подождем, пока гептан испарится – на стекле образуются бесцветные пластинчатые кристаллики. В том, что это нафталин, можно убедиться по характерному запаху.
Одно из отличий гептана от воды в том, что его молекулы неполярны, а молекулы воды полярны. Кроме того, между молекулами воды есть водородные связи, а между молекулами гептана их нет.
Для растворения нафталина в гептане требуется разорвать слабые межмолекулярные связи между молекулами нафталина и слабые межмолекулярные связи между молекулами гептана. При растворении образуются столь же слабые межмолекулярные связи между молекулами нафталина и гептана. Тепловой эффект такого процесса практически равен нулю.
За счет чего же нафталин растворяется в гептане? Только за счет энтропийного фактора (растет беспорядок в системе нафталин – гептан).
Для растворения нафталина в воде необходимо, кроме слабых связей между его молекулами, разорвать водородные связи между молекулами воды. При этом водородные связи между молекулами нафталина и воды не образуются. Процесс получается эндотермическим и настолько энергетически невыгодным, что энтропийный фактор здесь помочь не в силах.
А если вместо нафталина взять другое вещество, молекулы которого способны образовывать водородные связи с молекулами воды, то будет ли такое вещество растворяться в воде?
Если нет других препятствий, то будет. Например, вы знаете, что сахар (сахароза С12Н22О11) прекрасно растворим в воде. Посмотрев на структурную формулу сахарозы, вы увидите, что в ее молекуле есть группы –О–Н, способные образовывать водородные связи с молекулами воды.
Убедитесь экспериментально, что сахароза малорастворима в гептане, и попробуйте самостоятельно объяснить, почему так различаются свойства нафталина и сахарозы.
Растворение нафталина в гептане и сахарозы в воде называют физическим растворением.
| Физическое растворение – растворение, при котором происходит разрыв и образование только межмолекулярных связей (включая водородные). |
Физически растворяться могут только молекулярные вещества.
| Растворитель – вещество, которое до образования раствора находилось в том же агрегатном состоянии, что и образовавшийся раствор. |
Другие компоненты раствора называются растворенными веществами.
Выявленные нами закономерности относятся и к случаям растворения в воде (да и в большинстве других растворителей) жидких и газообразных веществ. Если все вещества, образующие раствор, до растворения находились в одном агрегатном состоянии, то растворителем обычно называют то вещество, которого в растворе больше. Исключение из этого правила – вода: ее обычно называют растворителем, даже если ее меньше, чем растворенного вещества.
Причиной физического растворения вещества в воде может быть не только образование водородных связей между молекулами растворяемого вещества и воды, но и образование других видов межмолекулярных связей. Так бывает прежде всего в случае растворения в воде газообразных веществ (например, углекислого газа или хлора), в которых молекулы вообще не связаны друг с другом, а также некоторых жидкостей с очень слабыми межмолекулярными связями (например, брома). Выигрыш в энергии достигается здесь за счет ориентации диполей (молекул воды) вокруг полярных молекул или полярных связей в растворяемом веществе, а в случае хлора или брома –вызван склонностью к присоединению электронов атомов хлора и брома, сохраняющейся и в молекулах этих простых веществ (подробнее –в § 11.4).
Во всех этих случаях вещества значительно хуже растворяются в воде, чем при образовании водородных связей.
Если из раствора удалить растворитель (например так, как вы это делали в случае раствора нафталина в гептане), то растворенное вещество выделится в химически неизменном виде.


2.Подскажите знак теплового эффекта растворения в воде этилового спирта (этанола).
3.Почему аммиак хорошо растворим в воде, а кислород – плохо?
4.Какое вещество лучше растворимо в воде – аммиак или фосфин (PH3)?
5.Объясните причину лучшей растворимости в воде озона, чем кислорода.
6.Определите массовую долю глюкозы (виноградного сахара, С6Н12О6) в водном растворе, если для его приготовления использовали 120 мл воды и 30 г глюкозы (плотность воды примите равной 1 г/мл). Какова концентрация глюкозы в этом растворе, если плотность раствора равна 1,15 г/мл?
7.Сколько сахара (сахарозы) можно выделить из 250 г сиропа с массовой долей воды, равной 35 %?.
2. Приготовление растворов.
В первом параграфе мы рассмотрели случаи растворения веществ, при которых химические связи оставались неизменными. Но так бывает далеко не всегда.
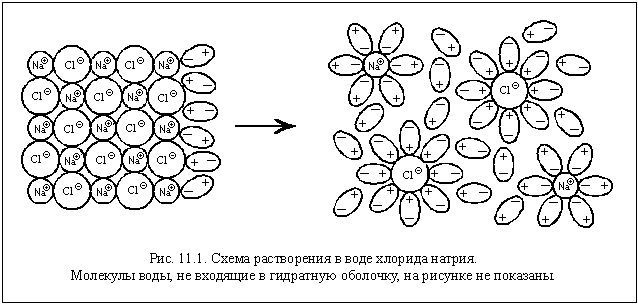
Поместим в пробирку несколько кристаллов хлорида натрия и добавим воду. Через некоторое время кристаллы растворятся. Что произошло?
Хлорид натрия – вещество немолекулярное. Кристалл NaCl состоит из ионов Na 
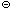
| Гидратная оболочка – окружение иона, состоящее из одного или нескольких слоев определенным образом ориентированных молекул воды. |
В виде уравнения реакции это можно записать так:
NaClкр + (n + m)H2O = [Na(H2O)n] 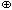
или сокращенно 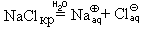
Можно записать и «молекулярное» уравнение этого процесса:(такое название сохранилось с тех пор, когда предполагалось, что все вещества состоят из молекул)
Гидратация – процесс образования гидратной оболочки.
Гидратированные ионы слабее притягиваются друг к другу, и энергии теплового движения оказывается достаточно для того, чтобы эти ионы не слипались в кристалл.
Практически наличие ионов в растворе легко подтвердить, изучив электропроводность хлорида натрия, воды и получившегося раствора. Вы уже знаете, что кристаллы хлорида натрия электрический ток не проводят, потому что в них хоть и есть заряженные частицы – ионы, но они » закреплены» в кристалле и не могут двигаться. Вода проводит электрический ток очень плохо, потому что в ней хоть и образуются за счет автопротолиза ионы оксония и гидроксид-ионы, но их очень мало. Раствор хлорида натрия, наоборот, хорошо проводит электрический ток, потому что в нем много ионов, и они могут свободно двигаться, в том числе под действием электрического напряжения.
Для разрыва ионных связей в кристалле и водородных связей в воде необходимо затратить энергию. При гидратации ионов энергия выделяется. Если затраты энергии на разрыв связей превышают энергию, выделяющуюся при гидратации ионов, то растворение эндотермическое, а если наоборот, то – экзотермическое.
Хлорид натрия растворяется в воде с практически нулевым тепловым эффектом, следовательно, растворение этой соли происходит только за счет увеличения энтропии. Но обычно растворение сопровождается заметным выделением теплоты (Na2CO3, CaCl2, NaOH и др.) или ее поглощением (KNO3, NH4Cl и др.), например:
При выпаривании воды из растворов, получившихся при химическом растворении, из них вновь выделяются растворенные вещества в химически неизменном виде.
| Химическое растворение – растворение, при котором происходит разрыв химических связей. |
И при физическом, и при химическом растворении образуется раствор того вещества, которое мы растворяли, например, раствор сахара в воде или раствор хлорида натрия в воде. Иными словами, растворенное вещество может быть выделено из раствора при удалении воды.
Любая порция помещенного в воду хлорида натрия (или другого подобного вещества) всегда растворялась бы полностью, если бы кроме процесса растворения
не протекал бы обратный процесс – процесс кристаллизации исходного вещества из раствора:
В момент помещения кристалла в воду скорость процесса кристаллизации равна нулю, но, по мере увеличения концентрации ионов в растворе, она увеличивается и в какой-то момент становится равной скорости растворения. Наступает состояние равновесия:
образовавшийся при этом раствор называется насыщенным.
| Насыщенный раствор – раствор, находящийся в равновесии с растворяемым веществом. |
| Растворимость вещества (в данном растворителе) – характеристика состава насыщенного раствора этого вещества. |


2.Определите массовую долю нитрата калия в насыщенном при 20 °С водном растворе этой соли, если при приготовлении такого раствора к 200 г воды прибавили 100 г нитрата калия, и при этом после окончания приготовления раствора 36,8 г нитрата калия не растворилось.
3.Можно ли при 20 °С приготовить водный раствор хромата калия K2CrO4 с массовой долей растворенного вещества, равной 45 %, если при этой температуре в 100 г воды растворяется не более 63,9 г этой соли.
4.Массовая доля бромида калия в насыщенном водном растворе при 0 °С равна 34,5 %, а при 80 °С – 48,8 %. Определите массу бромида калия, выделившегося при охлаждении до 0 °С 250 г насыщенного при 80°С водного раствора этой соли.
5.Массовая доля гидроксида кальция в насыщенном водном растворе при 20 °С равна 0,12 %. Сколько литров насыщенного при этой температуре раствора гидроксида кальция (известковой воды) можно получить, имея в своем распоряжении 100 г гидроксида кальция? Плотность раствора примите равной 1 г/мл.
6.При 25 °C массовая доля сульфата бария в насыщенном водном растворе составляет 2,33·10 –2 %. Определите минимальный объем воды, необходимой для полного растворения 1 г этой соли.
Многие вещества при соприкосновении с водой вступают с ней в химические реакции. В результате такого взаимодействия при избытке воды, как и при растворении, получается раствор. Но если из этого раствора удалить воду, исходного вещества мы не получим.
Какие продукты образуются при химической реакции вещества с водой? Это зависит от типа химической связи в веществе; если связи ковалентные, то от степени полярности этих связей. Кроме этого, влияние оказывают и другие факторы, с некоторыми из которых мы познакомимся.
а) Соединения с ионной связью
Большинство ионных соединений либо химически растворяются в воде, либо не растворяются. Особняком стоят ионные гидриды и оксиды, то есть соединения, содержащие те же элементы, что и сама вода, и некоторые другие вещества. Поведение ионных оксидов при контакте с водой рассмотрим на примере оксида кальция.
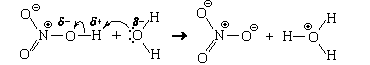
Оксид кальция, будучи ионным веществом, мог бы химически растворяться в воде. При этом в раствор переходили бы ионы кальция и оксид-ионы. Но двухзарядный анион – не самое устойчивое валентное состояние атома кислорода (хотя бы потому, что энергия сродства ко второму электрону всегда отрицательна, да и радиус оксид-иона сравнительно мал). Поэтому атомы кислорода стремятся понизить свой формальный заряд. В присутствии воды это оказывается возможным. Оказавшиеся на поверхности кристалла оксид-ионы взаимодействуют с молекулами воды. Эту реакцию можно представить в виде схемы, показывающей ее механизм (схемы механизма).
Для лучшего понимания происходящего условно разделим этот процесс на этапы:
1. Молекула воды поворачивается к оксидному иону атомом водорода (противоположно заряжены).
2. Оксид-ион делится с атомом водорода неподеленной парой электронов; между ними образуется ковалентная связь (образуется по донорно-акцепторному механизму).
3. У атома водорода на единственной валентной орбитали (1s) оказывается четыре электрона (два «старых» и два «новых»), что противоречит принципу Паули. Поэтому атом водорода отдает пару электронов связи («старых» электронов) атому кислорода, входящему в состав молекулы воды, тем более что эта пара электронов и так была в значительной степени смещена к атому кислорода. Связь между атомом водорода и атомом кислорода разрывается.
4. За счет образования связи по донорно-акцепторному механизму формальный заряд на бывшем оксидном ионе становится равным –1 е; на атоме кислорода, входившем прежде в состав молекулы воды, появляется заряд, также равный –1 е. Таким образом образуются два гидроксидных иона.
5. Не связанные теперь ионной связью с оксид-ионами ионы кальция переходят в раствор и гидратируются:
Положительный заряд ионов кальция как бы «размывается» по всему гидратированному иону.
6. Образовавшиеся гидроксид-ионы тоже гидратируются:
Отрицательный заряд гидроксид-иона при этом тоже «размывается».
Суммарное ионное уравнение реакции оксида кальция с водой
CaOкр + H2O 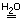
aq + 2OH
В растворе появляются ионы кальция и гидроксид-ионы в соотношении 1:2. То же самое получилось бы при растворении в воде гидроксида кальция. И действительно, выпарив воду и высушив остаток, мы можем получить из этого раствора кристаллический гидроксид кальция (но отнюдь не оксид!). Поэтому часто уравнение этой реакции записывают так:
и называют » молекулярным » уравнением этой реакции. И в тех, и в других уравнениях буквенные индексы иногда не приводят, что часто сильно затрудняет понимание происходящих процессов, а то и просто вводит в заблуждение. Вместе с тем, отсутствие буквенных индексов в уравнениях допустимо, например, при решении расчетных задач
Кроме оксида кальция, точно также взаимодействуют с водой следующие оксиды: Li2O, Na2O, K2O, Rb2O, Cs2O, SrO, BaO – то есть оксиды тех металлов, которые и сами реагируют с водой. Все эти оксиды относятся к основным оксидам. Остальные ионные оксиды с водой не реагируют.
Совершенно аналогично реагируют с водой и ионные гидриды, например, гидрид натрия NaH. Ион натрия только гидратируется, а гидрид-ион реагирует с молекулой воды:
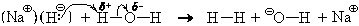
В результате в растворе остается гидроксид натрия.
Ионное уравнение этой реакции
NaHкр + H2O = Na 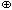
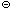
,
а » молекулярное» уравнение – NaHкр + H2O = NaOHр + H2 .
б) Вещества с металлической связью
В качестве примера рассмотрим взаимодействие с водой натрия.
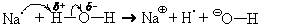
На схемах кривая полустрелка означает передачу или перемещение о д н о г о э л е к т р о н а
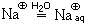
так же, как и ион натрия, гидратируется гидроксид-ион 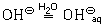
Из-за неполярности своих молекул водород в воде практически нерастворим и выделяется из раствора в виде газа. Ионное уравнение этой реакции
2Naкр + 2H2O = 2Na 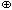
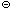
2Naкр + 2H2O = 2NaOHр + H2
Так же, как натрий, при комнатной температуре с водой бурно реагируют Li, К, Rb, Cs, Ca, Sr, Ba. При нагревании с ней реагирует и Mg, а также некоторые другие металлы.
в) Вещества с ковалентными связями
Аналогично, но несколько более сложно с водой реагирует N2O5, P4O10 и некоторые другие молекулярные оксиды. Все они – кислотные оксиды.
N2O5 + H2O = 2HNO3;
P4O10 + 6H2O = 4H3PO4.
Во всех этих реакциях образуются кислоты, которые при наличии избытка воды с ней реагируют. Но, прежде чем рассмотреть механизм этих реакций, посмотрим, как реагирует с водой хлороводород – молекулярное вещество с сильно полярными ковалентными связями между атомами водорода и хлора:
HClг + H2O = H3O 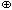
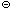
При низких температурах из такого раствора может быть выделен кристаллический хлорид оксония (H3O)Cl (tпл = –15 °С).
Взаимодействие HCl и H2O можно представить себе и по-другому:
то есть как результат передачи протона от молекулы хлороводорода к молекуле воды. Следовательно, это кислотно-основная реакция.
Аналогично происходит взаимодействие с водой азотной кислоты
что тоже можно представит как передачу протона:
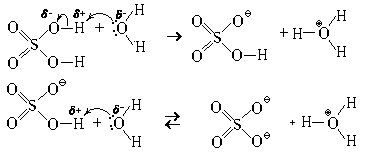
Кислоты, в молекулах которых несколько гидроксилов (OH-групп), реагируют с водой в несколько стадий (ступенчато). Пример – серная кислота.
Второй протон отщепляется значительно труднее, чем первый, поэтому вторая стадия этого процесса обратима. Сравнив величину и распределение зарядов в молекуле серной кислоты и в гидросульфат-ионе, попробуйте самостоятельно объяснить это явление.
При охлаждении из растворов серной кислоты могут быть выделены индивидуальные вещества: (H3O)HSO4 (tпл = 8,5 °С) и (H3O)2SO4 (tпл = – 40 °С).
Анионы, образующиеся из молекул кислот после отрыва одного или нескольких протонов, называются кислотными остатками.
Из молекулярных простых веществ с водой при обычных условиях реагируют только F2, Cl2, Br2 и, в крайне незначительной степени, I2. Фтор бурно реагирует с водой, полностью ее окисляя:
При этом протекают также и другие реакции.
Значительно важнее реакция хлора с водой. Обладая высокой склонностью к присоединению электронов (молярная энергия сродства к электрону атома хлора равна 349 кДж/моль), атомы хлора частично сохраняют ее и в молекуле (молярная энергия сродства к электрону молекулы хлора равна 230 кДж/моль). Поэтому, растворяясь, молекулы хлора гидратируются, притягивая к себе атомы кислорода молекул воды. У некоторых из этих атомов кислорода атомы хлора могут акцептировать неподеленную пару электронов. Дальнейшее показано на схеме механизма:
Суммарное уравнение этой реакции
Cl2 + 2H2O = HClO + H3O 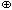
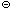
Но реакция обратима, поэтому устанавливается равновесие:
Cl2 + 2H2O 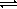
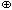
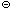
Cl2 + H2O 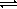
Аналогично с водой реагирует бром, только равновесие в этом случае сильно смещено влево. Йод же с водой практически не реагирует.
Чтобы представить себе, в какой степени хлор и бром физически растворяются в воде, а в какой – реагируют с ней, используем количественные характеристики растворимости и химического равновесия.
Мольная доля хлора в насыщенном при 20°С и атмосферном давлении водном растворе равна 0,0018, то есть на каждую 1000 молекул воды приходится примерно 2 молекулы хлора. Для сравнения, в насыщенном при тех же условиях растворе азота мольная доля азота равна 0,000012, то есть одна молекула азота приходится примерно на 100000 молекул воды. А для получения насыщенного при тех же условиях раствора хлороводорода на каждые 100 молекул воды нужно взять около 35 молекул хлороводорода. Отсюда можно сделать вывод, что хлор хоть и растворим в воде, но незначительно. Растворимость брома несколько больше – примерно 4 молекулы на 1000 молекул воды.
Константа равновесия обратимой химической реакции хлора с водой
Cl2 + 2H2O 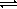


2.Изобразите схему, иллюстрирующую механизм взаимодействия с водой кальция.
3.Почему металлы IА группы бурно реагируют с водой, а медь, железо, хром или свинец практически не реагируют?
4.Составьте ионные и » молекулярные» уравнения реакций с водой оксидов натрия, стронция и бария. Для реакции с водой оксида лития приведите схему, иллюстрирующую ее механизм.
5.Приведите уравнения реакций, позволяющих осуществить следующие превращения:
а) Li Li2O
LiOH; б) Ca
CaO
Ca(OH)2.
6.Составьте уравнения реакций, по которым можно получить а) хромовую кислоту (H2CrO4) из оксида хрома(VI), б) йодноватую кислоту (HIO3) из оксида йода(V), в) селеновую кислоту (H2SeO4) из оксида селена (VI).
7.Приведите уравнения реакций, позволяющих осуществить следующие превращения:
а) S SO2
SO3
H2SO4 ;
б) P P4O10
H3PO4.
8.Что происходит при » растворении» в воде бромоводорода? Ответ проиллюстрируйте уравнениями реакций.
9.Запишите уравнение обратимой реакции брома с водой и составьте схемы механизмов прямой и обратной реакций.
При химическом растворении ионных веществ происходит гидратация переходящих в раствор ионов. Гидратируются как катионы, так и анионы. Как правило, гидратированные катионы прочнее, чем анионы, а гидратированные простые катионы — прочнее, чем сложные. Это связано с тем, что у простых катионов есть свободные валентные орбитали, которые могут частично акцептировать неподеленные электронные пары атомов кислорода, входящих в молекулы воды.
При попытке выделить исходное вещество из раствора, удаляя воду, получить его часто не удается. Например, если мы растворим в воде бесцветный сульфат меди CuSO4, то получим раствор голубого цвета, который придают ему гидратированные ионы меди:
После упаривания раствора (удаления воды) и охлаждения из него выделятся кристаллы синего цвета, имеющие состав CuSO4· 5H2O (точка между формулами сульфата меди и воды означает, что на каждую формульную единицу сульфата меди приходится указанное в формуле число молекул воды). Исходный сульфат меди можно получить из этого соединения, нагрев его до 250 ° С. При этом происходит реакция:
CuSO4· 5H2O = CuSO4 + 5H2O .
| Кристаллогидраты — вещества, включающие в себя обособленные частицы H2O, в которых атомы кислорода связаны с двумя атомами водорода ковалентными связями, а частицы Н2О в целом связаны с другими атомами либо химическими, либо межмолекулярными связями. |
При образовании кристаллогидратов из исходных веществ и воды в молекулах воды не происходит разрыва связей О—Н.
Если кристаллизационная вода удерживается в кристаллогидрате слабыми межмолекулярными связями, то она легко удаляется при нагревании:
Na2CO3· 10H2O = Na2CO3 + 10H2O (при 120 ° С);
K2SO3· 2H2O = K2SO3 + 2H2O (при 200 ° С);
CaCl2· 6H2O = CaCl2 + 6H2O (при 250 ° С).
Если же в кристаллогидрате связи между молекулами воды и другими частицами близки к химическим, то такой кристаллогидрат или дегидратируется (теряет воду) при более высокой температуре, например:
Al2(SO4)3· 18H2O = Al2(SO4)3 + 18H2O (при 420 ° С);
СoSO4· 7H2O = CoSO4 + 7H2O (при 410 ° С);
или при нагревании разлагается с образованием других химических веществ, например:
2
2
Таким образом, взаимодействие с водой безводных веществ, образующих кристаллогидраты, может быть как химическим растворением, так и химической реакцией.


2.Определите состав кристаллогидрата сульфата магния, если массовая доля воды в нем равна 51,2%. 3.Какова масса воды, выделившейся при прокаливании декагидрата сульфата натрия (Na2SO4· 10H2O) массой 644 г?
4.Сколько безводного хлорида кальция можно получить, прокаливая 329 г гексагидрата хлорида кальция?
5.Дигидрат сульфата кальция CaSO4· 2H2О при нагревании до 150° С теряет 3/4 своей воды. Составьте формулу образующегося кристаллогидрата (алебастра) и запишите уравнение превращения гипса в алебастр.
6.Определите массу медного купороса и воды, которые необходимо взять для приготовления 10 кг 5 %-го раствора сульфата меди.
7.Определите массовую долю сульфата железа(II) в растворе, полученном при смешении 100 г железного купороса (FeSO4· 7H2O) с 9900 г воды. 


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору