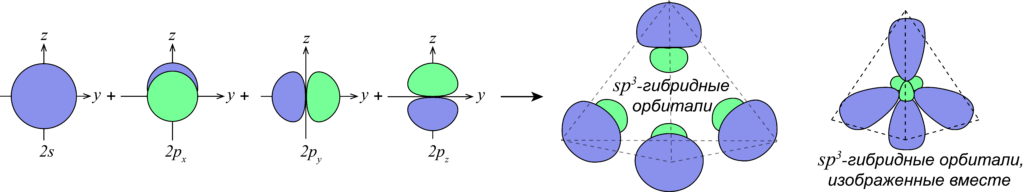
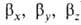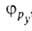Что такое гибридизация электронных орбиталей
Гибридизация электронных орбиталей и геометрия молекул
В 1930 г. Слейтером и Л. Полингом была развита теория образования ковалентной связи за счет перекрывания электронных орбиталей – метод валентных связей. В основе этого метода лежит метод гибридизации, который описывает образование молекул веществ за счет «смешивания» гибридных орбиталей («смешиваются» не электроны, а орбитали).
Определение типа гибридизации молекул с ковалентной связью
Определить тип гибридизации можно только для молекул с ковалентной связью типа АВn, где n больше или равно двум, А – центральный атом, В – лиганд. В гибридизацию вступают только валентные орбитали центрального атома.
Определим тип гибридизации на примере молекулы BeH2.
Первоначально записываем электронные конфигурации центрального атома и лиганда, рисуем электронно-графические формулы.
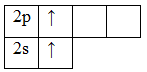
Атом бериллия (центральный атом) имеет вакантные 2p-орбитали, поэтому, чтобы принять по одному электрону от каждого атома водорода (лиганд) для образования молекулы BeH2 ему необходимо перейти в возбужденное состояние:
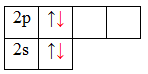
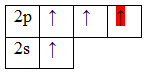
Образование молекулы BeH2 происходит за счет перекрывания валентных орбиталей атома Be
* красным цветом обозначены электроны водорода, черным – бериллия.
Тип гибридизации определяют по тому, какие орбитали перекрылись, т.о., молекула BeH2 находитс в sp – гибридизации.
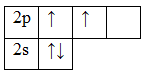
Помимо молекул состава ABn, методом валентных связей можно определить тип гибридизации молекул с кратными связями. Рассмотрим на примере молекулы этилена C2H4. В молекуле этилена кратная двойная связь, которая образована 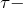
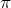
У атома углерода имеется еще одна вакантная p-орбиталь, следовательно, чтобы принять 4 атома водорода ему необходимо перейти в возбужденное состояние:
Определение геометрической структуры молекул
Геометрическую структуру молекул, а также катионов и анионов состава АВn можно с помощью метода Гиллеспи. В основе этого метода – валентные пары электронов. На геометрическую структуру оказывают влияние не только электроны, участвующие в образовании химической связи, но и неподеленные электронные пары. Каждую неподеленную пару электронов в методе Гиллеспи обозначают Е, центральный атом – А, лиганд – В.
Если неподеленных электронных пар нет, то состав молекул может быть АВ2 (линейная структура молекулы), АВ3 (структура плоского треугольника), АВ4 (тетраэдрическая структура), АВ5 (структура тригональной бипирамиды) и АВ6 (октаэдрическая структура). От базисных структур могут быть получены производные, если вместо лиганда появляется неподеленная электронная пара. Например: АВ3Е (пирамидальная структура), АВ2Е2 (угловая структура молекулы).
Чтобы определить геометрическую структуру (строение ) молекулы необходимо определить состав частицы, для чего вычисляют количество неподеленных лектронных пар (НЕП):
НЕП = (общее число валентных электронов – число электронов, пошедших на образование связи с лигандами) / 2
На связь с H, Cl, Br, I, F уходит по 1-му электрону от А, на связь с O – по 2 электрона, а на связь с N – по 3 электрона от центрального атома.
Рассмотрим на примере молекулы BCl3. Центральный атом – B.
НЕП = (3-3)/2 = 0, следовательно неподеленных электронных пар нет и молекула имеет структуру АВ3 – плоский треугольник.
Подробно геометрическое строение молекул разного состава представлено в табл. 1.
Таблица 1. Пространственное строение молекул
Гибридизация орбиталей
Вы будете перенаправлены на Автор24
Наибольшее количество соединений в органической химии обладает молекулярным строением. Атомы с данным типом строения составляют исключительно ковалентные связи.
Типы ковалентных связей
Ковалентной называется тип связи, который возникает между атомами за счет обобществления ими части своих внешних электронов.
Ковалентные связи в соответствии с числом обобществленных электронных пар делят на:
Орбитали могут быть двух форм:
Связи способны отличаться в зависимости от типа перекрытия орбиталей.
Строгий квантово-механический расчет валентных связей не представляется возможным, поскольку уравнение Шредингера на сегодняшний день не получило точного решения для какой-либо сложной молекулы. Некоторые попытки приближенного решения этого уравнения приводят к неплохим и понятным результатам.
Для характеристики химической связи при помощи уравнения Шредингера сделаем следующие допущения:
Готовые работы на аналогичную тему
Гипотеза гибридизации
Гибридизация орбиталей – это гипотетический процесс, в нем орбитали, которые первоначально обладали различными формами и энергиями соединяются.
Гипотеза о гибридизации считает, что из нескольких атомных орбиталей с различными энергиями и различной симметрией образуется такое же количество гибридных орбиталей с одинаковой энергией и одинаковой симметрией.
Гибридизация считается возможной только при образовании химических связей. Гибридизируются, в основном, атомные орбитали, имеющие частичное заполнение (имеющие по одному электрону). Так, если, например, рассматривается атом углерода, то гибридизации атомных орбиталей предшествует возбуждение.
Гипотезу о гибридизации с успехом используют для нескольких атомов, например:
Теорию гибридизации предложил Л. Полинг. Данная теория стала центральной в методе валентных связей.
Гибридизация – это не реальный процесс в физике, а модель, при помощи которой объясняют структуру молекулы, причину изменения вида атомных орбиталей при создании ковалентных химических связей.
Данную гипотезу первоначально использовали для рассмотрения простых молекул, несколько позднее ее применение расширили, усложнив молекулы.
Заметим, что существуют другие, более сложные квантово-механические приемы с помощью которых строят молекулярные орбиталь из негибридизированных атомных орбиталей, при этом получают такие же результаты.
Теория гибридизации легла в основу теории отталкивания электронных пар Гиллеси – Найхолма. В соответствии с которой, каждому типу гибридизации отвечает своя ориентация в пространстве гибридных орбиталей центрального атома.
3.2. Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа.
Большинство органических соединений имеют молекулярное строение. Атомы в веществах с молекулярным типом строения всегда образуют только ковалентные связи друг с другом, что наблюдается и в случае органических соединений. Напомним, что ковалентным называется такой вид связи между атомами, который реализуется за счет того, что атомы обобществляют часть своих внешних электронов с целью приобретения электронной конфигурации благородного газа.
По количеству обобществлённых электронных пар ковалентные связи в органических веществах можно разделить на одинарные, двойные и тройные. Обозначаются данные типы связей в графической формуле соответственно одной, двумя или тремя чертами:
Кратность связи приводит к уменьшении ее длины, так одинарная С-С связь имеет длину 0,154 нм, двойная С=С связь – 0,134 нм, тройная С≡С связь – 0,120 нм.
Типы связей по способу перекрывания орбиталей
Как известно, орбитали могут иметь различную форму, так, например, s-орбитали имеют сферическую, а p-гантелеобразную форму. По этой причине связи также могут отличаться по способу перекрывания электронных орбиталей:
• ϭ-связи – образуются при перекрывании орбиталей таким образом, что область их перекрывания пересекается линией, соединяющей ядра. Примеры ϭ-связей:
• π-связи – образуются при перекрывании орбиталей, в двух областях – над и под линией соединяющей ядра атомов. Примеры π-связей:
Как узнать, когда в молекуле есть π- и ϭ-связи?
При ковалентном типе связи ϭ-связь между любыми двумя атомами есть всегда, а π-связь имеет только в случае кратных (двойных, тройных) связей. При этом:
Укажем данные типы связей в молекуле бутин-3-овой кислоты:
Гибридизация орбиталей атома углерода
Гибридизацией орбиталей называют процесс, при котором орбитали, изначально имеющие разные формы и энергии смешиваются, образуя взамен такое же количество гибридных орбиталей, равных по форме и энергии.
В случае атомов углерода в гибридизации всегда принимает участие s-орбиталь, а количество p-орбиталей, которые могут принимать участие в гибридизации варьируется от одной до трех p-орбиталей.
Как определить тип гибридизации атома углерода в органической молекуле?
| Количество атомов, с которыми связан атом углерода | Тип гибридизации атома углерода | Примеры веществ |
| 4 атома | sp 3 | CH4 – метан |
| 3 атома | sp 2 | H2C=CH2 – этилен |
| 2 атома | sp | HC≡CH — ацетилен |
Потренируемся определять тип гибридизации атомов углерода на примере следующей органической молекулы:
Радикал. Функциональная группа
Под термином радикал, чаще всего подразумевают углеводородный радикал, являющийся остатком молекулы какого-либо углеводорода без одного атома водорода.
Название углеводородного радикала формируется, исходя из названия соответствующего ему углеводорода заменой суффикса –ан на суффикс –ил.
| Формула углеводорода | Название углеводорода | Формула радикала | Название радикала |
| CH4 | метан | -CH3 | метил |
| C2H6 | этан | -С2Н5 | этил |
| C3H8 | пропан | -С3Н7 | пропил |
| СnН2n+2 | …ан | -СnН2n+1 | … ил |
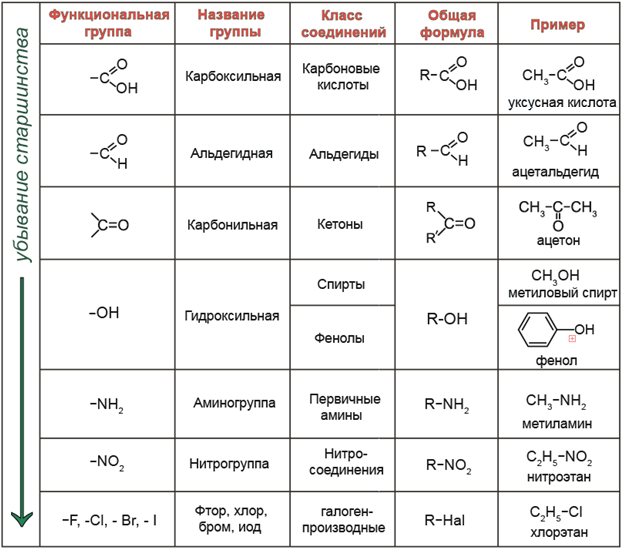
Функциональная группа — структурный фрагмент органической молекулы (некоторая группа атомов), который отвечает за её конкретные химические свойства.
В зависимости того, какая из функциональных групп в молекуле вещества является старшей, соединение относят к тому или иному классу.
R – обозначение углеводородного заместителя (радикала).
Радикалы могут содержать кратные связи, которые тоже можно рассматривать как функциональные группы, поскольку кратные связи вносят вклад в химические свойства вещества.
Если в молекуле органического вещества содержится две или более функциональных группы, такие соединения называют полифункциональными.
Орбитальная гибридизация
Гибридизация описывает связывание атомов с точки зрения атома. Для углерода с тетраэдрической координацией (например, метана CH 4 ) углерод должен иметь 4 орбитали с правильной симметрией для связи с 4 атомами водорода.
Конфигурация основного состояния углерода 1s 2 2s 2 2p 2 или более легко читается:
| C | ↑ ↓ | ↑ ↓ | ↑ | ↑ |
| 1 с | 2 с | 2p | 2p | 2p |
| C * | ↑ ↓ | ↑ | ↑ | ↑ | ↑ |
| 1 с | 2 с | 2p | 2p | 2p |
Энергия, высвобождаемая при образовании двух дополнительных связей, более чем компенсирует требуемую энергию возбуждения, энергетически благоприятствуя образованию четырех связей CH.
| C * | ↑ ↓ | ↑ | ↑ | ↑ | ↑ |
| 1 с | sp 3 | sp 3 | sp 3 | sp 3 |
В CH 4 четыре гибридных sp 3 орбитали перекрываются водородными 1s орбиталями, образуя четыре σ (сигма) связи (то есть четыре одинарные ковалентные связи) одинаковой длины и силы.

Аналогичным образом можно объяснить другие углеродные соединения и другие молекулы. Например, этен (C 2 H 4 ) имеет двойную связь между атомами углерода.
| C * | ↑ ↓ | ↑ | ↑ | ↑ | ↑ |
| 1 с | sp 2 | sp 2 | sp 2 | 2p |
| C * | ↑ ↓ | ↑ | ↑ | ↑ | ↑ |
| 1 с | зр | зр | 2p | 2p |
что дает две sp-орбитали и две оставшиеся p-орбитали. Химическая связь в ацетилене (этине) (C 2 H 2 ) состоит из sp-sp-перекрытия между двумя атомами углерода, образующего σ-связь, и двух дополнительных π-связей, образованных p-p-перекрытием. Каждый углерод также связывается с водородом в виде перекрытия σ s – sp под углом 180 °.
sp x гибридизация
sp x d y гибридизация
sd x гибридизация
В некоторых комплексах переходных металлов с низким числом d-электронов p-орбитали не заняты, и sd x- гибридизация используется для моделирования формы этих молекул. [11] [13] [12]
Расширение октета
В некоторых учебниках по общей химии гибридизация представлена для координационного числа основной группы 5 и выше с использованием схемы «расширенных октетов» с d-орбиталями, впервые предложенной Полингом. Однако в настоящее время такая схема считается некорректной в свете расчетов вычислительной химии.
| Координационный номер | Форма | Гибридизация | Примеры |
|---|---|---|---|
| 5 | Тригональный бипирамидный | sp 3 d гибридизация | PF 5 |
| 6 | Восьмигранный | sp 3 d 2 гибридизация | SF 6 |
| 7 | Пентагональный бипирамидальный | sp 3 d 3 гибридизация | ЕСЛИ 7 |
В 1990 году Эрик Альфред Магнуссон из Университета Нового Южного Уэльса опубликовал статью, окончательно исключающую роль d-орбитальной гибридизации в связывании в гипервалентных соединениях элементов второго ряда ( период 3 ), что положило конец спору и путанице. Отчасти путаница происходит из-за того, что d-функции важны в базисных наборах, используемых для описания этих соединений (в противном случае возникают неоправданно высокие энергии и искаженная геометрия). Кроме того, вклад d-функции в волновую функцию молекулы велик. Эти факты были неправильно интерпретированы как означающие, что d-орбитали должны участвовать в связывании. [14] [15]
Резонанс
| Координационный номер | Резонансные структуры |
|---|---|
| 5 | Тригональный бипирамидный |
 | |
| 6 | Восьмигранный |
 | |
| 7 | Пентагональный бипирамидальный |
 |
Гибридизация связанных орбиталей определяется правилом Бента : «Атомный характер концентрируется на орбиталях, направленных к электроположительным заместителям».
Молекулы с неподеленными парами
Для молекул с неподеленными парами связывающие орбитали представляют собой изовалентные sp x гибриды. Например, две образующие связь гибридные орбитали кислорода в воде могут быть описаны как sp 4,0, что дает межглазничный угол 104,5 °. [17] Это означает, что они имеют характер 20% s и характер 80% p и не подразумевают, что гибридная орбиталь образована из одной s и четырех p-орбиталей на кислороде, поскольку подоболочка кислорода 2p содержит только три p-орбитали. Формы молекул с неподеленными парами следующие:
В таких случаях есть два математически эквивалентных способа представления одиночных пар. Они могут быть представлены орбиталями сигма- и пи-симметрии, подобными теории молекулярных орбиталей, или эквивалентными орбиталями, подобными теории VSEPR.
Гипервалентные молекулы
| Количество гибридов с изовалентной связью (отмечено красным) | ||||
|---|---|---|---|---|
| Два | Один | — | ||
| Гипервалентный компонент [16] | Линейная ось (одна р-орбиталь) | Качели | Т-образный | Линейный |
 |  |  | ||
| Квадратный плоский экватор (две р-орбитали) | Квадрат пирамидальный | Квадратный планарный | ||
 |  | |||
| Пентагональный плоский экватор (две р-орбитали) | Пятиугольная пирамидальная | Пятиугольный плоский | ||
 |  | |||
Связующие орбитали, образованные из гибридных атомных орбиталей, можно рассматривать как локализованные молекулярные орбитали, которые могут быть образованы из делокализованных орбиталей теории молекулярных орбиталей путем соответствующего математического преобразования. Для молекул в основном состоянии это преобразование орбиталей оставляет неизменной полную многоэлектронную волновую функцию. Гибридное орбитальное описание основного состояния, следовательно, эквивалентно делокализованному орбитальному описанию для полной энергии основного состояния и плотности электронов, а также геометрии молекулы, которая соответствует минимальному значению полной энергии.
Два локализованных представления
Молекулы с множественными связями или множественными неподеленными парами могут иметь орбитали, представленные в терминах сигма- и пи-симметрии или эквивалентных орбиталей. Различные методы валентных связей используют одно из двух представлений, которые имеют математически эквивалентные полные многоэлектронные волновые функции и связаны унитарным преобразованием набора занятых молекулярных орбиталей.
ГИБРИДИЗАЦИЯ АТОМНЫХ ОРБИТАЛЕЙ
квантовохим. способ описания перестройки орбиталей атома в молекуле по сравнению со своб. атомом. Являясь формальным мат. приемом, Г. а. о. позволяет отразить нарушение сферич. симметрии распределения электронной плотности атома при образовании хим. связи. Сущность Г. а. о. состоит в том, что электрон молекулы вблизи выделенного атомного ядра характеризуется не отдельной атомной орбиталью (АО), а линейной комбинацией атомных орбита-лей с разл. значениями азимутального и магнитного квантовых чисел. Такая линейная комбинация наз. гибридной (гибридизированной) орбиталью (ГО). Как правило, гибридизация затрагивает лишь высшие и близкие по энергии занятые АО своб. атома. Напр., для атомов элементов второго периода периодич. системы типичная форма ГО 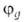
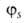
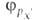
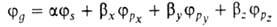
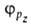
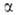
Полезное
Смотреть что такое «ГИБРИДИЗАЦИЯ АТОМНЫХ ОРБИТАЛЕЙ» в других словарях:
ГИБРИДИЗАЦИЯ АТОМНЫХ ОРБИТАЛЕЙ — способ описания перестройки орбиталей атома при переходе от свободного атома к молекуле. В молекуле электрон характеризуется не отдельной атомной орбиталью, а их линейной комбинацией. sр3 Гибридные орбитали (получены из одной s орбитали и трёх р… … Естествознание. Энциклопедический словарь
Гибридизация (химия) — У этого термина существуют и другие значения, см. Гибридизация. Модель молекулы метана, образованной sp3 гибридными орбиталями … Википедия
Гибридизация — Гибридизация: Гибридизация (биология) скрещивание разнородных организмов, получение гибридов. Гибридизация (химия) специфическое взаимодействие атомных орбиталей в молекулах. Гибридизация ДНК полное или частичное комплементарное спаривание двух… … Википедия
МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ МЕТОДЫ — приближенные квантовохим. методы расчета волновых ф ций, энерге тич. уровней и св в молекул. Основаны на том, что для каждого из электронных состояний молекулы как многоэлектронной системы полная волновая ф ция составляется из произведений… … Химическая энциклопедия
Sp² связь — Гибридизация орбиталей концепция смешения разных, но близких по энергии орбиталей данного атома, с возникновением того же числа новых гибридных орбиталей, одинаковых по энергии и форме. Гибридизация атомных орбиталей происходит при возникновении … Википедия
Теория валентных связей — Рис.1. Модель перекрывания атомных орбиталей при образовании сигма связи Теория валентных связей ( … Википедия
МАГНЕТИЗМ — 1) особая форма вз ствия между электрич. токами, между токами и магнитами (т. е. телами с магнитным моментом) и между магнитами; 2) раздел физики, изучающий это взаимодействие и св ва в в (магнетиков), в к рых оно проявляется. Основные проявления … Физическая энциклопедия
МОЛЕКУЛА — (новолат. molecule, уменьшит. от лат. moles масса), наименьшая ч ца в ва, обладающая его осн. хим. св вами и состоящая из атомов, соединённых между собой химическими связями. Число атомов в М. составляет от двух (Н2, О2, HF, KCl) до сотен и тысяч … Физическая энциклопедия
ВАЛЕНТНЫХ СВЯЗЕЙ МЕТОД — (метод валентных схем), метод приближенного решения электронного ур ния Шрёдингера для многоэлектронных молекулярных систем. Основан на представлениях о двухцентровых хим. связях между атомами в молекуле, образуемых двумя электронами. Эти… … Химическая энциклопедия
Хронология химии — Хронология науки химии это список различных работ, исследований, идей, изобретений и экспериментов, которые в значительной мере изменили взгляды человечества на строение вещества и материи и процессы происходящие с ними, которые в данный… … Википедия