Что такое допинг контроль своими словами
Допинг-контроль
Допинг-контроль — проверка, направленная на выявление факта применения спортсменом допинга (запрещенных лекарственных средств) во время тренировок или соревнований.
Допинг-контроль проводят медицинские службы. На территории РФ, функции допинг-контроля осуществляет Независимая Национальная антидопинговая организация РУСАДА.
Ссылки
Полезное
Смотреть что такое «Допинг-контроль» в других словарях:
допинг-контроль — Планирование, реализация и управление процессом допинг контроля, включающим распределение допинг тестов, сбор и обработку проб, проведение лабораторного анализа, обработку результатов, разбирательство судебных дел и апелляций. ОКОИ может учредить … Справочник технического переводчика
допинг-контроль — допинг контроль, допинг контроля … Орфографический словарь-справочник
допинг-контроль — сущ., кол во синонимов: 1 • допингконтроль (2) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Допинг-контроль — 5. Допинг контроль представляет собой процесс, включающий в себя планирование проведения тестов, взятие проб, их хранение, транспортировку, лабораторный анализ проб, послетестовые процедуры, а также проведение соответствующих слушаний и… … Официальная терминология
допинг-контроль — м. Экспресс анализ крови спортсмена на наличие допинга непосредственно после выступления в соревнованиях. Толковый словарь Ефремовой. Т. Ф. Ефремова. 2000 … Современный толковый словарь русского языка Ефремовой
допинг-контроль — д опинг контр оль, я … Русский орфографический словарь
допинг-контроль — до/пинг контро/ль, до/пинг контро/ля … Слитно. Раздельно. Через дефис.
допинг-контроль — <<допинг контр<>о<>ль>> я; м. Спорт. Медицинское обследование перед соревнованием с целью контроля за соблюдением запрета на использование допинговых средств … Энциклопедический словарь
допинг-контроль — я; м.; спорт. Медицинское обследование перед соревнованием с целью контроля за соблюдением запрета на использование допинговых средств … Словарь многих выражений
допинг-контроль в соревновательный период — Тестирование, при котором спортсмен выбирается для проведения допинг теста в связи с его участием в конкретном состязании (если правила, установленные Международной спортивной федерацией или соответствующей антидопинговой организацией не… … Справочник технического переводчика
Допинг-контроль — как это происходит?
В мире делается много антидопинговых проб, как во время турниров и соревнований, так и между ними. Рассмотрим, что такое допинг в спорте.
Что такое допинг-контроль?
Допинг-контроль — это процесс, который включает в себя взятие проб, проведение анализов, различные послетестовые процедуры, рассмотрение апелляций и проведение слушаний.
Как идёт процесс обсуждения и признания какого-либо вещества допингом?
Как правило, запрещенные вещества не сразу признаются допингом. В течение определенного срока квалифицированные специалисты отслеживают такие субстанции. Но бывают случаи, когда вещество сразу же признают допингом.
Специалисты центра ведут мониторинг субстанций в специальных лабораториях. Для исследований применяется специальное оборудование. Срок ведения мониторинга определяется ведущим специалистом центра.
После завершения мониторинга все полученные данные отправляют в комитет WADA (антидопинговое агентство). Данная организация проводит:
Процедурные правила допинг-контроля
Все спортсмены, которым присвоена высшая квалификация обязательно проходят специальный допинг-контроль. Для этого берётся образец мочи. В спортивных лабораториях проходит проверка.
Далее оглашаются полученные результаты. При обнаружении каких-либо запрещенных веществ спортсмен безоговорочно дисквалифицируется.
Перед проведением процедуры, спортсмена высшей квалификации должны проинформировать. Ему должны сообщить дату и точное время, а также другие нюансы.
После этого, сотрудник преподносит спортсмену так называемый бланк подтверждения. После ознакомления с бланком, спортсмен высшей категории должен поставить свою подпись. Теперь, бланк подтверждения действует так сказать юридически.
Как правило, спортсмену высшей квалификации необходимо прибыть в специальный пункт в течение одного часа. Если он не успеет прибыть в назначенное время, то процедура проводиться не будет. Кроме этого, в таком случае будет считаться, что данный спортсмен высшей квалификации употребляет какие-либо запрещенные субстанции.
В таком случае применяются определенные санкции:
Соответствующие санкции применяться в 99% случаев. Всегда возможны какие-либо исключения.
1. До прибытия в пункт спортсмена высшей квалификации обязательно должен кто-то сопровождать. Это может быть сотрудник лаборатории или судья. Ответственное лицо контролирует передвижение спортсмена. Согласно действующим нормам, он не может мочиться до проведения соответствующей процедуры.
2. По прибытии в соответствующий пункт, лицо, у которого будет взята проба, обязано предоставить какой-либо документ:
3. Для проведения специальных исследований необходимо определенное количество мочи — 75 миллилитров. Поэтому обязательно должны предоставить какие-либо напитки:
4. После этого ему предлагают пройти в комнату, в которой проходит взятие пробы. Спортсмена обязательно должно сопровождать административное лицо (судья). При проведении процедуры взятия образца, необходимо руководствоваться правилом — обнажить тело до определенного уровня.
5. Согласно действующим рекомендациям разрешается проводить стимуляцию мочеотделения. Существует два официальных способа:
6. После проведения соответствующей процедуры, административное лицо проводит разделение на 2 части:
7. После этого административное лицо (судья) должно убедиться в пригодности взятой пробы для проведения соответствующих исследований в лаборатории. Потом емкость закрывают крышкой. После этого административное лицо (судья) должно поставить уникальный код, а также опломбировать флакон.
8. Далее специальные флаконы ещё раз тщательно проверяют. Но теперь на протекание. Административное лицо должно удостовериться в герметичности и надежности флакона.
9. Теперь проверить флакон необходимо спортсмену высшей квалификации:
10. И последний этап. Сотрудники кладут флаконы в защищенный контейнер. После этого контейнер обязательно пломбируют. Теперь в сопровождении охраны, защищенные контейнеры транспортируют в лабораторию для проведения исследований.
Кто производит забор допинг-проб?
Согласно действующему законодательную определяют 2 вида контроля:
Задолго до поступления на работу, все «офицеры» проходят тщательный отбор:
Данные «офицеры» представляют такие организации:
Пример, корпорация IDTM. Данная корпорация проводит контроль спортсменов, которые занимаются легкой атлетикой.
Пробы чего берутся на допинг-контроль?
Согласно действующему законодательству, на специальный допинг-контроль берётся образец мочи. Исследование других материалов не проводиться.
Может ли спортсмен отказаться?
Действующие правила запрещают отказываться от прохождения данной процедуры. В противном случае участник соревнований будет безоговорочно дисквалифицирован. То есть комиссия задокументирует принятие положительной пробы.
Иногда можно взять паузу. Например, это может быть молодая мама, которой нужно покормить своего ребенка. Но даже в таком случае необходимо грамотно обосновать причину, для того чтобы комиссия предложила взять паузу.
Как происходит сдача пробы?
Как правило, образец сдают в специальном пункте. Участник соревнований может передвигаться по пункту только в присутствии административного лица.
Недобросовестные спортсмены для подмены флакона могут пользоваться различными хитростями и уловками:
Как быстро делается анализ?
Сроки выполнения анализа зависят от масштабности соревнований:
Как долго хранятся пробы и где?
На сегодняшний день срок хранения образцов значительно изменился. Некоторые из них хранят до 8 лет. Длительное хранение необходимо для проведения повторных анализов. Для чего это нужно?
Таким образом анализ полученных результатов проводиться спустя несколько лет. Полученные результаты оглашаются. Некоторые участники прошедших соревнований получают неутешительные результаты.
Взятые пробы хранятся в специальных лабораториях, которые тщательно охраняться от недобросовестных лиц.
Антидопинговый паспорт
С юридической точки зрения полученные результаты на допинг-контроле ничем не отличаются от показателей в антидопинговом паспорте.
Анализ показателей антидопингового паспорта осуществляется очень просто:
После проведения исследования проводиться обсуждение результатов. Как правило, учитывается мнение 3 сотрудников лаборатории. Однако полученные результаты не являются прямым доказательством.
Что такое антидопинговый паспорт
Антидопинговым паспортом называют электронную запись участника соревнований, которая содержит различную информацию. Это так называемые биологические маркеры, которые сопоставляются с полученными результатами допинг-контроля. При проведении анализа проб сотрудники лаборатории используют данную информацию.
На сегодняшний день для проведения анализа широко используются данные только гематологического паспорта.
Зачем нужен антидопинговый паспорт
Данный гормон непосредственно влияет на выносливость человека. Также переливание крови воздействует на изменение некоторых параметров крови выносливость. Поэтому эти данные очень важны при проведении анализа.
При проведении исследований учитываются эти показатели крови.
Как он показывает прием допинга?
Каждый участник крупных соревнований и турниров обязательно сдает кровь в специальном пункте:
Далее на специальном оборудовании проводиться анализ крови. Программа автоматически вносит полученные данные. А после этого анализирует показатели крови.
Кроме этого, программа определяет нормы показателей крови для каждого участника соревнований. То есть делает «коридоры» с верхней и нижней границей. Все это позволяет определить использование запрещенных веществ.
Перепроверка пробы
Перепроверка пробы дает возможность обнаружить запрещенные вещества. Если такие субстанции будут обнаружены, то спортсмен понесет заслуженное наказание. Перепроверка пробы может проводиться через много лет.
На каком основании перепроверяются пробы?
Существует организация, которая принимает решение о проведении перепроверки пробы. И имя ей — WADA. Также принимать решение о проведении перепроверки может международная федерация.
Перепроверка пробы осуществляется при разработке нового метода обнаружения каких-либо запрещенных веществ. При разработке такого метода, специализированная лаборатория предлагает международной федерации и WADA провести перепроверку пробы. А уже эти организации принимают окончательно решение.
Сколько раз можно перепроверять пробы?
Законно можно перепроверять пробы много раз. Однако никто не отменял законы физики. Для проведения каждого анализа используется определенное количество мочи. Поэтому в среднем можно провести две перепроверки.
Когда начали проверять спортсменов на использование запрещенных препаратов?
Впервые проверять спортсменов начали в 1968 году. Но сами пробы были взяты в 1963 году. Делать такие анализы стало возможным благодаря развитию технологий. Для анализа проб использовалось специальное оборудование.
Основными методами анализа были:
Запрещенный список
Классы запрещенных веществ:
В 2014 году список немного изменили. Были добавлены аргон и ингаляция ксенона.
Санкции за нарушения антидопинговых правил
Санкции могут быть в отношении как лабораторий, так и спортсменов. Если лаборатория допустила какое-либо нарушение, то она может лишиться аккредитации. Даже при совершении нарушения специализированная лаборатория имеет право защищаться. Таким образом проходят судебные разбирательства и рассматриваются все обстоятельства дела.
Все участники соревнований, административные лица, технический персонал должны соблюдать правила так называемого антидопингового Кодекса. Впервые он был опубликован в 2003 году.
Организаторы соревнований самостоятельно устанавливают санкции. Каждый случай нарушения рассматривается индивидуально. Если персонал или тренер способствовал нарушению, то они понесут более строгое наказание, нежели сам спортсмен.
Какие санкции могут применяться в отношении спортсмена?
В большом спорте допинг является запрещенной темой. Спортсмены, которые посвятили всю жизнь спорту не хотят быть дисквалифицированы. Поэтому вынуждены отказываться от применения запрещенных веществ.
«Никто не отворачивается, в помещении зеркала, тебя видно с любого ракурса». Как устроен допинг-контроль и можно ли его обмануть?
Допинг-тестирование – сложный процесс, от которого зависят не только результаты отдельных атлетов, но и судьба команд, имидж индустрии.
С каждым годом процедура забора проб усложняется, но все еще остается неидеальной и довольно унизительной для спортсменов – и их это закономерно раздражает.
Как обманывали: накладной пенис, мыло и морковка
Если контроль появился сразу вслед за изобретением допинга, то методы обмана совершенствовались одновременно с развитием контроля.
В 1980-х спортсменам было нетрудно обмануть анализ мочи. Самый распространенный прием – обильное питье: запрещенные вещества таким образом вымывались из организма, а не очень чувствительный тест не определял малые дозы. Обесцвеченная от диуретиков моча все равно вызывала подозрения у инспекторов, и в конце концов WADA запретило препараты-маскировщики (которые сами по себе не являются допингом). На помощь читерам приходила морковка и другие овощи с высоким содержанием каротина – моча приобретала естественный цвет.
Стероиды прятали иначе – они не растворяются в воде и откладываются в жировых тканях: чтобы скрыть следы их употребления, приходилось интенсивно худеть.
Допинг-империя ГДР расцвела на Олимпиаде-80: чемпионам давали стероиды с 12 лет (даже принудительно) – спустя годы они мучились со здоровьем
Когда тесты усовершенствовались и простое разбавление уже не действовало, спортсмены меняли образцы. Здесь изощренность доходила до дикости: женщины помещали в себя презервативы или специальные колбы, наполненные чужой мочой, мужчины вводили в мочевой пузырь чистые образцы через катетер.
Какое-то время популярностью пользовался накладной пенис. Такие и сейчас в свободной продаже – стоят в районе 160 долларов (по скидке – 130), в описании говорится, что пенис идеально подходит для имитации болезни или пранков. Отдельно оговаривается, что накладной орган не предназначается для нарушения закона. В наборе идет синтетическая моча и даже грелка для поддержания температуры.
В разное время искусственным пенисом пользовались звезда НБА Ламар Одом и легенда бокса Майк Тайсон – оба скрывали наличие наркотиков в организме.
Метод был востребован до последних лет: в 2013-м накладной пенис на допинг-контроле использовал итальянский бегун Дэвис Личчарди.
Помимо подмены мочи существовал и другой вариант обмана: некоторые жулики использовали обычное мыло, чтобы скрыть наличие в организме ЭПО. В мыле содержится фермент, расщепляющий эритропоэтин. Спортсмены перед сдачей проб натирали руки мылом, а затем мочились на пальцы. Когда атлетов заставляли мыть руки перед процедурой, особо отчаянные прятали мыло под крайней плотью.
Анализ крови обмануть куда сложнее, но переливание дает эффект маскировки, поэтому WADA его и запретило. Логично, что появление тестов крови и биологических паспортов породило новые виды обхода правил: уменьшение доз применения препарата, так называемое микродозирование, способствует быстрой очистке организма от допинга, а методы контроля генного допинга вообще в зачаточном состоянии.
Как проходит процедура забора?
Сейчас допинг-контроль – жестко регламентированная процедура, ее этапы могут изучить не только спортсмены и специалисты, но и все желающие. Описание процесса есть на сайтах антидопинговых агентств. Сдача мочи проходит в 10 этапов – от уведомления спортсмена до подписания протокола. Главные нюансы:
• Офицер подробно описывает процесс спортсмену, а с момента уведомления постоянно следит за ним и его действиями. При этом спортсмен может позвать представителя (обычно это касается несовершеннолетних атлетов и паралимпийцев) или переводчика.
• Еще одна опция – запрос отсрочки. Но и тут все строго – причина должна быть уважительной: выполнение обязательств перед СМИ, участие в церемонии награждения или продолжающемся соревновании, получение медицинской помощи или выполнение заминки.
• На пункте допинг-контроля спортсмены могут есть и пить, но сами несут за это ответственность. Если проба будет недостаточно плотной из-за избытка жидкости, то офицер потребует повтора процедуры.
• Атлет выбирает одну из трех емкостей, сам проверяет пломбы на пробирках и оставляет их у себя до того момента, пока их не запечатают.
• Далее происходит сам процесс сдачи. Инспектор допинг-контроля сопровождает спортсмена в кабинку туалета (важно, чтобы специалист был одного пола с атлетом), а затем наблюдает за сдачей пробы: «Спортсмен должен обеспечить ясный, беспрепятственный обзор процесса предоставления пробы».
• После получения образца пробу разливают по пробиркам А и Б, проверяют на плотность (если потребуется, процедуру повторяют) и заполняют протокол.
Во время сдачи крови основные пункты процесса те же самые. Но потребуется медицинский персонал, а также объяснение ограничений после процедуры – например, какое-то время нельзя перегружать руку, из которой взяли кровь.
А что говорят спортсмены?
Они прекрасно знают об истории допинг-контроля и о методах обмана. Двукратная олимпийская чемпионка по синхронному плаванию Алла Шишкина, активно развивающая инстаграм, знакомила подписчиков со способами мошенничества:
«В штаб-квартире WADA даже есть музей всех предметов, которые отобрали у спортсменов при попытке обхода бдительного взгляда допинг-офицера. Я смогла найти фото некоторых в интернете, но по рассказам знаю, что были и более хитроумные приборы: искусственные руки, где в пальце помещался резервуар для чистой мочи, различные колбы, которые женщины помещали прямо в своем теле и т.д. Не говоря уже о том, что в лабораторию отправлялась подкрашенная вода, сок и холодный чай».
А победительница Сочи-2014 в парном катании Татьяна Волосожар рассказывала о минусах процедуры. Проблемы возникают из-за стеснения и недостаточного количества анализа (нужно – минимум 90 мл).
«Тест на допинг – самая неприятная процедура. И довольно унизительная, если говорить честно. Вместе с офицером допинг-контроля ты идешь в туалет. Там тебе дают специальную баночку, в которую ты должен, извините, справить малую нужду, причем прямо на глазах у контролера. Никто никуда не отворачивается, более того, в помещении могут быть установлены зеркала, чтобы тебя было отлично видно с любого ракурса, так исключается вероятность даже попыток подмены допинг-пробы.
При этом объем анализа довольно большой, не всегда получается сдать его с первого раза, и может пройти несколько часов, прежде чем ты в несколько подходов, скажем так, наконец-то сдашь этот несчастный тест».
Грандиозный допинг-бан в фигурке: Марии Сотсковой дали 10 лет за подделку документов. Она катала на Олимпиаде с Медведевой и Загитовой
Вопрос этичности допинг-тестирования поднимается часто, но все же чаще обсуждают этичность использования допинга. А вот уместность забора анализа во время соревнований – отдельная тема. В конце августа чемпион мира в барьерном спринте Сергей Шубенков разнес РУСАДА за не вовремя появившегося допинг-офицера.
На Кубке России по легкой атлетике в Брянске тот пришел к бегуну после предварительных забегов. Шубенков попросил отсрочку, на что имел полное право, но не предусмотрел одного – спортсмен не может идти в туалет, если допинг-офицер еще не взял пробу. Отсрочка тут уже не действует.
«Инспектор находится со мной рядом, но перед финальной разминкой мне захотелось в туалет, а меня туда не пускают, если хочешь, то сходи в баночку. И мне начинают рассказывать, как мне надо делать свою работу. На все это я начинаю заводиться, меня это все очень бесит, мне кажется, что инспекторы даже получают какое-то удовольствие от всего процесса. В конце концов я был вынужден согласиться на процедуру контроля, сократив драгоценное время на подготовку».
Шубенков заметил, что допинг-офицеры, несмотря на соблюдение регламента, не понимают особенностей спорта, с которым имеют дело. Но это и не входит в обязанности специалистов, а вот спортсмены должны следовать правилам и не использовать допинг.
Несмотря на развитие допинг-контроля, его до сих пор обходят: объясняют подозрительные пробы поцелуями и сексом или сверлят дырку в стене лаборатории. Вряд ли допинг когда-нибудь исчезнет из спорта, так что вся надежда – на еще более строгий контроль.
Допинг-контроль: методы и тесты
Содержание
Исторические аспекты анализа низкомолекулярных веществ в допинг-контроле [ править | править код ]
Классификация стимулирующих препаратов [ править | править код ]
Запрещенные субстанции [ править | править код ]
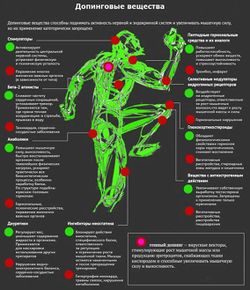
Классификация запрещенных субстанций и методов воздействия, предложенная Международным олимпийским комитетом (МОК) и Всемирным антидопинговым агентством (ВАДА)
Одним из спорных веществ, запрещенных WADA является ноотропный препарат фенотропил.
Класс наркотических веществ включает такие субстанции, как опиоидные анальгетики морфинового типа и близкие по структуре вещества, за несколькими исключениями, в частности этилморфина и кодеина, сделанными из-за их незначительного анальгетического воздействия. Использование других лекарственных препаратов не опиоидного типа, например ацетилсалициловой кислоты или диклофенака, разрешено.
Применение стимуляторов и наркотиков представляет интерес преимущественно во время соревнований, тогда как анаболические препараты являются эффективным средством воздействия в период проведения тренировочных занятий. Вещества, стимулирующие рост мышечной ткани и увеличение силовых показателей, были внесены в список запрещенных субстанций МОК в 1976 г., а после 1993 г. в класс анаболических препаратов были включены не только стероиды — производные тестостерона, но и β2-агонисты, поскольку они также вызывают анаболический эффект при использовании в дозах, существенно превышающих терапевтические (Reedset al., 1998; Wagner, 1989; Stallion et al., 1991; Hoher, TroidI, 1995).
Диуретики рассматриваются в качестве допинговых препаратов на основании следующих фактов: а) спортсмены, соревнующиеся в видах спорта, где происходит разделение на весовые категории, могут снижать массу тела искусственно стимулированным диурезом, т. е. увеличением выделения мочи; б) увеличение водных потерь приводит к разбавлению мочи и снижению концентрации выделяемых веществ. Таким образом, диуретики могут маскировать применение запрещенных субстанций, для которых установлен количественный порог содержания в моче. Класс диуретиков, в частности, может служить демонстрацией физико-химической гетерогенности одной группы препаратов. На основании химической структуры, места и механизма воздействия диуретические препараты могут быть разделены, но меньшей мере, на 6 групп. Это так называемые тиазиды (например, гидрохлортиазиды), производные сульфамоилбензойной кислоты (например, фуросемид), осмотические диуретики (например, маннитол), ингибиторы карбоангидразы (например, ацетазоламид), производные феноксиуксусной кислоты (например, этакриновая кислота) и калийсберегающие диуретики (например, спиронолактон).
Препараты, блокирующие β-адренорецепторы (также называемые β-блокаторы), запрещены для применения в таких видах спорта, как стрельба и прыжки на лыжах из-за их седативного эффекта. В общем структурная формула β-блокаторов включает фенольное кольцо с оксипропаноламиновой боковой цепью, которая заканчивается изопропиловым или третбутиловым остатком (как в случае иропранолола и левобунолола), либо фенилэтаноламиноиое ядро с заменами боковых атомов водорода, например на нитритный остаток (нифеналол). Современные β-блокаторы могут иметь и несколько иную структуру, как например лекарственный препарат небиволол. Начиная с 1988 г. этот класс препаратов был включен МОК в список запрещенных к применению субстанций.
В списке запрещенных субстанций, приведенном выше, есть и другие классы запрещенных веществ, таких, как пептидные гормоны, однако здесь мы будем рассматривать только низкомолекулярные химические соединения.
Методы анализа [ править | править код ]
В целом предварительное хроматографическое разделение экстрактов, полученных из биологических материалов, таких, как кровь, моча или волосы является в большей или меньшей степени обязательным условием для последующего аналитического анализа. Это позволяет получить более подробную информацию об анализируемых образцах; например, разница во времени удержания позволяет разделить стереоизомеры, кроме того, так можно отделить вещества, представленные в образце в небольших концентрациях, от тех которые составляют его значительную часть. Современные хроматографические системы основаны на применении капиллярной газовой хроматографии или высокоэффективной жидкостной хроматографии, оба эти метода чрезвычайно сложны и развились в отдельные разделы аналитической химии.
Газовая хроматография [ править | править код ]
Сегодня капиллярные колонки представляют собой наиболее распространенное средство для проведения газовой хроматографии (ГХ) с целью допинг-контроля. Их высокая эффективность с точки зрения качества разделения, износоустойчивость и необыкновенное разнообразие неподвижных фаз обеспечивает широкий выбор для создания различных методик и возможности для решения таких задач, как проведение полного анализа или скрининг специфических веществ. Колонка состоит из трех основных элементов: (а) внешнего защитного покрытия; (б) слоя сорбента из плавленого кварца и (в) неподвижной фазы.
Кварцевое покрытие. Сорбирующий слой изготовлен из синтетического кварцеподобного стекла высокой степени чистоты с низким содержанием примесей оксидов металлов. Такое покрытие благодаря наличию групп силанола имеет чрезвычайно активную поверхность, которая может реагировать с полярными группами анализируемых веществ, такими, как гидроксильные, карбоксильные и тиольные остатки, а также первичными и вторичными аминами, что приводит к появлению «хвостов» у пиков разделяемых веществ и снижению интенсивности пиков. Поэтому при подготовке колонки производится деактивация силанольных групп с помощью подходящей химической обработки, например путем триметилсилилирования. Полученное таким образом покрытие хорошо подходит для нанесения неподвижной фазы.
Неподвижная фаза. Неподвижная фаза в газовой хроматографии играет основную роль, поскольку именно она определяет время удержания, качество разделения и форму пиков анализируемых веществ. Эта особая часть капиллярной колонки состоит либо из полисилоксанов/силиконов, полиэтиленгликолей (ПЭГ) либо из пористого слоя сорбента. Чаще всего в качестве неподвижной фазы используют замещенные полисилоксаны, которые обладают высокой стойкостью и сроком службы. Общая химическая структура неподвижных фаз изображена на основе полисилоксанов, которые представляют собой цепочку из чередующихся кислорода и кремния с боковыми замещающими группами, присоединяющимися по две к каждому атому кремния. Структура и количество замещающих групп являются характеристикой каждой неподвижной фазы. Используют преимущественно четыре замещающие группы в разном соотношении: а) метальные; б) фенильные; в) цианопропильные, г) трифторпропильиыс остатки. Выбор замещающих групп и их относительная представленность в неподвижной фазе определяют полярность ГХ колонки. Еще одним материалом, применяемым для формирования неподвижной фазы в ГХ-колонках, является ПЭГ, основной характеристикой которого является молекулярный вес или длина цепей полимера. Существенное отличие этого материала от полисилоксана заключается в возможности создания неподвижных фаз с определенным значением pH, т. е. кислотных или щелочных колонок, которые демонстрируют лучшие показатели при разделении кислотных или щелочных соединений соответственно. Основным недостатком является высокая чувствительность к кислороду, особенно при повышенных температурах, которая приводит к разрушению неподвижной фазы и сокращает срок службы колонки. Неподвижные фазы для адсорбционной хроматографии состоят из мельчайших частичек пористых материалов (например, полимеров, оксида алюминия, молекулярных сит), которые присоединяют к кварцевому покрытию капилляра с помощью химических линкеров. Благодаря высокой адсорбирующей способности в отношении газообразных веществ такие неподвижные фазы используют преимущественно для хроматографии наиболее летучих компонентов или газов, которые обычно плохо связываются с неподвижными фазами на основе полисилоксанов или ПЭГов, поэтому температуры разделения здесь не превышают 35 ’С. В случае применения так называемых капиллярных ГХ колонок PLOT (porous layer open tubular) твердофазная абсорбция газов является основным механизмом разделения, обеспечивающим эффективное удержание летучих веществ. В то же время сильная адсорбция анализируемого вещества на неподвижной фазе не позволяет использовать такие колонки для деления менее летучих веществ.
Внешняя оболочка. Поскольку капилляры из сплавленного кварца очень хрупкие, для них требуется защитное внешнее покрытие. Для этой цели обычно используют полиимид, который обладает двумя достоинствами: во-первых, колонки с полиимидной оболочкой достаточно прочные и не требуют деликатного обращения, во-вторых, полиимид покрывает и заполняет все трещины в капиллярах из сплавленного кварца, предотвращая увеличение дефектов.
После рассмотрения устройства капиллярной колонки для газовой хроматографии следует отметить еще два параметра, оказывающих заметное влияние на качество хроматографического разделения: размеры колонки, т. е. длина, диаметр и толщина пленки неподвижной фазы, а также газы-носители.
Тогда как длина и диаметр колонки влияют в основном на разрешение пиков, толщина пленки неподвижной фазы определяет емкость колонки и удержание анализируемых веществ. Длина колонки прямо пропорциональна количеству теоретических тарелок, а поскольку разрешение пропорционально корню квадратному количества теоретических тарелок, разрешение также будет пропорционально корню квадратному длины колонки. Иными словами, удвоение длины колонки (а значит, и количества теоретических тарелок) будет приводить к улучшению разрешения не на 100 %, а только на 25—35 %; уменьшение длины колонки на 50 % приведет к ухудшению разделения примерно на 15 — 25 %. Кроме того, количество теоретических тарелок обратно пропорционально диаметру колонки, следовательно, уменьшение диаметра колонки будет увеличивать эффективность газовой хроматографии, т. е., поскольку разрешение пропорционально квадратному корню из количества теоретических тарелок, уменьшение диаметра колонки в два раза также позволит улучшить разделение на 25—35 %, как, например, при замене колонки с внутренним диаметром 0,2 мм2 на колонку с диаметром 0,11 мм2. Емкость колонки непосредственно определяется толщиной пленки неподвижной фазы. Если толщина слоя неподвижной фазы 0,1—0,2 мкм подходит для анализа 20—50 нг вещества, то для анализа количеств больше 125 нг необходима колонка с толщиной неподвижной фазы 0,5 мкм, поэтому толщина пленки должна быть подобрана в соответствии с предполагаемым количеством анализируемых веществ, наносимых на ГХ колонку.
Кроме того, на параметры хроматографического разделения влияет также используемый в качестве носителя газ, эта зависимость описывается кривой Ван Деемтера. В качестве газов-носителей часто используют гелий и водород, причем последний обеспечивает превосходную оптимальную линейную скорость, в результате чего значительно улучшается качество разделения. Явный недостаток водорода щ его высокая воспламеняемость.
Жидкостная хроматография [ править | править код ]
По сравнению с газовой, принадлежности для жидкостной хроматографии отличаются значительным разнообразием размеров, наполнителей и, поскольку разделение происходит при переносе в жидком носителе, большим набором органических растворителей и буферов. Помимо того, в жидкостной хроматографии (ЖХ) в зависимости от свойств анализируемых веществ могут применяться несколько различных механизмов разделения (нормально-фазовая, обращенно-фазовая, ионообменная и ситовая). В этом кратком обзоре мы коснемся только обращенно-фазовой хроматографии (ОФХ ), которая чаще всего используется при проведении анализов с целью допинг-контроля.
Картриджи. Для использования в ЖХ предлагаются картриджи-колонки различного диаметра. После усовершенствования материалов-наполните-лей (т.е. неподвижной фазы, см. ниже) в лабораториях допинг-контроля для анализа низкомолекулярных соединений чаще всего используют колонки длиной 30—120 мм с внутренним диаметром 1,0— 4,6 мм, тогда как в прежние времена для высокоэффективной жидкостной хроматографии (ВЭЖХ) применялись гораздо более объемные и длинные колонки. Уменьшение длины колонок стало возможным после появления обладающих высокой специфичностью высокоизбирательных масс-анализаторов, которые позволяют осуществлять разделение веществ на основании их масс-спегара, благодаря чему потребность в оптимальном хроматографическом разделении анализируемых веществ стала не столь актуальной. Кроме того, была существенно повышена производительность колонок для ЖХ, и это значительно сократило время, необходимое для разделения пиков.
Неподвижная фаза. Как отмечалось выше, определяющим фактором в хроматографии являются параметры неподвижной фазы и жидкостная хроматография в этом не исключение. Здесь необходимо учитывать различные характеристики, в частности размер частиц (3—50 мкм), особенности носителя (частицы силикагеля сферической или неправильной формы), наличие химически связанной фазы (например, С4, С8, С18) и размер пор (50—4000 А).
Для оценки характеристики эффективности хроматографической колонки часто используют пара-метр «количество тарелок п» или «высоту тарелки h». Уравнение Ван Деемтера в его простейшем виде описывает обратную взаимосвязь размера частиц и высоты тарелки; это означает, что уменьшение размера частиц ведет к улучшению эффективности хроматографии, а именно разрешения (Yamashita, Fenn, 1984а; Engelhardt et al., 1985). Поэтому существует тенденция к уменьшению размера частиц наряду с использованием очень коротких колонок в высокоскоростной хроматографии для обеспечения требуемого разрешения пиков.
Чаще всего в качестве материала для приготовления неподвижной фазы обратно фазовой хроматографии используется силикагель. Представленные в продаже виды силикагеля отличаются по своим физическим характеристикам, таким, как площадь специфической поверхности, средний диаметр пор, специфический объем пор и форма. Предполагая, что частицы имеют открытые поры цилиндрической формы, можно выразить взаимосвязь между первыми упомянутыми переменными следующим уравнением:
где 0 — средний диаметр пор, нм; Vp — специфический объем пор, млт»1; Оsp — специфическая площадь поверхности, м2т
‘ (Scott, 1982). При средней площади поверхности, равной около 300 м2т
‘, и диаметре пор 10 им специфический объем пор будет составлять примерно 1 млт»1. В настоящее время как носитель для создания неподвижной фазы в обращенно-фазовой ЖХ в большинстве случаев используют сферические частицы силикагеля, поскольку с помощью его можно достичь более высокой плотности упаковки по сравнению с частицами неправильной формы, полученными при полимеризации кремниевой кислоты. На поверхности такие частицы несут гидроксильные группы (силанольные остатки), которые могут быть использованы для создания химически привитой фазы; она и будет определять свойства колонки для ВЭЖХ. В продаже представлен широкий выбор разнообразных фаз, позволяющий решать самые различные задачи хроматографического разделения, например, часто используют фазы с привитыми феи ильными С18-, С8- и С4-группами, либо более полярные материалы, такие, как фазы с привитыми циано-, амино- и диольными группами. Более того, созданы еше более сложные системы, позволяющие разделять молекулы-стерсоизомеры одного соединения. Самых последних результатов в области высокопроизводительного хроматографического анализа удалось добиться благодаря созданию так называемой монолитной колонны, представляющей собой единый кусок органического полимера или диоксида кремния со сквозными порами в нем, полученный прямой полимеризацией соответствующих мономеров. Такой материал отличается более высокой стабильностью и, что важно, более высокой производительностью по сравнению с обычными колонками, заполненными отдельными частицами.
Подвижная фаза. В случае ОФГ неподвижная фаза является неполярным, а подвижная — полярным компонентом. Обычно в ОФГ применяют буферные системы, состоящие, например, из KH2PO4/H3PO4 или NaH2РО4 в сочетании с такими органическими растворителями, как метанол или ацетонитрил, которые хорошо подходят для анализа с помощью ультрафиолетовых (УФ) детекторов. В то же время применение ВЭЖХ в сочетании с МС предъявляет более серьезные требования к характеристикам элюэнтов, поскольку в отношении ЖХ существуют ограничения на допустимый диапазон pH, выбор растворителя, содержание добавок в растворителе и скорость подачи элюзита, направленные на достижение оптимальных результатов масс-спектрометрии (Wheeler, 1955). Обычно в случае ионизации при атмосферном давлении (например, злектрораспылением) требуется добавление легколетучих растворителем для предотвращения примесей ионов анализируемого вещества, поэтому часто применяемые фосфатные, боратные или сульфатные добавки здесь не подходят, вместо них используют ацетат аммония, формиат аммония или тетраэтиламмониумгидроксид. Более того, при использовании ионизации электрораспыленном не допускаются ингредиенты, которые дают сильные ионные пары, в результате чего после десорбции происходит нейтрализация ионов. Первостепенное значение имеет поддержание pH, особенно в случае ионизации электрораспылепием, поскольку этот параметр усиливает ионизацию анализируемого вещества. Анализ соединений, имеющих щелочную природу, следует производить при кислом pH, применяя такие добавки, как уксусная или муравьиная кислота в концентрации 0,1 —1,0 X. в то время как соединения с кислотными свойствами (например, карбоновые кислоты) легче ионизируются в щелочной среде, которую можно создать, например, добавлением гидроксида аммония. В числе часто используемых органических растворителей те же, что применяются и при обычной ВЭЖХ без МС. т. с. метанол, этанол и ацетонитрил.
Детекторы [ править | править код ]
Детекция и идентификация разделенных хроматографией веществ в допинг-контроле имеет чрезвычайно важное значение. К настоящему времени разработано множество различных систем детекции, в частности пламенно-ионизационный детектор (ПИД), азотно-фосфорный детектор (АФД), УФ фотометрический детектор, а также масс-спектрометрические детекторы, такие, как квадрупольные, времяпролетные, ионные ловушки, масс-анализаторы ионно-циклотронного резонанса с Фурье-преобразо-ванием, тройные квадрупольныс детекторы, магнитные секторные анализаторы. Кроме того, в продаже имеются приборы, включающие два и более различных типов детектирующих устройств, а также разработаны различные прикладные системы для определения применения запрещенных веществ, которые базируются на использовании специальных методик приготовления образцов в сочетании с хроматографией и детектором, обладающих хорошей чувствительностью и избирательностью.
Пламенно-ионизационные детекторы применяются в сочетании с газоном хроматографией уже достаточно давно и являются, пожалуй, одними из наиболее универсальных. Выходящий из хроматографической колонки газ смешивается с воздухом, насыщенным водородом, и воспламеняется с помощью электроподжига. При сгорании водорода в воздухе образуется незначительное количество ионов, однако при пиролизе в пламени водорода большинство органических соединений дает значительное количество ионов и электронов и это приводит к увеличению проводимости. На так называемый коллектор или собирающий электрод подается напряжение, под действием которого возникает электрический ток, величина которого пропорциональна количеству образца, сгоревшего после выхода из хроматографической колонки. Ток регистрируется с помощью амперметра, преобразуется в цифровой сигнал и отображается в виде пика на хроматограмме.
Азотно-фосфорный детектор (АФД) представляет собой разновидность ПИД. Основное различие заключается в том, что непосредственно нал форсункой горелки располагается стеклянный или керамический элемент. Низкое соотношение водород/воздух не позволяет поддерживать пламя, что приводит к снижению ионизации углеводов. Однако щелочные ионы па поверхности керамического элемента способствуют ионизации соединений, содержащих фосфор или азот, облегчая их детекцию па фоне остальных веществ, имеющих преимущественно углеводную природу.
ДЕТЕКТОР ПОГЛОЩЕНИЯ УЛЬТРАФИОЛЕТОВОГО ИЗЛУЧЕНИЯ
Тогда как ПИД и АФД могут применять только в сочетании с ГХ, детектор УФ-поглощения, начиная с конца 1960-х гг., является одним из наиболее распространенных анализаторов для ВЭЖХ. Принцип его работы основан на обычной спектрометрии и законе Бера—Ламберта:
где I0 — интенсивность падающего света; I — интенсивность прошедшего света; е — коэффициент экстинкции (поглощения); с — концентрация поглощающего анализируемого вещества; d — толщина слоя поглощающего вещества. На практике элюируемые вещества после ВЭЖХ колонки проходят через ячейку определенной длины, источник света испускает УФ-излучение (например, дейтериевая лампа, 190 — 600 нм) постоянной интенсивности, которое через монохроматор попадает на ячейку, интенсивность пропущенного света определенной длины волны определяется с помощью фотодиодов.
Описанные детекторы позволяют распознавать вещества, разделенные хроматографией — ГХ или ВЭЖХ. Основным недостатком этих детекторов является их низкая специфичность и, соответственно, недостаток подробной информации об анализируемых веществах. Это стало причиной того, что аналитические приборы с масс-спектрометрическими детекторами становятся основным средством при проведении анализов с целью допинг-контроля, которое применяется в сочетании с ГХ и ВЭЖХ и дополняет возможности «традиционной» инструментальной базы на основе ПИД, АФД и УФ-детекторов. Для определения веществ с помощью МС необходимо перевести анализируемое вещество в ионную форму. Этого можно добиться рядом технических приемов, выбор которых происходит с учетом особенностей используемой хроматографической системы. В настоящее время в ГХ-системах, оснащенных масс-спектрометрическим анализатором, используют ионизацию электронным ударом или химическую ионизацию, тогда как в ВЭЖХ-установках применяется ионизация электрораспылепием, химическая ионизация при атмосферном давлении, а также фотоионизация при атмосферном давлении. Далее вкратце рассмотрим принципы ионизации электронным ударом и электрораспылением, а также квадрунольный анализатор и ионную ловушку — инструменты, которые чаще всего используют в лабораториях допинг-контроля.
Способы ионизации [ править | править код ]
ИОНИЗАЦИЯ ЭЛЕКТРОННЫМ УДАРОМ
Ионизация электронным ударом (EI) широко используется для создания позитивно заряженных ионов анализируемых веществ после разделения на ГХ-колонке. Электроны испускаются с катода (нагретая вольфрамовая или рениевая нить) и, ускоряясь под действием электрического поля, устремляются к аноду. Пучок разогнанных до определенной энергии электронов пересекает под прямым углом поток газа с элюируемыми веществами, поступающий из ГХ. При столкновении электронов, обладающих энергией 70 эВ (напряжение между катодом и анодом устанавливается равным 70 В), с молекулами анализируемого вещества, которое является источником ионов, могут происходить разнообразные процессы ионизации, например:
В случае позитивной ионизации наиболее важным механизмом является образование позитивно заряженной молекулы (АВ+) при потере электрона, выбитого ускоренным электроном из электронного потока между катодом и анодом (1). Кроме того, анализируемая молекула АВ может потерять два электрона, что приведет к образованию заряженной молекулы АВ2+ (2). Молекула АВ может также захватить свободный электрон и приобрести отрицательный заряд АВ’ (3). Помимо описанных выше вариантов воздействия электронного удара на вещество, выходящее с ГХ-колонки, следует принимать во внимание и другие последствия этого способа ионизации. Основным результатом электронного удара является образование высокоэнергетических катион- радикалов, распадающихся на ионы. В результате детекции этих ионов масс-селективным анализатором формируется характерный масс-спектр соответствующего вещества. В зависимости от происходящих перемещений и потерь электронов продуктами ионизации могут быть как радикалы, так и ионы с парным числом электронов.
ИОНИЗАЦИЯ ЭЛЕКТРОРАСПЫЛЕНИЕМ (ИЭР)
За разработку способа мягкой ионизации методом электрораспыления в 2002 г. присуждена Нобелевская премия по химии. Джон Фенн был награжден за фундаментальные исследования процессов ионизации макромолекул, которые были опубликованы еще в 1984 г. Ямашита и Фснном (Yamashita, Fenn, 1984b; Voyksner, 1997). Суть метода заключается в том, что жидкости, содержащие протонированные и депротонированные молекулы, распыляются через капиллярный наконечник при высоком напряжении (1 кВ и выше). При этом формируются заряженные капли, которые уменьшаются в объеме за счет испарения растворителя и последующего дробления, в результате образуются мельчайшие капли, обладающие очень высоким зарядом. В результате из этих мельчайших капель образуются газообразные ионы — этот процесс описывают две различные теории: модель заряженного остатка (Dole et al., 1968) и испарение ионов (Iribame, Thomson, 1976). Схематическое изображение основных процессов, происходящих при ионизации электрораспылением. Сначала распространение электрического ноля по жидкости внутри капилляра приводит к формированию положительного заряда иа поверхности жидкости, в результате чего происходит искажение мениска, формирование конусообразного выступа и распыление капель, обладающих значительным положительным зарядом. При испарении растворителя размер капель уменьшается, тогда как их заряд остается неизменным. Затем под действием нарастающего электростатического отталкивания происходит дальнейшее дробление капель, которое продолжается, пока они не достигнут Релеевского предела устойчивости. Это явление происходит одновременно с дальнейшим испарением растворителя, благодаря чему формируются частицы очень малого размера, обладающие высоким зарядом. В результате, как предполагается (Dole et al., 1968), образуются частицы, имеющие лишь один ион, а испарение растворителя приводит к возникновению газообразного иона (модель заряженного остатка). Альтернативная гипотеза постулирует, что эмиссия ионов происходит непосредственно с поверхности частиц вещества размером менее 10 нм, что также приводит к формированию газообразных ионов (испарение ионов) (Kcbarle, Но, 1997).
Масс-анализаторы [ править | править код ]
Ионы анализируемого вещества, полученные одним из способов ионизации, далее подвергаются анализу с помощью масс-селективных детекторов, например квадрупольного или ионной ловушки. Для работы обоих этих детекторов необходим глубокий вакуум, их можно использовать в сочетании как с ГХ (и ионизации вещества электронным ударом), так и с ВЭЖХ (например, с ионизацией электрораспылением) системами разделения. Поскольку ионизация электронным ударом происходит в вакууме, для подключения масс-анализатора не требуется никаких специальных приспособлений для выравнивания давлений, однако ионизация электрораспылением осуществляется при атмосферном давлении, поэтому современные системы ГХ-ИЭР-МС оборудованы сложными системами, обеспечивающими поддержание в масс-анализаторе необходимого давления.
Квадрупольный масс-спектрометр состоит из четырех стержней, которые могут быть изготовлены из различных материалов, например из плавленого кварца, покрытого слоем золота. Противоположные стержни соединены между собой, а расположенные рядом — изолированы друг от друга. Сначала ионы, образовавшиеся в источнике ионов, направляются с ускорением в центр квадруполя. Под действием переменного электрического поля, приложенного к стержням, по направлению к центральной линии квадруполя формируются позитивные или негативные поля, таким образом позитивные ионы, пролетающие вдоль стержней квадруполя, отталкиваются позитивными и притягиваются негативной поляризацией. Степень отклонения прямо пропорциональна приложенному напряжению, его частоте (т. е. продолжительность воздействия переменного поля) и массе ионов. Кроме того, к парам стержней прикладывается постоянное напряжение. В результате ионы с различным соотношением массы и заряда могут перемещаться в двухмерном поле квадруполя, если прикладываемые поочередно постоянное и переменное поля чередуются с частотой, которая обеспечивает устойчивое колебательное движение. Эти параметры можно изменять с целью оптимизации масс-селекции, благодаря чему становится возможным пропускать отдельные ионы или записывать полный спектр, выполняя в течение заданного времени поочередное сканирование в различных диапазонах соотношения масса/заряд (Budzikiewicz, 1998; Lottspeich, Zorbas, 1998).
Ионы, изолированные с помощью квадруполя, могут подвергаться дальнейшим исследованиям, как это происходит в масс-спектрометрах с тройным квадруполом. В таком масс-спектрометре имеются три соединенных между собой квадруполя, первый из которых используется для того, чтобы из пучка ионов, попадающего в масс-спектрометр, отобрать ионы с определенными характеристиками (масса/заряд). Во втором квадруполе, так называемой камере столкновений, отобранные ионы соударяются с молекулами газа (аргон или азот) и подвергаются дальнейшему распаду, степень которого зависит от приложенного ускоряющего напряжения и давления газа в камере для столкновений. Образовавшиеся в результате столкновения ионы измеряются в третьем квадруполе либо путем сканирования полного спектра либо измерения отдельных ионов, что позволяет получить информацию о процессах фрагментации, а также о структуре анализируемого вещества.
КВАДРУПОЛЬНАЯ ИОННАЯ ЛОВУШКА
В качестве альтернативы масс-спектрометрам с квадрупольным анализатором часто используют анализаторы с квадрупольной ионной ловушкой. Еще в 1953 г. Вольфганг Пол с соавторами описал возможность использования трехмерного квадруполя в качестве «ионной ловушки», а в последнее десятилетие на основе этого предположения были созданы сложные масс-спектрометры с ионными ловушками (Louris et al., 1987, 1989; Patterson et al., 2002). Ha рис. 5.10 представлена схема устройства ионной ловушки, которая состоит из двух чашеобразных электродов (один со входом для ионов, а другой с отверстием для их выхода) и кольцевого электрода. Определенное сочетание радиочастотных и постоянных напряжений, прикладываемых к электродам ионной ловушки, позволяет удерживать ионы внутри нее. Ионы, которые формируются во внешнем источнике ионов (например, с использованием ионизации электронным ударом или ялектрораспылением), попадают в ионную ловушку, содержащую газ (гелий или аргон) под давлением равным около 1 мторр. Чаще используют гелий, который замедляет ионы, отклоняя их траекторию к центру ловушки. Кроме того, наличие газа позволяет снизить кинетическую энергию ионов при их столкновениях с молекулами газа, что также способствует захвату ионов ловушкой. Удержание ионов в широком диапазоне значений отношения масса/заряд определяется переменным напряжением, которое подается на кольцевой электрод. Поэтому последовательный выброс ионов, предоставляющий возможность их масс-избиратель-ной детекции, обеспечивается так называемым состоянием неустойчивости, которое создается путем постепенного увеличения переменного напряжения на кольцевом электроде в сочетании с приложением переменного напряжения к чашеобразным электродам на концах ионной ловушки, что приводит к возникновению резонансного движения. Ионы с определенным соотношением масса/заряд выходят на нестабильные траектории и выбрасываются через отверстия на чашеобразном электроде (выход ионов) и детектируются с помощью электронного умножителя.
Помимо эффективного режима сканирования, спектрометры с ионными ловушками предоставляют широкие возможности для МСп экспериментов. Избирательное удаление ионов из ловушки, накопление определенного типа ионов-предшественников с последующей их резонансной активацией позволяет добиться диссоциации, индуцированной столкновениями (collision activated dissociation, CAD). В результате образуется спектр ионных продуктов, предоставляющий объем информации, сопоставимый с тем, который дают эксперименты с использованием тройного квадруполя. Вместе с тем ионная ловушка обладает важным преимуществом, поскольку позволяет отбирать, накапливать и расщеплять иоиы, получаемые в МС/МС-экспериментах, а именно МС3, предоставляя информацию о возможных способах фрагментации и составе образующихся при диссоциации ионах, что представляет значительный интерес, особенно в случае масс-спектрометрии в сочетании с ионизацией электрораспылеиием.
Очистка и приготовление образцов [ править | править код ]
Согласно установленным правилам, для анализа на запрещенные субстанции при допинг-контроле спортсмены сдают главным образом мочу. Кроме того, в определенных случаях для идентификации конкретных препаратов могут быть получены образцы крови, плазмы/сыворотки и волос. Приготовление образцов является чрезвычайно важным элементом допинг-контроля, поскольку в значительной мере обеспечивает достижение максимально возможной определенности результатов и необходимой чувствительности при проведении анализов. К настоящему времени разработаны разнообразные приемы очистки образцов от солей и других примесей, в частности выделения целевого анализируемого вещества.
Жидкостная экстракция [ править | править код ]
Чаще всего и, вероятно, дольше всего используется метод приготовления образцов жидкостной экстракции. В одной из первых работ, посвященных идентификации бензедрина (рацемическая смесь амфетаминсульфата) и его метаболитов в моче человека, жидкостная экстракция применялась для определения скорости экскреции (Richter, 1938). В частности, пробы мочи подвергали гидролизу 2 н. гидроксидом натрия и экстрагировали петролейиым эфиром. В последующие десятилетия были описаны многочисленные методики очистки веществ, содержащихся в биологических жидкостях, с применением жидкостной экстракции. В основу всех этих методик был положен один и тот же принцип: изменение pH до необходимого значения и экстракция кислых, нейтральных или щелочных компонентов (Keller, Ellenbogen, 1952; Axelrod, 1954; Beckett, Rowland; 1965; Beckett, Wilkinson, 1965; Kolb, Patt, 1965; Cartoni, Cavalli, 1968). Знание величины pi анализируемых веществ предоставляет возможность многократной экстракции проб и/или повторной экстракции их компонентов при различных pH различными растворителями. Стремление к созданию более детальных, специфических и чувствительных методов анализа сопровождалось совершенствованием и развитием процедур жидкостной экстракции, направленным на снижение количества коэкстрагируемых примесей, создающих помехи при анализе. Разработанные принципы и сегодня используются в методах скрининга и подтверждения при проведении анализов с целью допинг-контроля (Donike et al., 1970; Spyrdaki et al., 2001; Van Eenoo et al., 2001; Thevis et al., 2003b), например, стимуляторы, такие, как амфетамины, эфедрины и их производные, обычно экстрагируют из проб мочи эфирами в щелочных условиях, вещества, экстрагированные органической фазой, концентрируются и подвергаются дальнейшему анализу ГХ-МС и/или ГХ-АФД. Помимо того, жидкостная экстракция применяется для анализа кортикостероидов (Fluri et al., 2001), диуретиков, веществ, блокирующих активность р-рецепторов и анаболических стероидов при различных условиях (т. е. в присутствии минеральных солей, органических растворителей и при разных значениях pH) (Geyer et al., 1997; Thevis et al., 2001; Deventer et al., 2002).
Очень мощным средством оказалась так называемая рсэкстракция или повторная экстракция, которая применялась уже в 1952 г. (Keller, Ellenbogen, 1952). Этот метод применяется для повышения чистоты образцов, которые предстоит подвергнуть анализу. В частности, экстракция анализируемых веществ в щелочных условиях в органический растворитель с последующим перемещением интересующих исследователя веществ из органической в закисленную водную фазу (0,06 н., НС1) доказала свою пригодность для подтверждающих тестов, например для Р2-агониста кленбутерола, благодаря крайне эффективному снижению количества разнообразных биологических примесей (Sigmund et al., 1998).
Твердофазная экстракция [ править | править код ]
Для ряда веществ используется альтернативный способ очистки и концентрации анализируемых веществ, содержа1цихся в биологических пробах, а именно твердофазная экстракция (ТФЭ ). Применение различных адсорбирующих материалов, в частности полистирола, С18 или ионообменных смол, позволило создать некоторые методики скрининга и получения доказательств, используемых при проведении допинг-контроля. В 1968 г. Брсдлоу продемонстрировал возможность экстракции стероидных коньюгатов нейтральными полимерными смолами (Bradlow, 1968). Дальнейшее совершенствование использованных им материалов и приемов позволило создать методику, пригодную для использования для проведения допинг-контроля, например па применение анаболических стероидов (Donike et al., 1984) и диуретиков (Thieme et al., 2001). Основным достоинством ТФЭ является возможность полной автоматизации процедуры экстракции образцов, включая подготовку картриджей, загрузку проб, промывку и последующую элюцию. Кроме того, в ходе ТФЭ можно производить дериватизацию анализируемых веществ (Lisi et al., 1991).
Иммуноаффинная хроматография [ править | править код ]
Иммуноаффинную хроматографию (ИАХ ) в качестве средства выделения анализируемых веществ из биологических проб стали применять относительно недавно. Суть метода заключается в том, что моно-или поликлональные антитела, способные образовывать нековалентную связь с различными частями анализируемых молекул, пришивают к носителю, например к сферическим частицам агарозы. Гелем, приготовленным из таких частиц, заполняют колонку с пористым фильтром на одном конце и пропускают через нее пробы мочи или плазмы. При пропускании через колонку искомых анализируемых веществ антитела, связанные с носителем, узнают их и связывают, формируя нековалентные комплексы, тогда как остальные молекулы, не способные взаимодействовать с антителами, элюируются с растворителем. Изменение условий элюирования позволяет разрушить комплекс вещество—антитело, не разрушая при этом самих молекул, и получить анализируемое вещество в очищенном виде, практически без посторонних примесей, для проведения дальнейшего анализа, например с помощью ГХ-МС. Химические реакции, лежащие в основе приготовления адсорбента для наполнения колонки, и основные процессы, положенные в основу метода иммуиоаффинной хроматографии, представлены на схеме 5.5. Чаще всего в качестве носителя используют частицы агарозы, которые предлагаются для продажи рядом фирм. Для того чтобы к этим частицам можно было пришить химическим путем пептиды или белки, поверхность этих частиц активируют. Наиболее часто применяют метод активации цианогенбромидом (CNBr), предложенный в 1967 г. Аксеном (Axen et al., 1967). В щелочных условиях CNBr реагирует с гидроксильными группами на поверхности частиц агарозы с образованием циановых эфиров и имидокарбонатов, которые, в свою очередь, вступают в химическую реакцию с антителами (Hermanson et al., 1992). Частицы агарозы с присоединенными к ним антителами, помещенные в колонку, узнают и избирательно связывают только специфические вещества или классы веществ, присутствующие в биологических образцах. Использование подходящих элюентов, например смеси воды и органических растворителей, позволяет освободить связанное с антителами вещество, сконцентрировать его и анализировать при помощи стандартных методов, в частности МС (Schanzer et al., 1996; Machnik et al., 1999). Снижение количества посторонних примесей приводит к улучшению соотношения сигнал/шум и снижению порога детекции методами ГХ-МС и ЖХ-МС/МС.
Метод дериватизации [ править | править код ]
ГХ-МС является основным инструментом скрининга и получения доказательств в лаборатории допинг-контроля. Такие системы обладают высокой специфичностью и чувствительностью к многочисленным веществам, занесенным в список запрещенных субстанций МОК и ВАДА. Однако для проведения анализа с помощью ГХ-МС вещества должны быть переведены в газообразную форму. Поскольку это требование для многих анализируемых веществ, например Р2-агонистов, различных диуретиков и блока-торов p-рецепторов, выполнить достаточно сложно, путем реакций с различными реагентами получают их более легколетучие производные. Превращениям подвергают в первую очередь гидроксильные группы и вторичные аминогруппы, поскольку именно их способность к гидрофильным взаимодействиям является одной из причин сниженной летучести. Одной из первых осуществлявшихся модификаций анализируемого вещества было ацетилирование с помощью уксусного ангидрида. Образовавшиеся молекулы необходимо было очищать от остатков уксусной кислоты и уксусного ангидрида, что обычно выполняли с помощью жидкостной экстракции. Поскольку этот способ получения производных для ГХ-МС анализа достаточно сложный и трудоемкий, были разработаны несколько дериватизационных агентов, в состав которых, как правило, входят остатки триметилсилила (ТМС). Приводим некоторые из таких агентов: гексаметилдисилазан (ГМДС), триметилсилилимидазол (ТМСИми) и N-метил-N-триметилсилилтрифторацетамид (МСТФА) (Donike, 1969). Последний является наиболее часто применяемым для дериватизации веществом, в частности в сочетании с иодидом аммония и этаптиолом, который in situ приводит к образованию триметилйодсилана (ТМИС), высокореактивного триметилсилилирующего реагента (Donike, 1973; Donike, Zinunermann, 1980). В присутствии ТМСИ происходит модификация гидроксильных и аминогрупп, а кетоновые остатки превращаются в енол-ТМС эфиры. Несколько других мощных реагентов применялись для введения в анализируемые молекулы трифторацетил (ТФА)-или гептафторбутил (ГФБ)-остатков, а именно N,N-бистрифторацетамид, N-метил-N-бистрифтораце-тамид (МБТФА) (Donike, Derenbach, 1976) или N-метил-N-бисгептафторбутиламид (МБГФБ) соответственно. Трифторацетилирование приводит к формированию более стабильных производных аминогрупп по сравнению с триметилсилилированием, поэтому возможна также избирательная модификация анализируемых веществ ТМС- и ТФА-группами, что делает возможным хроматографическое разделение стереоизомеров таких стимуляторов, как эфедрины (Opfermann, Schanzer, 1996; Thevis et al., 2003b).
Читайте также [ править | править код ]
Предупреждение [ править код ]