Что такое дисплазия предстательной железы у мужчин
Доброкачественная гиперплазия простаты
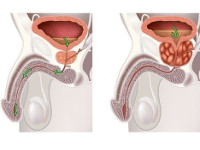
Доброкачественная гиперплазия простаты — это патология, связанная с ростом железистой ткани, влекущим увеличением органа в размерах. Альтернативное название — аденома простаты. Болезнь провоцирует нарушения работы мочевыделительной системы. Ее характерные признаки — неполное опустошение мочевого пузыря, слабая струя урины, частые позывы. При ДГПЖ возможны разные пути лечения — консервативное или хирургическое.
Общие сведения о болезни
Доброкачественная гиперплазия предстательной железы, как правило, развивается с возрастом. Болезнь диагностируется у ⅓ части мужчин после 50 лет и у 90% пациентов после 85 лет. Почти 30 миллионов мужчин по всему миру беспокоят нарушения мочеиспускания, связанные с патологическим разрастанием тканей простаты.
По статистике доброкачественная гиперплазия чаще диагностируется у афроамериканцев, что связано с популяционными особенностями — повышенной концентрацией тестостерона, активностью фермента 5-альфаредуктазы, экспрессией рецепторов андрогенов. Реже всего доброкачественная гиперплазия выявляется у представителей монголоидной расы — жителей Азии. Ученые связывают эту особенность с регулярным употреблением продуктов питания, содержащих фитостеролы.
Причины развития доброкачественной гиперплазии
На развитие заболевания влияет целый комплекс факторов. Основная причина разрастания тканей — возрастные изменения, влекущие гормональные колебания. В этом случае мужская мочеполовая система функционирует без сбоев, но запускается естественное старение организма. Предполагается, что доброкачественная гиперплазия становится следствием стимуляции рецепторов простаты на фоне повышения концентрации эстрадиола и дигидротестерона.
Не исключено также влияние других факторов. Риск развития аденомы повышают:
Как развивается доброкачественная гиперплазия
Доброкачественная гиперплазия проходит в своем развитии три последовательные стадии, отличающиеся степенью поражения органа и клинической картиной:
При диагностике врач оценивает не только клинические проявления болезни, но и размеры патологического разрастания тканей. В зависимости от объема возможны:
Чем больше объем разрастания предстательной железы, тем сильнее сдавливаются мочевыводящие пути, поэтому лечение нельзя откладывать. Если не принимать меры, изменения коснутся мочевого пузыря. Гладкая мускулатура заменяется соединительной тканью, которая менее эластична. Стенки органа становятся тонкими, а его объем увеличивается. На слизистых формируются эрозивные участки, присоединяется инфекция. Застой мочи на фоне сужения уретрального канала и изменений мочевого пузыря — причина тяжелых патологий почек, требующих экстренного лечения.
Клиническая картина
В начале развития доброкачественная гиперплазия предстательной железы провоцирует симптомы, которые можно принять за воспаление уретры. Характерные признаки:
При отсутствии лечения доброкачественная гиперплазия прогрессирует. Мужчину беспокоит сильное желание помочиться, недержание мочи, что связано с нарушением иннервации на фоне роста аденомы.
На поздних этапах пациент не может произвольно опорожнять мочевой пузырь. Его беспокоит капельное подтекание мочи. Симптомы связаны с критическим сдавливанием уретры, ослаблением координации работы мочевого пузыря, воспалением на его стенках.
Диагностика доброкачественной гиперплазии
При подозрении на разрастание тканей простаты до начала лечения требуется консультация андролога или уролога. После сбора информации о жалобах проводится ректальный осмотр предстательной железы, но он не всегда информативен. При пальпации определяется увеличение простаты. Ее покровы ровные, эластичные, безболезненные на ощупь.
Диагноз доброкачественная гиперплазия ставится на основе осмотра, результатов инструментальной диагностики и лабораторных исследований. Для выявления аденомы предстательной железы, оценки ее размеров, стадии, а также своевременной диагностики сопутствующих нарушений пациенту назначаются:
Если доброкачественная гиперплазия предстательной железы осложняется патологиями почек, для выбора тактики лечения дополнительно потребуется консультация нефролога. При подозрении на злокачественную опухоль простаты проводится биопсия.
Лечение доброкачественной гиперплазии
При выборе способа лечения врач оценивает симптомы, которые вызывает доброкачественная гиперплазия простаты. Возможны четыре варианта тактики действий:
Хирургическое лечение сопряжено с рисками осложнений и длительным реабилитационным периодом, поэтому к нему прибегают, если другие методики не привели к результату. По статистике, доброкачественная гиперплазия требует оперативного вмешательства лишь в 15-20% случаев. Остальные пациенты проходят консервативное лечение с длительным либо пожизненным приемом препаратов.
После терапии пациенту потребуется уделять достаточно внимания профилактике болезни. Доброкачественная гиперплазия будет беспокоить меньше, если убрать из рациона жирную пищу, сделав акцент на белковых продуктах и овощах, а также подключить умеренную физическую активность.
Филиалы и отделения, в которых лечат доброкачественную гиперплазию простаты
НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиала ФГБУ «НМИЦ радиологии» Минздрава России.
Современные возможности медикаментозного лечения доброкачественной гиперплазии ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2].
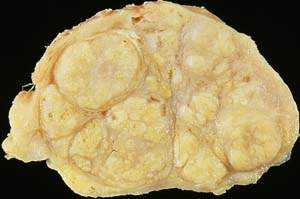 |
| Рисунок 1. Доброкачественная гиперплазия предстательной железы (макропрепарат) |
К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2]. Около 80% мужчин старше 80 лет страдают этим заболеванием. Другая статистика свидетельствует, что из всех заболеваний, которым подвержены мужчины старше 50 лет, на долю доброкачественной гиперплазии простаты приходится 36% [1]. Эти сведения настолько общеизвестны, что ухудшение качества мочеиспускания часто рассматривается как естественное явление.
Клинически данное заболевание проявляется различными симптомами, связанными с нарушением пассажа мочи по нижним мочевым путям. При значительно выраженной инфравезикальной обструкции, как правило, прибегают к хирургическому вмешательству. Оперативное лечение по поводу ДГПЖ показано 30% больных в возрасте от 50 до 80 лет [4]. Однако в последние годы все большую популярность завоевывает медикаментозная терапия доброкачественной гиперплазии предстательной железы. Это, с одной стороны, объясняется вполне логичным желанием врача и пациента по возможности избежать операции, с другой — развитием представлений о патогенезе расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы.
До недавнего времени патогенез расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы рассматривали с позиции классических представлений о механической инфравезикальной обструкции и развитии вторичных структурно-функциональных изменений детрузора (компенсация, декомпенсация). За последние два десятилетия получены принципиально новые данные о природе повышенного внутриуретрального сопротивления. Его перестали отождествлять исключительно с механическим сдавлением шейки мочевого пузыря и задней уретры. Обнаружен динамический компонент обструкции, который состоит в повышении тонуса указанных анатомических структур за счет активности a-адренорецепторов. Появились также иные трактовки происхождения ирритативных симптомов. Их считают проявлением первичного нестабильного мочевого пузыря и не связывают напрямую с обструкцией [5].
Результаты нашей работы свидетельствуют, что при ДГПЖ клиническая симптоматика развивается вследствие недостаточности энергетического метаболизма и гипоксии детрузора в условиях повышенного уретрального сопротивления [3]. Об этом свидетельствуют:
Причины нарушений энергетического метаболизма и функций детрузора крайне многообразны. В частности, к таким нарушениям могут привести повышение активности симпатической нервной системы, расстройства органного кровообращения, авитаминоз (группа В), хронические заболевания дыхательной и сердечно-сосудистой систем, влияние приема ряда фармакологических препаратов, угнетающих дыхательную цепь, и, естественно, обструктивные нарушения уродинамики и т. д. Весьма важно, что нарушения гипоксического характера в гладкомышечной ткани могут иметь и первичный митохондриальный генез (первичные нарушения энергетического метаболизма детрузора [3].
Необходимо отметить, что у больных ДГПЖ в нижнем отделе мочевого тракта протекают два параллельных процесса — формирование уретральной обструкции и нарушение энергетического метаболизма детрузора (митохондриальная недостаточность).
Подобное представление патогенеза расстройств мочеиспускания открывает широкие возможности для фармакотерапии. Сокращения и расслабления детрузора можно достичь с помощью средств метаболической терапии, прямого улучшения снабжения детрузора кислородом и т. д. Наиболее значимые расстройства основных функций мочевого пузыря все же опосредованы расстройствами кровообращения. И если процесс обратим, то до или после хирургического вмешательства можно существенно влиять на функциональное состояние мочевого пузыря с помощью вазоактивных препаратов, к которым в первую очередь относятся a1-адреноблокаторы.
При определении критериев отбора пациентов для медикаментозной терапии ДГПЖ мы воспользовались рекомендациями IV Международного консультативного комитета по ДГПЖ.
Основу настоящего исследования составили собственные клинические наблюдения за 1724 пациентами (средний возраст 61,4 года), страдающими ДГПЖ и получавшими различные варианты медикаментозного лечения. Нами применялись препараты всех групп, использующихся в настоящее время для лечения ДГПЖ: a-адреноблокаторы, блокаторы 5-a-редуктазы, препараты растительного происхождения и их комбинации. Схемы проведенного лечения и характеристика групп пациентов приведены в табл. 1.
Из наиболее многочисленной и популярной сегодня группы препаратов для медикаментозного лечения ДГПЖ — селективных a-адреноблокаторов мы использовали альфузозин, теразозин, доксазозин и тамсулозин. Общее число пациентов, получавших a-адреноблокаторы, составило 1408. Финастерид был взят нами как классический представитель блокаторов 5-a-редуктазы. Из препаратов растительного происхождения мы использовали пермиксон и таденан.
В пяти группах общей численностью 1305 человек проводилась терапия селективными a-адреноблокаторами в течение длительного периода времени по стандартным схемам и в стандартных дозах. Результаты лечения приведены в табл. 2.
Улучшение качества мочеиспускания отметили в среднем 86,74% пациентов. Суммарный балл I-PSS сократился на 38,68% к окончанию первого года лечения и на 43,4% к окончанию курса терапии. Балл QOL уменьшился на 29,04% и 35,58% соответственно. Максимальная скорость потока мочи увеличилась на 45,25% к окончанию первого года лечения и стабилизировалась на достигнутом уровне. Количество остаточной мочи сократилось в среднем на 57,6%. Процент пациентов, по тем или иным причинам выбывших из исследования, был тождествен во всех группах и равнялся 14,38%.
Особо следует остановиться на препарате тамсулозин (омник, Yamanouchi) — пока единственном простатселективном a1А-адреноблокаторе на отечественном рынке. Этот препарат обладает рядом свойств, которые позволяют его использовать в различных функциональных тестах. Прежде всего это возможность назначения единой терапевтической дозы (один раз в сутки по 0,4 мг). А отсутствие выраженного влияния на артериальное давление и сердечную деятельность избавляет от необходимости титрования дозы. Мы согласны с рядом авторов, которые считают возможным применение коротких курсов терапии тамсулозином в качестве прогностических тестов эффективности лечения a1-адреноблокаторами, что может иметь решающее значение при выборе того или иного метода медикаментозного лечения ДГПЖ [4].
Части больных (группа А5) проведена проверка возможности разрешения острой задержки мочеиспускания (ОЗМ) приемом альфузозина по 5 мг два раза в сутки. Эта терапия проводилась пациентам с впервые возникшей ОЗМ и отсутствием симптомов нарушения мочеиспускания в анамнезе. Положительный эффект был достигнут у 8 из 14 пациентов (57,1%), которым параллельно приему альфузозина производилось кратковременное (трое суток) дренирование мочевого пузыря катетером. Единовременный прием суточной дозы альфузозина (10 мг) способствовал восстановлению самостоятельного мочеиспускания лишь у одного из четырех пациентов, которым проводилась подобная терапия. Вероятно, это объясняется гипотонией детрузора, усугубляющейся в ситуации длительного перерастяжения мочевого пузыря на фоне задержки мочеиспускания.
Для изучения эффективности и безопасности комбинированной медикаментозной терапии ДГПЖ препаратами разных групп, а также для уточнения целесообразности проведения терапии нами были созданы три группы.
В первой группе (К1) пациенты получали проскар по 5 мг/сут. параллельно с приемом теразозина по 5-10 мг/сут. Обращало на себя внимание значительное повышение показателей максимальной скорости потока мочи (+40%), характерное для группы монотерапии a-адреноблокаторами, и постепенное, на протяжении курса лечения, снижение объема предстательной железы (-20,4%), характерное для группы монотерапии финастеридом. Очевидно, что положительные изменения показателей мочеиспускания в этой группе являются следствием воздействия обоих препаратов. Тем не менее процент выбывших пациентов в этой группе был крайне высоким — 32,3%. Основной причиной прекращения комбинированной терапии ДГПЖ пациенты называли неприемлемо высокую стоимость лечения.
В третьей группе комбинированной терапии (К3) лечение проводилось финастеридом по 5 мг/сут. в сочетании с пермиксоном по 160 мг два раза в сутки. Через два года после начала лечения 50% пациентов покинули группу, приводя причиной отказа от дальнейшей терапии высокую стоимость лечения при отсутствии быстрого улучшения качества мочеиспускания. При сравнении полученных данных с результатами в других группах очевидно, что эффективность лечения в третьей существенно ниже.
Таким образом, эффективность медикаментозной терапии больных ДГПЖ при соблюдении показаний и противопоказаний к ее назначению, правильном выборе препарата и схемы его назначения высока и достигает в среднем 80,2%. При этом эффективность монотерапии a-адреноблокаторами составляет 86,7%, блокаторами 5a-редуктазы — 69,4%, препаратами растительного происхождения — 69,3% и при комбинированной терапии — 95,45%. Комбинированная медикаментозная терапия a-адреноблокаторами в сочетании с блокаторами 5a-редуктазы эффективнее монотерапии этими препаратами. С целью снижения стоимости лечения возможен переход на монотерапию блокаторами 5a-редуктазы после достижения выраженного регресса обструктивной симптоматики. Медикаментозная терапия a-адреноблокаторами является эффективным способом консервативного лечения острой задержки мочеиспускания. Терапия должна проводиться на фоне кратковременного (трое суток) дренирования мочевого пузыря уретральным катетером.
Литература
1. Гориловский Л. М. Эпидемиология и факторы риска развития доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 10-18.
2. Лопаткин Н. А., Перепанова Т. С. Клинический опыт лечения больных доброкачественной гиперплазией предстательной железы a1-адреноблокатором альфузозином // Урол. и нефрол., 1997, № 5, с. 14-17.
3. Лоран О. Б., Вишневский Е. Л., Вишневский А. Е. Лечение расстройств мочеиспускания у больных доброкачественной гиперплазией простаты a-адреноблокаторами. Монография. М., 1998.
4. Сивков А. В. Медикаментозная терапия доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 67-83.
5. McConnell J. D. Prostatic growth: new insights into hormonal regulation // Br. J. Urol. 1995. Vol.76.(suppl.1). P. 5-10.
Доброкачественная гиперплазия предстательной железы — разрастание железистой ткани и стромы переходной зоны простаты, приводящее к увеличению органа. Аденома простаты может вызывать нарушения мочевыделения: слабую струю мочи, чувство неполного опорожнения мочевого пузыря, частые или ночные позывы, парадоксальную ишурию. Диагноз устанавливают по данным уровня ПСА, ТРУЗИ, урофлоуметрии и опросника оценки симптомов IPSS. Лечение коррелирует с объемом железы, возрастом, сопутствующей патологией и выраженностью симптомов: применяют тактику ожидания, медикаментозную терапию, оперативные вмешательства, включая малоинвазивные методики.
МКБ-10
Общие сведения
Доброкачественная гиперплазия предстательной железы (аденома простаты, ДГПЖ, ДГП) — общая мировая проблема, с которой сталкивается одна треть мужчин старше 50 лет и 90% пациентов, доживших до 85 лет. По статистике, около 30 млн. мужчин имеют мочеполовую дисфункцию, связанную с ДГПЖ, и эта цифра с каждым годом увеличивается. Патология чаще встречается у афроамериканцев с изначально более высоким уровнем тестостерона, активностью 5-альфа-редуктазы, ростовых факторов и экспрессии рецепторов андрогенов (популяционная особенность). У жителей восточных стран аденому простаты регистрируют реже, что, по-видимому, связано с употреблением в пищу большого количества продуктов, содержащих фитостеролы (рис, соя и ее производные).
Причины ДГПЖ
Патогенез
Тестостерон в организме мужчины содержится в различных концентрациях: в крови его уровень больше, в простате — меньше. У возрастных мужчин происходит снижение уровня тестостерона, но уровень дигидротестостерона остается высоким. Значимая роль принадлежит специфичному для простаты ферменту 5-альфаредуктазе, благодаря которой тестостерон переходит в 5-альфа-дигидротестостерон. К его действию максимально чувствительны андрогенные рецепторы и ДНК ядер клеток простаты, которые стимулируют синтез факторов роста и тормозят апоптоз (нарушение программируемых процессов естественного отмирания). В результате старые клетки живут дольше, а новые активно делятся, вызывая пролиферацию ткани и рост аденомы.
Увеличенная простата способствует затруднению мочеиспускания на фоне сужения простатической части уретры (особенно, если рост аденомы направлен внутрь мочевого пузыря) и повышению тонуса гладкомышечных волокон стромы. На начальной стадии патологии состояние компенсируется за счет усиленной работы детрузора, который напрягаясь, позволяет моче эвакуироваться полностью.
По мере прогрессирования появляются морфологические изменения стенки мочевого пузыря: часть мышечных волокон заменяется соединительнотканными. Емкость органа постепенно увеличивается, а стенки становятся тоньше. Слизистая оболочка также претерпевает изменения: типичны гиперемия, трабекулярная гипертрофия и дивертикулы, эрозивные изъязвления и некроз. При присоединении вторичной инфекции развивается цистит. Доброкачественная гиперплазия простаты и застой мочи приводят к обратному току урины, цистолитиазу, гидронефротической трансформации почек и ХПН.
Классификация
В андрологии принято несколько классификаций ДГПЖ. В зависимости от объема железы (его определяют с помощью УЗИ и измеряют в кубических сантиметрах) выделяют малую (до 25 см³), среднюю (26-80 см³), крупную (более 80 см³) и гигантскую аденому (свыше 250 см³). Классификация Гюйона выделяет три клинических стадии ДГПЖ:
Симптомы ДГПЖ
Симптомы зависят от степени обструкции мочеиспускательного канала. Если увеличенная простата сдавливает уретру, появляются жалобы на учащенное мочеиспускание малыми порциями, особенно, в ночные часы, вялую струю, ощущение неполного опорожнения, независимо от частоты мочеиспускания. По мере роста аденоматозных узлов изменяется иннервация, в результате чего возникают ургентные позывы — неконтролируемое желание помочиться с последующим неудержанием мочи.
На продвинутой стадии развивается парадоксальная ишурия — невозможность полностью помочиться с одновременным подтеканием мочи по каплям, что связано с атонией стенок мочевого пузыря, а также с детрузорно-сфинктерной диссинергией — отсутствием синхронной работы между мышцей, ответственной за изгнание урины, и расслаблением сфинктера мочеиспускательного канала. Чтобы опорожнить мочевой пузырь, некоторые мужчины вынуждены мочиться по женскому типу ‒ сидя. Клинические проявления доброкачественной гиперплазии предстательной железы непатогномоничны и могут сопровождать любую обструкцию, включая стриктуру уретры, дивертикул, опухоль и пр., поэтому только на основании оценки симптомов установить диагноз невозможно.
Осложнения
Осложнения гиперплазированной простаты могут включать ряд состояний. На фоне ДГП в 35% проявляется острая задержка мочеиспускания. Остаточная моча имеет свойство кристаллизироваться, в этом случае в мочевом пузыре формируются конкременты с вторичным воспалением. Повышенное внутрипузырное давление способствует образованию пузырно-мочеточниковых рефлюксов, гидронефроза и ХПН. Если рассматривать осложнения терапии аденомы предстательной железы, то существует вероятность развития стриктур уретры после трансуретральной резекции (5-7%), недержания мочи (1-2%), эректильной дисфункции (9-14%), ретроградной эякуляции (74-87%), шеечного склероза мочевого пузыря (2-4%).
Диагностика
Диагноз устанавливается урологом или андрологом. Ректальный осмотр информативен только при условии достижимого расположения опухоли. При пальцевом обследовании простата увеличена, однородна, безболезненна, консистенция ее эластична, срединная бороздка сглажена. Биопсия предстательной железы не является рутинным способом и показана только при подозрении на рак простаты. Пациенту с подозрением на нарушение функции почек необходима консультация нефролога.
Существует специальный опросник, разработанный для оценки степени выраженности симптомов обструкции нижних мочевыводящих путей. Анкета состоит из 7 вопросов, связанных с распространенными симптомами доброкачественной гиперплазии предстательной железы. Частота каждого симптома оценивается по шкале от 1 до 5. При суммировании получают общую оценку, которая влияет на дальнейшую тактику лечения (динамическое наблюдение, консервативная терапия или операция): от 0-7 — слабо выраженная симптоматика, 8-19 — средняя, 20-35 ‒ серьезная проблема с мочеиспусканием. Инструментальная и лабораторная диагностика при ДГПЖ включает:
Дифференциальную диагностику проводят с опухолевым процессом мочевого пузыря или простаты, цистолитиазом, травмой, интерстициальным и пострадиационным циститом, нейрогенным мочевым пузырем, стриктурой уретры, склерозом простаты, меатостенозом, клапанами уретры, фимозом, простатитом.
Лечение ДГПЖ
Терапия аденомы простаты коррелирует со степенью выраженности обструктивных симптомов и осложнений, на выбор тактики лечения влияет возраст пациента и сопутствующая патология. Все существующие способы лечения направлены на восстановление адекватной деривации мочи. Варианты терапии включают:
Прогноз и профилактика
Прогноз для жизни благоприятный, большинству пациентов достаточно длительного (пожизненного) приема современных лекарственных препаратов для нормализации функции мочеиспускания. Необходимость в операции возникает только у 15-20% мужчин. После аденомэктомии рецидив болезни не превышает 5%, малонивазивные методики не дают 100% гарантии исцеления и могут выполняться неоднократно. Улучшению прогноза в последнее десятилетие поспособствовало внедрение малоинвазивных методов лечения, что позволяет минимизировать осложнения, угрожающие жизни больных. Для нормализации эректильной функции необходима консультация андролога-сексолога.
Данные исследований по профилактике рака простаты показывают, что диета с низким содержанием животного жира и красного мяса и высоким содержанием белка и овощей может снизить риск симптоматической ДГПЖ. Физическая активность хотя бы 1 час в неделю на 34% уменьшает вероятность ноктурии.