Что такое дискодуральный конфликт 1 степени
Университет
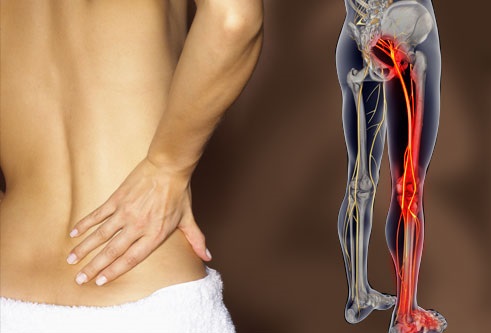
Часто от пациентов слышишь: мол, врачи лечили остеохондроз и радикулит, потом сделали МРТ/КТ позвоночника, а оказалось, что была грыжа межпозвонкового диска (МПД), и теперь будто бы спасет только операция. Неужели это единственный выход?
Мнений на сей счет много, поскольку проблемой занимаются врачи разных специальностей. Неврологи отговаривают от операции, мануальные терапевты гарантируют полное излечение, а нейрохирурги заявляют, что лишь они избавят от страданий, иначе могут наступить необратимые нарушения.
Какой метод лечения грыжы межпозвонкового диска лучше, какую грыжу оперировать открытым доступом, а в каких случаях — малоинвазивным? Особенно впечатляют фильмы, демонстрирующие малоинвазивные дорогостоящие вмешательства, к примеру, лазерную вапоризацию, после которой пациент полностью излечивается — его хоть сейчас отправляй в космос.
Для правильного понимания проблемы необходимо вспомнить основные моменты патогенеза заболевания.
Как вырастают грыжи межпозвонкового диска
Здоровый межпозвонковый диск состоит из замыкающих пластинок, фиброзного кольца, в центре которого находится пульпозное ядро — это очень прочное эластичное образование, способное выдерживать значительные нагрузки. Поэтому при травме позвоночника чаще наблюдаются переломы его, чем повреждения МПД. С годами развиваются дистрофические процессы (расстройство питания), они начинаются с межпозвонкового диска, переходят на другие элементы позвоночно-двигательного сегмента и определяются как остеохондроз позвоночника. Это хроническое мультифакторное рецидивирующее заболевание, генетическая предрасположенность к нему наблюдается в 80% людей. Важно отметить, что дегенерация (вырождение) диска и его естественное старение — это один процесс, но разноскоростной, осложняющийся грыжеобразованием. Ранняя возрастная изношенность позвоночника является выражением недостаточности биологического совершенства человека — как дань природе за переход в вертикальное положение.
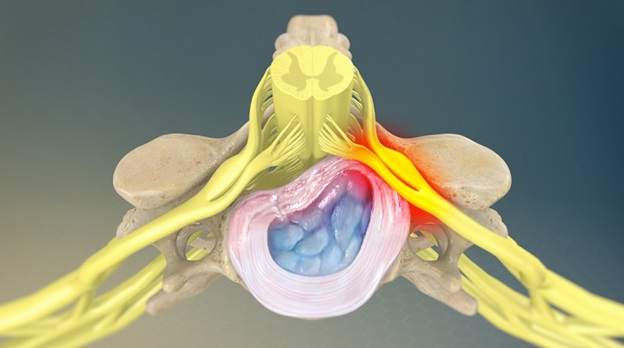
Вначале наблюдаются внутридисковые изменения (выпячивание) МПД, затем фиброзное кольцо не выдерживает нагрузки, и пульпозное ядро разрывает его, образуя истинную грыжу МПД (выпадение). Выпадения ядра могут иметь разные направления: кверху или книзу, так называемые грыжи Шморля (клинически малозначимые); кпереди; и самые неприятные — кзади, когда фрагменты ядра выпадают в эпидуральное пространство позвоночного канала и часто приводят к диско-радикулярному конфликту. При этом дегенеративный процесс распространяется и вверх, и вниз на другие МПД (наиболее часто на L4-L5, L5-S1, C5-C6, C6-C7) и даже отделы позвоночника — чаще поясничный, затем шейный (до 30%) и реже — грудной (менее 1%).

1 стадия: начальные дистрофические изменения в пульпозном ядре и задней части фиброзного кольца (рис. 1),
2 стадия: смещение (протрузия) пульпозного ядра кзади (рис. 2),
3 стадия: выпадение секвестров пульпозного ядра в позвоночный канал, где начинается его рассасывание или фиброз (рис. 3).
В «докомпьютерную эру» многие исследователи отмечали, что секвестр диска рассасывается, и этот процесс идет быстрее в васкуляризированном эпидуральном пространстве. Новые высокоразрешающие методы нейровизуализации позволили в динамике наблюдать за этим процессом. Первая порция выпавшего пульпозного ядра может на КТ значительно уменьшиться в размере в период ремиссии, но неудачное движение или перегрузка приводят к повторному выпадению другой порции ядра, вызывая обострение.
Поначалу нейрохирурги, удалявшие грыжи МПД, считали их доброкачественными опухолями-хондромами и не связывали патологию с МПД.
Помогли разобраться исследования Дрезденской школы патологоанатомов во главе с G. Schmorl (1926 г.). При посмертном анализе 5000 позвоночников людей разного возраста хрящевые узелки были обнаружены в 38% случаев (как правило, у лиц старше 50 лет). С этими результатами перекликаются и современные данные, полученные на добровольцах: в 50% КТ позвоночника и в 37% миелографий, выполненных населению всех возрастов, определялись выраженные патологические изменения МПД. И пациенты не имели никаких жалоб. Чем старше больной, тем чаще на КТ/ МРТ проявлялся остеохондроз позвоночника, а в пожилом возрасте (>60 лет) он наблюдается в 100% случаев.
Что делать при грыже 10 мм, если консервативное лечение малоэффективно
Вопрос поставлен конкретно, но однозначно ответить нельзя. Понятно, что уже необходима хирургическая помощь.
В Беларуси используются несколько методик хирургического лечения грыж межпозвонкового диска.
Чрескожное малоинвазивное удаление грыж. Это попытка добиться устранения диско-радикулярного конфликта с минимальной травматизацией позвоночника, не нарушая его стабильности. При чрескожных операциях, когда уменьшают (выпаривают) или механически удаляют пульпозное ядро (не вскрывая позвоночный канал) для снижения внутридискового давления. Невозможно воздействовать на выпавшие секвестры грыжи МПД. Поэтому показания для этих вмешательств — грыжи менее 6 мм (см. «Медицинский вестник» от 12.02.2009 № 7, ‘ГРЫЖА И «СТО» ДОРОГ НЕЙРОХИРУРГА, Чреcкожные методики лечения грыж межпозвонкового диска (МПД)’). Считается, что при таком размере фиброзное кольцо полностью не разорвалось и процесс формирования грыжи находится на 1–2 стадиях.
При грыже более 10 мм подходят другие хирургические технологии. Сейчас их известно уже более сотни, и появляются новые.
Стандартная микродискэктомия. Ее называют золотым стандартом нейрохирургического лечения грыж МПД. Удаляются выпавшая часть и остатки пульпозного ядра в МПД. При остром развитии болезни (пациенты отмечают, будто что-то «хрустнуло», «стрельнуло» в спине) у лиц среднего и молодого возраста результаты лечения хорошие. Хотя операция и с минимальной травматизацией ткани (разрез кожи у опытных нейрохирургов составляет 2–3 см), она все же усугубляет дегенеративно-дистрофический процесс в оперируемом МПД и уменьшает его высоту, в результате не всегда достигается прогнозируемый результат. Чтобы сохранить функциональные возможности МПД после удаления грыжи, предлагалось зашивать рану фиброзного кольца. Специально разработали новую операцию — аннулопластику (J. Cauthen, 2002). Однако она оказалась неэффективной из-за больших нагрузок и низкого регенерационного потенциала фиброзного кольца; вновь наблюдались рецидивы грыжи.
Результаты стандартной микродискэктомии ухудшаются из-за возраста пациентов, большой длительности заболевания, повторных микродискэктомий на том же уровне; улучшаются — проявлениями остеохондроза только на одном уровнем, удаление больших грыж МПД (> 6 мм по данным КТ).
Показания к стандартной микродискэктомии разработаны давно и основаны на неврологических проявлениях грыж. Делятся на относительные и абсолютные. В отношении абсолютных показаний к стандартной микродискэктомии все авторы единодушны: компрессия конского хвоста, некупируемый выраженный болевой приступ или явления миелорадикулоишемии с параличом отдельных групп мышц (подобно острому животу) требуют срочного вмешательства. А вот оправданность микродискэктомий при относительных показаниях признается не всеми (Я. Ю. Попелянский, 2003; Е. Л. Толпекин, Ф. В. Олешкевич, 2006).
Эпидурохемонуклеолизис. Адресное пролонгированное лечение комплексом лекарств (бупивакаин, лидаза, вит. В12) по катетеру, поставленному через нижнее крестцовое отверстие в эпидуральное пространство, под Rtg-контролем. Методика позволяет доставлять лекарства непосредственно к зоне диско-радикулярного конфликта, не нарушая целостности анатомических структур. Критерием эффективности является уменьшение размера грыжи при контрольных КТ-обследованиях. При анализе результатов лечения по данной технологии выявлено, что лучшие получены при грыжах более 6 мм, когда имеется разрыв фиброзного кольца и задней продольной связки, и лидаза непосредственно воздействует на секвестры грыж МПД.
Основываясь на фактах патогенеза заболевания, приведенных выше результатах лечения, нельзя утверждать, что размеры грыж МПД являются основополагающим фактором для показаний к оперативному лечению. Нет четкой корреляции между размерами грыжи и выраженностью неврологических проявлений, и, наоборот, при остроразвившейся некупируемой боли в пояснице с выраженной клинической картиной радикулопатии, в большинстве случаев мы находим большие по размерам грыжи МПД.
Кто рассудит нейрохирурга и ортопеда
Задние грыжи межпозвонкового диска — это патология опорно-двигательного аппарата и периферической нервной системы, поэтому в принципах оказания хирургической помощи имеются две позиции — нейрохирургов и ортопедов.
Большинство нейрохирургов считают, что основная причина страданий — в компрессии нервных структур, вызванной грыжей МПД, а ее оперативное удаление — залог выздоровления.
Других позиций придерживаются ортопеды, обращая основное внимание на дегенеративно-дистрофический процесс в МПД, поэтому направляют свои усилия на восстановление правильных анатомических взаимоотношений в позвоночно-двигательном сегменте.
Идеальным решением проблемы явилось бы не только устранение диско-радикулярного конфликта, но и восстановление функции и высоты МПД. Пока это не достижимая цель. Нерешенным остается и хирургическое лечение при многоуровневых поражениях.
В последние десятилетия на стыке этих дисциплин сформировалась новая наука — вертеброневрология.Конференции и симпозиумы на эту тему созываются чуть ли не ежегодно. В 1992 г. на советско-американском симпозиуме по поводу лечения остеохондроза позвоночника американский вертеброневролог A. White отмечал, что эффективность лечения таких больных зависит от качества совместной работы многопрофильных «спинальных» бригад, в состав которых должны входить терапевт, хирург, психиатр, рентгенолог, физиотерапевт. Ведущим врачом бригады должен быть не хирург, а специалист, лучше знающий больного, его психосоциальный статус, условия труда, материальные обстоятельства, реабилитационный ресурс. Такой доктор взял бы на себя ответственность в принятии решения по хирургическому лечению, пред- и после-операционному ведению. В нашей стране решение этой проблемы лежит в создании центров вертеброневрологии, где пациенты могли бы получить экстренную и плановую помощь всех специалистов, работающих в этой области. Больным с болями в спине не пришлось бы по несколько раз обращаться к неврологу (терапевту) в поликлинику, затем ждать КТ/МРТ обследования, что значительно увеличивает дооперационный период.
В клинике неврологии и нейрохирургии БГМУ разработана и внедрена методика поэтапного лечения пациентов с неврологическими проявлениями остеохондроза позвоночника по принципу нарастания радикализма:
1. лечебные паравертебральные блокады с гормональными и ферментными препаратами, или транссакральный эпид-урохемонуклеолизис;
2. стандартная микродискэктомия с эндоскопической ассистенцией;
3. стандартная микродискэктомия + эпидурохемонуклеолизис (при многоуровневой патологии);
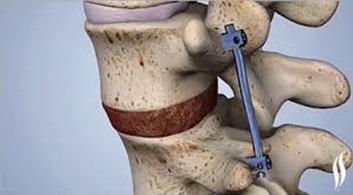
4. стандартная микродискэктомия + динамическая стабилизация позвоночника U-имплантантом (при выраженной динамической нестабильности и повторных операциях).
Евгений ТОЛПЕКИН, врач-нейрохирург, кандидат мед. наук
Медицинский вестник, 26 ноября 2009
Корешковый синдром поясничного отдела
Причины
Любые морфологические образования или патологические процессы, которые приводят к компрессионному воздействию на нервный корешок, могут стать причиной корешкового синдрома.
Основными причинами поясничной радикулопатии являются:
У пациентов моложе 50 лет наиболее частой причиной корешкового синдрома в поясничном отделе позвоночника является грыжа межпозвоночного диска. После 50 лет корешковая боль часто вызвана дегенеративными изменениями позвоночника (стеноз межпозвоночного отверстия).
Факторы риска развития поясничной радикулопатии:
Симптомы
Симптомы, возникающие в результате корешкового синдрома (радикулопатии), локализуются в зоне иннервации конкретного корешка.
Паттерны боли
Начало появления симптомов у пациентов с пояснично-крестцовой радикулопатией (корешковым синдромом) часто бывает внезапным и включает боль в пояснице.
Сидение, кашель или чихание могут усугубить боль, которая распространяется от ягодицы по задней поверхности голени, лодыжки или стопы.
Необходимо быть бдительным при наличии определенных симптомов (красных флажков). Такие красные флажки могут означать более тяжелое состояние, требующее дальнейшего обследования и лечения (например, опухоль, инфекция). Наличие лихорадки, потери веса или ознобов требует тщательного обследования.
Возраст пациента также является фактором при поиске других возможных причин симптоматики у пациента. Лица моложе 20 лет и старше 50 лет подвержены повышенному риску возникновения более серьезных причин боли (например, опухоли, инфекции).
Диагностика
Первичный диагноз корешкового синдрома пояснично-крестцового отдела позвоночника выставляется на основании симптоматики истории болезни и данных физического обследования (включая тщательное изучение неврологического статуса). Тщательный анализ моторной, сенсорной и рефлекторной функций позволяет определить уровень поражения нервного корешка.
Если пациент сообщает о типичной односторонней иррадиирущей боли в ноге и есть один или несколько положительных результатов неврологического теста, то тогда диагноз радикулопатии очень вероятен.
Тем не менее, существует ряд состояний, которые могут проявляться схожими симптомами. Дифференциальную диагностику необходимо проводить со следующими состояниями:
Для постановки клинически достоверного диагноза, как правило, требуются инструментальные методы диагностики:
Лечение
Лечение корешкового синдрома пояснично-крестцового отдела позвоночника будет зависеть от тяжести симптоматики и клинических проявлений. Чаще всего, используется консервативное лечение, но в определенных случаях бывает необходимо хирургическое лечение.
Консервативное лечение:
Иглорефлексотерапия. Этот метод широко используется в лечении корешкового синдрома в пояснично-крестцовом отделе позвоночника и помогает как снизить симптоматику в остром периоде, так и входит в комплекс реабилитации.
Хирургическое лечение
Оперативные методы лечения корешкового синдрома в пояснично-крестцовом отделе позвоночника необходимы в тех случаях, когда есть устойчивость к консервативному лечению или имеются симптомы, свидетельствующие о выраженной компрессии корешка такие как:
Некоторые хирургические процедуры, используемые для лечения поясничной радикулопатии:
Прогноз
В большинстве случаев удается лечить корешковый синдром в пояснично-крестцовом отделе позвоночника консервативно (без хирургического вмешательства) и восстановить трудоспособность. Продолжительность лечения может варьироваться от 4 до 12 недель в зависимости от тяжести симптомов. Пациентам обязательно необходимо продолжать в домашних условиях выполнять упражнения для улучшения осанки, а также на растяжение, усиление и стабилизацию. Эти упражнения необходимы для лечения состояния, вызвавшего корешковый синдром.
Сравнительный анализ клинической эффективности минимально инвазивных хирургических методик при лечении пациентов с диcко-радикулярным конфликтом поясничного отдела позвоночника
Введение
Материал и методы
В исследование включены 315 пациентов, которым в Центре нейрохирургии НУЗ «Дорожная клиническая больница на ст. Иркутск-Пассажирский» ОАО РЖД в период с 2010 по 2016 г. выполнены оперативные вмешательства. Исследование одобрено этическим комитетом ФГБОУ ВО «Иркутский государственный медицинский университет» (протокол №3 от 19.12.14).
Предварительно для подтверждения компрессионного характера клинических проявлений использовались пункционные диагностические методики.
В полость МПД вводили 5—10 мл физиологического раствора и йодсодержащего водорастворимого контрастного вещества (Ультравист, Германия), при усилении корешковой симптоматики инвазивный тест считали положительным.
В качестве критериев включения в исследование и исключения из него использованы показания и противопоказания к осуществлению малоинвазивного оперативного лечения ДРК на поясничном уровне.
Критерии включения:
— стойкий корешковый болевой синдром с сенсорными расстройствами в течение 6—8 нед, не купирующийся эпидуральными инъекциями стероидных гормонов;
— наличие, по данным нейровизуализации, клинически значимой парамедианной и парафораминальной грыжи или протрузии МПД размером до 6 мм, сужающей межпозвонковые отверстия;
— уровень поражения LIII—LIV, LIV—LV.
Критерии исключения:
— острый неврологический дефицит, требующий экстренного реконструктивного вмешательства, например каудальный синдром;
— наличие медианной грыжи или протрузии МПД, по данным нейровизуализации, более 6 мм, в том числе секвестрированной;
— уровень поражения LI—LII, LII—LIII, LV—SI;
— клинико-рентгенологические признаки сегментарной нестабильности (сагиттальная ангуляция более 10°, линейная трансляция более 4 мм);
— центральный стеноз позвоночного канала;
— предшествующие операции на позвоночнике.
Пациенты оперированы с помощью оригинального инструментария одной хирургической бригадой. Все операции выполнялись под местной анестезией в положении пациента лежа на животе с разгрузочными валиками. Общим при выполнении ЗБЭД и ПМН декомпрессором являлась рабочая зона в области передних отделов треугольника Камбина. Ее анатомическими ориентирами служили выходящий из межпозвонкового отверстия корешок, формирующий переднелатеральную границу; твердая мозговая оболочка дурального мешка — медиальная граница. Триангулярная зона свободна от нервно-сосудистых структур, спинномозговой корешок располагается под вышележащим корнем дуги, поэтому вероятность его повреждения минимальна. Интраоперационно при помощи электронно-оптического преобразователя верифицировали уровень пораженного МПД.
Выделены две группы исследования: в 1-й выполнялась ЗБЭД (n=163), во 2-й — ПМН декомпрессором (n=152). ЗБЭД осуществлялась по общепринятой методике: место введения пункционной иглы располагалось на 9—12 см латеральнее срединной линии к МПД под углом 50—65° по отношению к дугоотростчатому суставу. После верификации положения иглы в МПД осуществлялась дискография. Далее выполнялись дилатация входа в МПД при помощи обтуратора, аннулотомия и дискэктомия с эндоскопическим контролем (рис. 1).
Во 2-й группе выполнялась ПМН декомпрессором классическим способом: игла вводилась под углом 35—50° к поверхности тела пациента во фронтальной плоскости, отступя на 8—12 см от средней линии. После пункции МПД проводилась дискография. После извлечения мандрена в канюлю устанавливался декомпрессор, который включался нажатием переключателя на корпусе. Осуществляли продвижение декомпрессора поступательными движениями от места введения в МПД до контралатеральной стороны фиброзного кольца. После окончания операции декомпрессор выводился из полости МПД, а экстрагированные части пульпозного ядра удалялись из рабочей части декомпрессора и накопительной колбы (рис. 2).
Пациентам, включенным в исследование, проводился комплексный дооперационный клинический и инструментальный анализ: поясничная спондилография в двух проекциях и с функциональными пробами в вертикальном положении, нейровизуализационный (магнитно-резонансная томография — 1,5 Т Magnetom Siemens Essenzal; мультиспиральная
компьютерная томография — Bright Speed Edge (4 спирали) («General Electric», США)) и нейрофизиологический (стимуляционная электронейромиография нижних конечностей) методы исследования.
После операции катамнез наблюдения составил минимум 30 и максимум 70 мес, медиана — 48 мес. Для сравнительного анализа исследовали пол, возраст, индекс массы тела, продолжительность операции, время активизации, длительность стационарного лечения, клинические параметры (уровень болевого синдрома по ВАШ, функциональное состояние по индексу ODI, субъективную удовлетворенность исходом операции по шкале Macnab), послеоперационные осложнения.
Статистическая обработка результатов исследования проведена с использованием Microsoft Excel и Statistica 8.0. Для оценки значимости различий выборочных совокупностей использовались критерии непараметрической статистики, в качестве нижней границы достоверности принят уровень статистической достоверности p 0,5) (рис. 3).
Рис. 3. Динамика болевого синдрома по ВАШ (0—100 мм) в исследуемых группах до операции, при выписке, через 12, 24, 36 и 48 мес после операции (данные представлены медианой и интерквартильным размахом в виде Me (25%; 75%)).
Сравнение значений ODI показало значимую положительную динамику функционального состояния после операции по сравнению с дооперационным уровнем в обеих группах: в 1-й — с 74 (68; 80) до 30 (24; 42) баллов при выписке и до 26,5 (19; 31) балла в среднем через 48 мес (pW 0,5) (рис. 4).
Рис. 4. Динамика качества жизни пациентов по индексу ODI (0—100) в исследуемых группах до операции, при выписке, через 12, 24, 36 и 48 мес после операции.
Данные представлены медианой и интерквартильным размахом в виде Me (25%; 75%).
При анализе отдаленных результатов лечения посубъективной шкале оценки удовлетворенности Macnab в среднем через 48 мес после операции в обеих группах отмечены отличные и хорошие результаты: у 52 (32%) и 93 (57%) пациентов соответственно в 1-й группе, 46 (29%) и 97 (62%) — соответственно во 2-й группе, неудовлетворительных результатов не зарегистрировано.
После проведения лечения ДРК с использованием пункционных методик осложнения составили в 1-й группе 5 (3,1%) случаев: инфицирование послеоперационной раны (2), спондилодисцит (1), прогрессирование дегенеративных изменений МПД (1), рецидив болевого синдрома менее чем через 1 мес (1); во 2-й группе 6 (3,8%) случаев: клинически подтвержденное повреждение спинномозгового корешка (1), инфицирование послеоперационной раны (1), спондилодисцит (1), прогрессирование дегенеративных изменений МПД (2), рецидив болевого синдрома менее чем через 1 мес (1). В этих случаях проведение дополнительного курса консервативного лечения способствовало стойкому клиническому улучшению. При анализе установлен низкий риск развития неблагоприятных осложнений, что подтверждает безопасность использованных хирургических методик.
Что такое дискодуральный конфликт?
Дискодуральный конфликт. Что это?
Дискодуральный конфликт – это конфликт между диском (межпозвонковый диск) и дурой (по-латински это твердая мозговая оболочка) – диск прикрепляется к твердой мозговой оболочке.
Разберем сегодня следующие вопросы:
что такое дискодуральный конфликт
Почему возникает боль?
3) Профилактика образования грыж
Твердая мозговая оболочка (ТМО) – это некий чулок, в котором находится наш головной и спинной мозг. Эта оболочка в норме вольно движется относительно
Боль, которая расходится по нервам и может отдавать до кончиков пальцев! А может болеть локально – плечо, бедро, колено. Однако нервы иннервируют не только руки и ноги, они иннервируют все, включая внутренние органы, и если нервы раздражаются прилипшей твердой мозговой оболочкой, то к органам приходят, так сказать, неправильные импульсы, и органы начинают работать не так как необходимо или, например, соответствующие мышцы становятся слабее, но до какого-то момента человек этого может и не замечать. Нередко болезнь начинается в месте залипания в спине (где-то на уровне одного из позвонков), и отдает дальше по ходу нервов в верхнюю или нижнюю конечность.
Если ТМО прилипает на уровне шеи, то как правило дает о себе знать плечо, лопатка, рука. Не считая боли или слабости часто бывает онемение части предплечья или пальцев. Если на уровне поясницы, то все то же самое происходит с ногами.
В процессе работы с дискодуральным конфликтом прилипшие места освобождаются, болевые ощущения исчезают, нормальная иннервация восстанавливается. Время от времени сопровождается недолгим обострением (1-2 дня), однако потом все проходит само и становится значительно легче, чем было ранее. Бывает, что человек испытывает дискомфорт годами и после разрешения диско-дурального конфликта получают облегчение, это похоже на фантастику! Преимущество техники, которую я применяю, в абсолютной безопасности для человека, все очень плавно постепенно.
Не считая непосредственно техники решения дискодурального конфликта можно применять и специальные упражнения – отлично подходят все виды сгибаний и прогибов, к примеру комплекс 5 тибетцев (технику исполнения легко отыскать на ютуб) или любые другие подобные.