Что такое дифильное строение
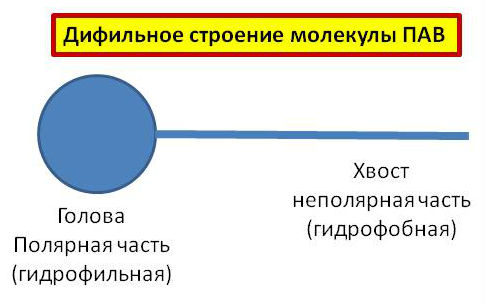
Молекулы поверхностно-активных веществ (ПАВ) обладают дифильным строением. Это значит, что одновременно они содержат полярную группу (голову) и неполярный углеводородный радикал (хвост).
Способность вещества концентрироваться на границе раздела фаз называется адсорбцией.
Радикалом в нашем случае является этил С2 H 5. Он представляет собой хвост, т.е. неполярную часть молекулы ПАВ. Полярной частью молекулы ПАВ является функциональная группа. В нашем случае это гидроксильная группа, определяющая принадлежность данного соединения к классу спиртов.
Таким образом, молекулы воды сильнее взаимодействуют друг с другом, чем между водой и неполярными углеводородными радикалами. В этом случае энергетически выгодным будет переход радикала в неполярную фазу. Молекулы воды выталкивают углеводородный радикал в аналогичную по полярности фазу. А переход полярной группы в неполярную фазу энергетически невыгоден, т.к. нужно еще затратить дополнительную энергию на гидратацию.
Таким образом, если рассмотреть раствор хлорида натрия в воде, то ионы натрия и хлора сильнее втягиваются в водную фазу, чем молекулы воды,т.к. ион-дипольное взаимодействие в этом случае сильнее, чем у молекул воды между собой (диполь-дипольное взаимодействие). В результате чего поверхностный слой насыщается водой, а хлорид натрия уходит в объем.
Поверхностно неактивные вещества (ПНВ) не концентрируются, поэтому А=0. ПНВ называют неадсорбирующимися веществами.
Поверхностная активность характеризует способность растворенного вещества адсорбироваться на границе раздела фаз. Адсорбируются вещества неодинаково. Для оценки способности веществ к адсорбции существует эмпирическое правило Дюкло-Траубе, которое формулируется следующим образом:
в гомологических рядах ПАВ при удлинении углеводородного радикала на величину гомологической разности поверхностная активность возрастает в 3,2 раза.
Поверхностно-активные вещества (ПАВ). Мыла
Органические вещества, снижающие поверхностное натяжение вследствие адсорбции на границе раздела фаз, называют поверхностно-активными веществами (ПАВ). Поверхностно-активные вещества имеют дифильное строение, т. е. состоят из полярной группы (—СООН, —COONa, —SО3Na, —ОН, —NH2 и др.) и неполярного углеводородного радикала C10—C18 (обычно линейного строения).
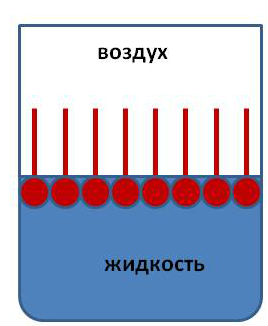
УВ радикал обладает поверхностной активностью в отношении неполярной фазы (газ, углеводородная жидкость, хлор, неполярная поверхность твердого тела) и выталкивается из полярной среды. В водном растворе ПАВ на границе с воздухом образуется адсорбционный слой с УВ радикалами, ориентированными в сторону воздуха. Концентрация ПАВ в этом слое выше, чем в объеме жидкости, поэтому ПАВ снижают поверхностное натяжение воды на границе с воздухом.
Уменьшение поверхностного натяжения воды увеличивает ее смачивающую способность и моющее действие.
По характеру гидрофильных и гидрофобных групп ПАВ можно разделить на 3 группы: анионоактивные (анионные), катионоакивные (катионные), неионогенные.
В катионных ПАВ поверхностную активность в водных растворах обеспечивают большие органические катионы. К катионным ПАВ относятся аминосоединения, аммониевые, сульфониевые и фосфониевые соединения. Наиболее известными являются соли четырехзамещенного аммония, диссоциирующие в водных растворах следующим образом:
где R — углеводородный радикал, содержащий 12—18 углеродных атомов, а Rl, R1, R3 — короткие радикалы (—СН3, —С2Н5).
Неионогенные ПАВ в водных растворах не диссоциируют на ионы. Такими веществами могут быть, например, соединения типа:
Наиболее часто используемыми в промышленности и в быту являются анионоактивпые ПАВ. В водных растворах этих ПАВ носителем поверхностно-активных свойств являются длинноцепочные анионы. Катионы влияют лишь на растворимость этих веществ.
К анионоактивным ПАВ относятся, в частности, давно используемые в качестве моющих средств мыла.
Жидкие калиевые мыла и твердые натриевые мыла получают растворением высших алифатических кислот в водных растворах едких щелочей:
Моющее действие (т. е. способность моющих средств и их растворов удалять с отмываемых поверхностей прилипшие частицы грязи и переводить их во взвешенное состояние в виде эмульсий и суспензий) мыл в жесткой воде сильно падает вследствие образования нерастворимых кальциевых и магниевых мыл:
Растворение мыла в воде сопровождается частичным гидролизом с образованием высшей кислоты и щелочи, которая оказывает вредное действие на многие ткани:
Синтетические моющие средства (СМС) — детергенты — не обладают отмеченными недостатками, характеризуются более высокой моющей способностью, доступностью сырья для их производства. Основой СМС являются синтетические ПАВ. Это могут быть и катионоактивные, и неионогенные ПАВ. Однако главным компонентом большинства СМС являются анионоактивные синтетические ПАВ. Рассмотрим важнейшие из них.
Алкилсульфонаты RSО3Na обладают высокой эмульгирующей и смачивающей способностью.
Способы получения
1.Сульфохлорирование предельных УВ (C12—C16) с последующим омылением алкилсульфохлорида:
2.Сульфоокисление предельных УВ и нейтрализация полученной алкансульфокислоты:
3.Присоединение гидросульфита натрия к алкенам:
Алкиларилсульфонаты химически устойчивы, сравнительно дешевы и эффективны.
Синтез осуществляется в две стадии:
Алкилсульфаты R – O – SO2 – ONa дают обильную пену.
Способы получения
1.Этерификация высших алифатических спиртов серной кислотой с последующей нейтрализацией образующихся кислых сложных эфиров:
2.Присоединение H2SО4 к алкенам и нейтрализация образовавшихся кислот:
СМС очень медленно разлагаются, вредные результаты их воздействия на природу и живые организмы непредсказуемы. Перевод ПАВ в пену, адсорбция активным углем, нейтрализация катионактивными веществами и др. недостаточно эффективны и очень дороги. Поэтому предпочтительна очистка сточных вод от ПАВ в отстойниках и в естественных условиях (в водоемах) путем биологического окисления под действием гетеротрофных бактерий, которые входят в состав активного ила. Процесс идет до превращения органических веществ в углекислый газ и воду. При биохимической очистке окисление ведется в присутствии ферментов. Микробиологический метод основан на использовании высокоактивных культур микроорганизмов. Получены штаммы бактерий, разрушающих алкилсульфаты, алкилсульфонаты, алкилбензолсульфонаты и др.
главная > справочник > химическая энциклопедия:
Поверхностно-активные вещества
Поверхностно-активные вещества (ПАВ), вещества, адсорбция которых из жидкости на поверхности раздела с другой фазой (жидкой, твердой или газообразной) приводит к значит. понижению поверхностного натяжения (см. Поверхностная активность). В наиболее общем и важном с практической точки зрения случае адсорбирующиеся молекулы (ионы) ПАВ имеют дифильное строение, т. е. состоят из полярной группы и неполярного углеводородного радикала (дифильные молекулы). Поверхностной активностью в отношении неполярной фазы (газ, углеводородная жидкость, неполярная поверхность твердого тела) обладает углеводородный радикал, который выталкивается из полярной среды. В водном растворе ПАВ на границе с воздухом образуется адсорбционный мономолекулярный слой с углеводородными радикалами, ориентированными в сторону воздуха. По мере его насыщения молекулы (ионы) ПАВ, уплотняясь в поверхностном слое, располагаются перпендикулярно поверхности (нормальная ориентация).
В зависимости от состояния ПАВ в растворе условно различают истинно растворимые (молекулярно-диспергированные) и коллоидные ПАВ. Условность такого разделения состоит в том, что одно и то же ПАВ может относиться к обеим группам в зависимости от условий и хим. природы (полярности) растворителя. Обе группы ПАВ адсорбируются на фазовых границах, т. е. проявляют в растворах поверхностную активность, в то время как объемные свойства, связанные с возникновением коллоидной (мицеллярной) фазы, проявляют лишь коллоидные ПАВ. Указанные группы ПАВ отличаются значением безразмерной величины, которая наз. гидрофильно-липофильным балансом (ГЛБ) и определяется отношением:
В нач. 60-х гг. 20 в. Д. Девисом была разработана шкала ГЛБ со значениями от О до 40. ПАВ с липофильными свойствами имеют низкие значения ГЛБ, с гидрофильными-высокие. Каждой группе атомов, входящей в молекулу ПАВ, приписывается групповое число. При сложении этих чисел получают ГЛБ по формуле:
ГЛБ = 

Хотя понятие о ГЛБ является достаточно формальным, оно позволяет определять области применения ПАВ. Так, для образования эмульсий вода/масло ГЛБ лежит в пределах 3-6, эмульсий масло/во да-8-16, для смачивателей-7-9, для моющих средств-13-15.
Поверхностная активность ПАВ, относящихся к разным группам, определяется по-разному. Для истинно растворимых ПАВ она равна макс. значению производной
Классификация ПАВ. В данной статье описывается классификация, принятая на III Международном конгрессе по ПАВ и рекомендованная Международной организацией по стандартизации (ISO)в 1960. Она основана на хим. природе молекул и включает четыре основного класса ПАВ: анионактивные, катионактивные, неионогенные и амфотерные. Иногда выделяют также высокомолекулярные (полимерные), перфторированные и кремнийорганические ПАВ, однако по химической природе молекул эти ПАВ м. б. отнесены к одному из вышеперечисленных классов.
Анионактивные ПАВ содержат в молекуле одну или несколько полярных групп и диссоциируют в водном растворе с образованием длинноцепочечных анионов, определяющих их поверхностную активность. Это группы: COOH(M), OSO 2 OH(M), SO 3 H(M), где M-металл (одно-, двух- или трехвалентный). Гидрофобная часть молекулы обычно представлена предельными или непредельными алифатическими цепями или алкилароматическими радикалами. Выделяют 6 групп анионактивных ПАВ.
1) Производные карбоновых кислот (мыла): RCOOM, ROOC (СН 2 ) n СООМ, RC 6 H 4 (СН 2 ) n СООМ, RCH=CH — —(СН 2 ) n СООМ. 2) Первичные и вторичные алкилсульфаты ROSO 3 M, R’R:CHOSO 3 M, алкиларилэтилсульфаты RC 6 H 4 C 2 H 4 OSO 3 M, алкилциклогексилэтилсульфаты RC 6 H 10 C 2 H 4 OSO 3 M и т.п. (см. Авироль, Ализариновое масло, Алкилсульфаты). 3)Алкил- и алкилбензолсульфонаты, сульфонаты сложных эфиров моно- и дикарбоновых кислот: RSO 3 M, RC 6 H 4 SO 3 M, ROOCCH 2 SO 3 M, ROOCCH 2 CH(COOR)SO 3 M (см. Алкилбензолсульфонаты, Нафталинсульфонаты, Сульфонаты). 4) Сульфо- и карбоксиэтоксилаты спиртов, сульфоэтоксилаты карбоновых кислот, сульфоэтоксилаты алкилфенилэтиловых спиртов, диметал-лич. соли сульфоянтарной кислоты, соли сульфатов непредельных кислот: RO(C 2 H 4 O) n SO 3 M, RO(C 2 H 4 O) n CH 2 COOM, RCOO (C 2 H 4 O) n SO 3 M, RC 6 H 4 (C 2 H 4 O) 2 SO 3 M, ROOCCH 2 CH •(COOM) SO 3 M, RCH (OSO 3 M)=CH (CH 2 ) n —COOM. 5) Азотсодержащие ПАВ: амидосульфонаты RCONR’—R:—SO 3 M, амиды сульфокарбоновых кислот RR’NOC—R:—SO 3 M, амидосульфаты RCONR’- R:—OSO 3 M, амидокарбоксилаты RCO(NH-R’—CO) n OM, вещества с карбокси- и сульфогруппами RCONH—R—OCOR:(SO 3 M) —COOM. Вместо амидной группы во мн. таких веществах м.б. также сульфоамидная группа, например RC 6 H 4 SO 2 NHCH 2 CH 2 SO 3 M. 6) Соли перфторир. карбоновых кислот, перфторир. сульфоацетатов, моно- и диалкил-фосфатов и фосфонатов, перфторир. фосфонаты и др. соединения.
Наиб. распространены алкилсульфаты и алкиларилсуль-фонаты. Оптим. поверхностно-активными свойствами обладают первичный додецилсульфат и прямоцепочечный доде-цилбензолсульфонат. Эти вещества термически стабильны, малотоксичны (ЛД 50 1,5-2 г/кг, белые мыши), не раздражают кожу человека и удовлетворительно подвергаются биол. распаду в водоемах (см. ниже), за исключением алкиларил-сульфонатов с разветвленной алкильной цепью. Они хорошо совмещаются с др. ПАВ, проявляя при этом синергизм, порошки их негигроскопичны. Вторичные алкилсульфаты обладают хорошей пенообразующей способностью, но термически неустойчивы и применяются в жидком виде. Вторичные алкилсульфонаты обладают высокой поверхностной активностью, но весьма гигроскопичны. Перспективными являются ПАВ, у которых гидрофильная часть состоит из неск. функц. групп. Напр., динатриевые соли сульфоянтарной кислоты обладают хорошими санитарно-гигиенич. свойствами наряду с высокими коллоидно-хим. и технол. показателями при растворении в жесткой воде. ПАВ, содержащие сульфониламидную группу, обладают биол. активностью. Хорошими свойствами обладает также додецил-фосфат.
Катионактивные ПАВ меньше снижают поверхностное натяжение, чем анионактивные, но они могут взаимодействовать химически с поверхностью адсорбента, например с клеточными белками бактерий, обусловливая бактерицидное действие. Взаимодействие полярных групп катионактивных ПАВ с гидроксильными группами волокон целлюлозы приводит к гидрофобизации волокон и импрегнированию тканей.
Амфотерные (амфолитные) ПАВ содержат в молекуле гидрофильный радикал и гидрофобную часть, способную быть акцептором или донором протона в зависимости от рН раствора. Обычно эти ПАВ включают одну или несколько основных и кислотных групп, могут содержать также и неионогенную полигликолевую группу. В зависимости от величины рН они проявляют свойства катионактивных или анионактивных ПАВ. При некоторых значениях рН, наз. изоэлектрической точкой, ПАВ существуют в виде цвиттер-ионов. Константы ионизации кислотных и основных групп истинно растворимых амфотерных ПАВ весьма низки, однако чаще всего встречаются катионно-ориентированные и анионно-ориентированные цвиттер-ионы. В качестве катионной группы обычно служит первичная, вторичная или третичная аммониевая группа, остаток пиридина или имидазолина. В принципе вместо N м. б. атомы S, P, As и т. п. Анионными группами являются карбоксильные, сульфонатные, сульфоэфирные или фосфатные группы.
По хим. строению и некоторому сходству свойств амфолитные ПАВ делят на 5 осн. групп: 1) алкиламинокарбоновые кислоты RNH (CH 2 ) n COOH; алкильный радикал амина обычно нормальный (прямоцепочечный), но если он расположен между аминной группой и карбоксильной, иногда имеет разветвленный характер. К этой же группе относят алкиламино-фенилкарбоновые кислоты RNHC 6 H 4 COOH; алкиламинокарбоновые кислоты с первичной, вторичной или третичной аминогруппой RCH (NH 2 ) COOH, RCH (NHR) COOH, R(CH 3 )NCH 2 COOH; с промежуточной гидроксильной, эфирной, сложноэфирной, амидной или сульфоамидной группой; вещества с двумя и более амино- и амидогруппами, с несколькими амино- и гидроксильными группами.
5) Полимерные амфолитные ПАВ: природные (белки, нуклеиновые кислоты и т.п.); модифицированные природные (олигомерные гидролизаты белков, сульфатир. хитин); продукты ступенчатой конденсации аминов, формальдегида, альбумина, жирных кислот; производные целлюлозы, полученные введением карбоксильных и диэтаноламиноэтильных групп; синтетические, в молекулах которых сочетаются структурные особенности всех приведенных выше групп амфотерных ПАВ (см., например, формулы XII-XVI).
Применение ПАВ. Мировое производство ПАВ составляет 2-3 кг на душу населения в год. Примерно 50% производимых ПАВ используется для бытовой химии (моющие и чистящие средства, косметика), остальное-в промышленности и с. х-ве. Одновременно с ежегодным ростом проиводства ПАВ соотношение между их применением в быту и промышленности изменяется в пользу промышленности.
ПАВ находят применение более чем в 100 отраслях народного хозяйства. Большая часть производимых ПАВ используется в составе моющих ср-в, в производстве тканей и изделий на основе синтетич. и прир. волокон. К крупным потребителям ПАВ относятся нефтяная, хим. промышленности, промышленность строит. материалов и ряд других. Наиолее важные применения ПАВ:
-повышение нефтеотдачи пластов посредством мицеллярного заводнения (оксиэтилированные алкилфенолы и спирты, алкилароматич. сульфонаты);
-антиокислительные, противозадирные и др. присадки в производстве минер. масел (мыла синтетич. жирных кислот, нефтяные сульфонаты, оксиэтилир. спирты) и пластич. смазок (производные фенолов, ариламины, алкил- и арилфосфаты);
-регулирование смачивания при флотации железных и марганцевых руд (мыла прир. и синтетич. жирных кислот, высшие алифатич. амины), руд редких металлов (алкиларсоновые и алкилфосфоновые кислоты, алкилароматические сульфонаты);
-эмульсионная полимеризация, получение полистирола и др. виниловых полимеров (карбоксиметилцеллюлоза, поливиниловый спирт, мыла синтетич. жирных кислот, алкилсульфаты, оксиэтилированные спирты и алкилфенолы);
Производство хим. волокон (оксиэтилир. амины и амиды, проксанолы и проксамины, высшие спирты и кислоты);
Механическая обработка металлов: адсорбц. понижение прочности, повышение скоростей резания, строгания, фрезерования (мыла прир. и синтетич. жирных кислот, алкилароматич. сульфонаты, оксиэтилир. спирты и т.д.);
Промышленность строит. материалов: регулирование мех. и рео-логич. свойств бетонных смесей за счет адсорбц. модифицирования компонентов (эфиры синтетич. жирных кислот, сульфонаты, алкиламины, алкилсульфаты, оксиэтилир. жирные кислоты);
Биологическое разложение ПАВ. Водные растворы ПАВ в большей или меньшей концентрации поступают в стоки промышленных вод и в конечном счете-в водоемы. Очистке сточных вод от ПАВ уделяется большое внимание, т. к. из-за низкой скорости разложения ПАВ вредные результаты их воздействия на природу и живые организмы непредсказуемы. Сточные воды, содержащие продукты гидролиза полифосфатных ПАВ, могут вызвать интенсивный рост растений, что приводит к загрязнению ранее чистых водоемов: по мере отмирания растений начинается их гниение, а вода обедняется кислородом, что в свою очередь ухудшает условия существования др. форм жизни в воде.
При биохимической очистке отработанных растворов ПАВ окисление ведется в присутствии ферментов. С увеличением температуры скорость окисления увеличивается, но выше 35 0 C ферменты разрушаются. Анионактивные ПАВ адсорбируются на межфазных поверхностях раздела, вследствие чего снижается ферментативный гидролиз жиров, белков и углеводов, приводящий к угнетению жизнедеятельности бактерий.
Механизм биоокисления ПАВ устанавливается путем изучения промежуточных продуктов распада. Так, в промежуточных продуктах распада алкилбензолсульфонатов обнаружены: алкилбензолсульфонаты с короткой алкильной цепью; сульфофенилкарбоновые кислоты в среднем с 4 атомами С в цепи; сульфокарбоновые кислоты с 5-6 атомами С; сульфодикарбоновые кислоты и сульфокислоты. Это позволяет предположить, что биоразложение начинается с концевой метильной группы. Чем ближе остаток продвигается к бензольному кольцу, тем окисление происходит медленнее. Конечной стадией является распад бензольного кольца на ненасыщенные соединения, которые окисляются достаточно быстро и полно.
Алифатические ПАВ окисляются быстрее, чем циклические, причем сульфонаты окисляются труднее, чем сульфаты.
По-видимому, это связано с тем, что сульфаты в воде гидролизуются. Прямоцепочечные первичные и вторичные алкилсульфаты за 1 ч полностью разрушаются в сточных водах. Алкилсульфаты с разветвленной цепью окисляются медленнее, а прямоцепочечные алкилбензолсульфонаты полностью распадаются лишь за 3 суток. Биоразложение катионактивных ПАВ мало изучено, некоторые исследователи не рекомендуют сбрасывать их в сточные воды.
Лит.: Коллоидные поверхностно-активные вещества, пер. с англ. под ред. А. Б. Таубмана, 3. H. Маркиной, M., 1966; Физико-химические основы применения поверхностно-активных веществ, Ташкент, 1977; Поверхностно-активные вещества. Справочник, под ред. А. А. Абрамзона и Г. M. Паевого, Л., 1979; Мицеллообразование, солюбилизация и микроэмульсии, пер. с англ., M., 1980; А б r а м з о н А. А., Поверхностно-активные вещества. Свойства и применение, 2 изд., Л., 1981; Успехи коллоидной химии, под ред. И. В. Петрянова-Соколова и К. С. Ахмедова, Ташкент, 1987. С. И. Файнгольд, В. П. Тихонов.
Х и м и я
Коллоидная химия
Поверхностно-активные вещества (ПАВ).
Что такое ПАВ?
Строение ПАВ
Работа ПАВ в дисперсных системах
Классификация ПАВ
По типу гидрофильных групп:
По характеру использования:
По длине гидрофобной цепи:
Использование ПАВ
Воздействие ПАВ на человека
Влияние ПАВ на окружающую среду.
Что такое ПАВ?
Поверхностно-активные вещества – это химические соединения, способные накапливаться на поверхности соприкосновения двух тел или двух термодинамических фаз (называемых поверхностью раздела фаз), и вызывающие снижение поверхностного натяжения веществ, образующих эти фазы.
На межфазной поверхности Поверхностно-активные вещества образуют слой повышенной концентрации — адсорбционный слой.
Строение ПАВ
Строго говоря, очень многие вещества при соответствующих условиях могут проявить поверхностную активность, т. е. адсорбироваться под действием межмолекулярных сил на той или иной поверхности, понижая её свободную энергию.
Однако поверхностно-активными обычно называются лишь те вещества, присутствие которых в растворах уже при весьма малых концентрациях (десятые и сотые доли %) приводит к резкому снижению поверхностного натяжения вещества этих растворов.
Как правило, такие вещества имеют дифильное строение молекул.
Слово дифильный можно перевести как «двояколюбящий» (от philéo — люблю). Или, выражаясь по-русски, дифильными можно назвать молекулы, имеющие сродство к веществам с разной природой.
Например, вода и масло почти не взаимодействуют друг с другом. Если их смешать в одной ёмкости, то такая смесь через некоторое время расслоится. Вода, как более тяжёлая, окажется внизу ёмкости, а масло соберётся в верхней её части.
Расслоение присходит потому, что масло и вода относятся к разным средам. Между молекулами этих сред действуют принципиально разные силы. Подробнее об этом в разделе: Взаимодействие «воды» и «масла».
Молекулы воды взаимодействуют друг с другом при помощи ориентационных сил, а молекулы масла – при помощи дисперсионных сил. Таким образом, при встрече вода и масло проявляют друг к другу безразличие.
В молекулах дифильных веществ одновременно присутствуют как полярные (гидрофильные) группы, так и неполярные (гидрофобные).
К ПАВам относятся карбоновые кислоты, их соли, спирты, амины, сульфокислоты и другие вещества.
Самым распространённым примером веществ с дифильной структурой являются мыла – натриевые и калиевые соли высших жирных кислот.
Работа ПАВ в дисперсных системах
Дифильные вещества обладают замечательным качеством. Они являются своего рода «мостиками», при помощи которых становится возможным взаимодействие фаз, до этого «игнорировавших» друг друга.
Действие таких веществ проявляется на поверхности соприкасающихся фаз и приводит к ативности сами вещества фаз, которые до этого момента не взаимодействовали.
Благодаря своим качествам ПАВы могут использоваться в составах моющих средств или стабилизаторов эмульсий.
В моющих средствах ПАВы работают следующим образом.
Молекула ПАВ – это дифильная молекула, имеющая в своём составе, как полярные (гидрофильные) группы, так и неполярные (гидрофобные).
Таким образом, своим гидрофобным хвостом она может взаимодействовать с молекулами загрязнения (как правило, имеющего жирную, т.е гидрофобную природу), а при помощи своей полярной группы связывается с полярной молекулой воды.
Одновременно с этим молекулы ПАВ внедряются в поверхностный слой загрязнения и понижают силы взаимного притяжения между молекулами загрязнения.
Говоря по-другому, молекулы ПАВ положительно адсорбируются в поверхностном слое загрязнения и снижают поверхностное натяжение взаимодействующих фаз. Это, в свою очередь, облегчает возможность отрыва отдельных кусочков загрязнения от основной его массы. Оторванные части загрязнения уносятся водой.
Самые известные моющие средства – мыла. Мыла представляют собой натриевые и калиевые соли жирных кислот (натриевые – твёрдые, калиевые – жидкие).
CH 3 (CH 2 ) n COONa.
Эму́льсия — дисперсная система, состоящая из микроскопических капель жидкости (дисперсной фазы), распределенных в другой жидкости (дисперсионной среде).
Дисперсная фаза и дисперсионная среда – это две фазы жидкостей, имеющих разную природу, и по этой причине, не растворяющиеся одна в другой, отторгающие друг друга.
Если уже знакомые нам воду и масло тщательно перемешать друг с другом при помощи миксера, то они образуют дисперсную систему, в которой маленькие частички воды будут соседствовать с частичками масла.
Но эта дисперсная система просуществует недолго. По уже известным нам причинам произойдёт расслоение фаз. Частички воды и масла будут укрупняться, соединяясь с себе подобными. Через некоторое время произойдёт образование двух монолитных фаз: масло вверху, вода внизу. Так что такую систему нельзя назвать дисперсной.
Чтобы дисперсная система состоялась, в её состав добавляют специальные вещества – стабилизаторы эмульсий или эмульгаторы.
Эмульгаторы представляют собой поверхностно активные вещества.
Представим себе эмульсию типа «масло в воде». В такой эмульсии микроскопические капельки масла будут распределены в объёме воды.
Эмульгатор, присутствующий в эмульсии, состоит из молекул дифильной природы. Своими гидрофобными хвостами молекулы эмульгатора будут взаимодействовать с молекулами масла. В результате этого взаимодействия вытянутые молекулы эмульгатора приобретут чёткую ориентацию: гидрофобные хвосты внутрь, полярные группы наружу.
Такое образование, напоминающее свернувшегося ежа, называется мицеллой.
Наружная поверхность мицеллы будет образована полярными (гидрофильными) группами эмульгатора. А эти группы, как мы знаем, могут взаимодействоать с молекулами воды, притягивая к себе противоположно заряженные части этих молекул.
Эта конструкция позволяет эмульсии избежать расслоения и в течение долгого времени сохраняет её стабильной.
Классификация ПАВ
Поверхностно активные вещества можно классифицировать по разным признакам. Мы приведём три вида классификаций:
По типу гидрофильных групп:
По характеру использования:
По длине гидрофобной цепи:
Классификация по типу гидрофильных групп:
Для ПАВ эта классификация является основной.
По типу гидрофильных групп ПАВы делят на:
— ионные, или ионогенные,
— неионные, или неионогенные.
Рабочее действие ПАВа обеспечивается именно адсорбционно активными ионами.
Если адсорбционно активны анионы (т.е. отрицательно заряженные ионы), то ПАВы называются анионными, или анионоактивными, если активны катионы (положительно заряженные ионы) — катионными, или катионо-активными.
Амфотерные (или амфолитные) ПАВ содержат в своём составе одновременно две функциональные группы, одна из которых имеет кислый, другая – основной характер. В зависимости от среды, в которой они находятся, амфотерные ПАВы могут принимать или отдавать протон и проявлять, таким образом, либо анионную либо катионную активность.
Анионные ПАВы, как говорилось выше, диссоциируют, образуя отрицательно заряженные органические анионы:
По своему составу анионные ПАВы, чаще всего — это органические кислоты и их соли:
R-COOН или R-COONa, R-COOК.
Наиболее распространены натриевые и калиевые соли жирных кислот. Их называют мылами. Натриевые соли имеют твёрдую консистенцию, калиевые – жидкую.
Также, большое распространение имеют соли кислых эфиров высокомолекулярных спиртов жирного ряда и серной кислоты с общей формулой:
Такие соли называются алкилсульфатами. Алкилсульфаты вырабатываются из спиртов с количеством углеродных атомов в цепи С12 – С14, получаемых из кокосового масла или гидрогенезацией кашалотного жира. Жирные спирты подвергаются фракционной дистилляции, и сульфатируются серной или хлорсульфоновой кислотой.
Полученный таким образом лаурилсульфат является одним из наиболее широко используемых анионных моющих средств. Его формула:
К анионным ПАВам принадлежат многие классы химических соединений. В таблице ниже приведём некоторые из них:
Некоторые анионные ПАВ
Na-соль первичных алкилсульфатов
Разветвлённые вторичные сульфаты
Соли высших жирных кислот (мыла)
Сложные эфиры моноглицеридсульфатов
Сульфированные жирноароматические карбоновые кислоты
Сложные эфиры сульфоянтарнойкислоты
Бутиловый эфир сульфорицинолевой кислоты
Сложные эфиры сульфонаталкилкарбоновых кислот
Модифицированные мыла N-метил-N-карбоксиметиламиды высших кислот
Конденсат полипептида с жирными кислотами
Конденсат полипептида и алкилсульфоновых кислот
Среди ПАВов именно анионные ПАВы получили самое большое распространение. Их объём производства превышает объёмы производства всех остальных ПАВ вместе взятых.
Катионные ПАВы при диссоциации образуют положительно заряженные поверхностно-активные органические катионы:
Катионные ПАВы — основания, обычно амины различной степени замещения, и их соли. Они представлены следующими соединениями:
Некоторые катионные ПАВ
Соли первичных аминов
Соли вторичных аминов
Соли третичных аминов
Четвертичные аммониевые соли
Объём производства катионных ПАВ значительно ниже, чем анионных, ни их роль с каждым годом возрастает благодаря их моющему и бактерицидному действию, а некоторые их представители, например цетилпиридиний хлорид, вошли в арсенал лекарственных средств.
Амфотерные (или амфолитные) ПАВ в зависимости от условий среды могут проявлять либо анионную, либо катионную активность.
Необходимым условием амфотерности ПАВ является близость констант и основной диссоциации.
Степень превращения ПАВа в катионную или анионную форму зависит от рН среды.
К амфотерным ПАВ относят чаще всего соединения, содержащие одновременно:
Наиболее типичным представителем этого класса ПАВ является альфа-алкил-бетаин, получивший торговое название бетаин:
Неионные ПАВ представляют собой высокомолекулярные соединения, которые в водном растворе не образуют ионов.
Растворимость этих ПАВ в воде обусловлена наличием в молекуле неионогенных групп – эфирных или гидроксильных (чаще всего полиэтиленгликолиевый остаток).
Неионные ПАВы представляют особую ценность для медицинской промышленности. Это объясняется несколькими причинами:
2. Неионные ПАВы обладают большой устойчивостью к воздействию щелочей, кислот и солей. Они совместимы с большинством лекарственных веществ, могут смешиваться с органическими растворителями.
3. В отличие от ионных ПАВ, неионные ПАВы оказывают меньшее раздражающее действие на кожный покров и слизистые оболочки. Они не агрессивны, повышают резорбцию лекарственных веществ; эффективны как вспомогательные вещества в приготовлении лекарственных форм.
К классу неионных ПАВ, не подвергающихся электролитической диссоциации принадлежат следующие соединения.
Некоторые неионные ПАВ
1. Полиэтиленоксидные производные
Эфиры полигликоля и высших жирных кислот
Алкилфениловый эфир полигликоля
Эфир ангидросорбита и жирных кислот (спены)
Полигликолевый эфир ангидросорбита и жирных кислот (твины)
3. Алкилоламиды жирных кислот
Полигликолевый эфир полипропиленгликоля
Полигликолевый эфир этилендиаминополипропиленгликоля
Классификация по характеру использования:
Частным случаем эмульгаторов являются пенообразователи и стабилизаторы пены.
Смачиватели – вещества, вызывающие пептизацию или диспергирование, т.е. измельчение твёрдых тел на мелкие частички или жидкой фазы на мелкие капельки.
Смачивание – первая фаза моющего действия, когда загрязнение распадается на отдельные частички или капельки и впоследствии обвалакивается ПАВом (солюблизируется), и удаляется водой.
Солюблизаторы – вещества, помогающие повысить растворение частиц другого вещества, слаборастворимого в данной жидкой среде.
Молекулы солюблизатора обвалакивают плохо растворимую в данной среде частичку и образуют вокруг неё, так называемую мицеллу.
Сама мицелла имеет сродство к среде растворителя и поэтому растворяется в нём, обеспечивая растворение изначально нерастворимой в нём частицы.
Смачивание, солюблизация, эмульгирование – все эти процессы являются стадиями моющего действия. Любой ПАВ, в той или иной степени, одновременно является и смачивателем, и солюблизатором, и эмульгатором, и моющим веществом. Но при этом, разные ПАВы проявляют разную эффективность на разных стадиях моющего действия. По этой причине они могут быть классифицированы на смачиватели, солюблизаторы, эмульгаторы и моющие средства.
Классификация ПАВ по длине гидрофобной цепи:
Этот вид классификации особенно важен в случаях, когда поверхностно-активные вещества выполняют роль стабилизаторов эмульсий (эмульгаторов).
Напомним, что эмульгаторы представляют собой дифильные вещества, молекулы которых имеют в своём составе, как полярную (гидрофильную) группу, так и неполярную (гидрофобную) часть.
В зависимости от длины углеводородного (гидрофобного) «хвоста» и силе полярных групп в молекуле такой молекулы, эмульгатор, в целом, будет проявлять или гидрофильные или гидрофобные качества. А от этого всецело будет менятся его роль при стабилизации разного рода эмульсий.
Гидрофильные эмульгаторы. Стабилизация эмульсий типа «вода в масле».
Эмульгаторы с относительно короткой гидрофобной частью, имеют большее сродство с водой и их, поэтому называют гидрофильными.
Гидрофильные эмульгаторы необходимы для стабилизации эмульсий типа «масло в воде». При добавлении гидрофильного эмульгатора в такую эмульсию вокруг капельки масла образуется сплошной слой эмульгатора, сообщающий ей некоторую гидрофильность и повышающий её устойчивость.
Добавление в такую же смесь гидрофобного эмульгатора, большая часть молекулы которого погружается в капельку масла, не обеспечивает устойчивости эмульсии, поскольку часть поверхности капельки остаётся «открытой» и легко может происходить слияние с другими капельками.
Гидрофобные эмульгаторы. Стабилизация эмульсий типа «вода в масле».
Эмульгаторы, молекулы которых имеют относительно длинную гидрофобную часть, обладают преимущественно гидрофобными свойствами. Такие эмульгаторы называют гидрофобными (или липофильными).
Гидрофобные эмульгаторы стабилизируют эмульсии типа «вода в масле». Их молекула, находящаяся большей своей частью в дисперсионной среде (масле), удерживается на поверхности капелек воды своей гидрофильной группировкой (Рис. а).
В результате вокруг каждой капельки воды образуется плотная оболочка из молекул эмульгатора, препятствующая слиянию дисперсной фазы (воды).
Попытка получить эмульсию такого же типа с гидрофильным эмульгатором оказалась бы безуспешной, так как молекулы эмульгатора разместились бы в основном внутри капелек воды (Рис. б).
Вместо сплошной оболочки вокруг капелек имелись бы лишь выступающие над их поверхностью отдельные гидрофобные группы эмульгатора, не препятствующие коалесценции капелек.
Таким образом, эмульгатор должен обладать сродством к дисперсионной среде.
В зависимости от типа желаемой эмульсии следует брать гидрофильные или гидрофобные эмульгаторы той или иной степени диссоциации.
Дисперсность эмульгаторов
Эмульгаторы для эмульсий типа м/в
Эмульгаторы для эмульсий типа в/м
CaCO3, CaSO4, Fe2O3, Fe(OH)3, SiO2, глина и др.
HgI2, PbO, сажа и др.
Желатин, казеин, альбумин, крахмал, декстрин, гуммиарабик, лецитин, желчные кислоты и др.
Смолы, каучук, холестерин и др.
Мыла щелочных металлов, красители
Мыла многовалентных металов
Гидрофильно-липофильный баланс ПАВ
Для количественной оценки пригодности ПАВов в разных областях использования, в том числе, в качестве эмульгаторов в различных средах был введен параметр, называемый гидрофильно-липофильным балансом (ГЛБ).
Каждому поверхно-активному веществу соответствует определённая величина ГЛБ.
Самое низкое значение ГЛБ имеет олеиновая кислота C17H33COOH (ГЛБ = 1),
Для всех остальных ПАВ величина ГЛБ находится в пределах от 1 до 40.
На основании величин ГЛБ определяется сфера использования ПАВ, например:
Использование ПАВ в зависимости от величины ГЛБ
Эмульсия вода в масле (в/м)
Эмульсия масло в воде (м/в)
ПАВ с липофильными свойствами имеют низкие значения ГЛБ, с гидрофильными – высокие.
Использование ПАВ
Мировое производство ПАВ постоянно возрастает, причём доля неионных и катионных веществ в общем выпуске всё время увеличивается.
В зависимости от назначения и химического состава ПАВы выпускают в виде твёрдых продуктов (кусков, хлопьев, гранул, порошков), жидкостей и полужидких веществ (паст, гелей).
Особое внимание всё больше и больше уделяется производству ПАВ с линейным строением молекул, которые легко подвергаются биохимическому разложению в природных условиях и не загрязняют окружающую среду.
ПАВ находят широкое применение в промышленности, сельском хозяйстве, медицине, быту. Важнейшие области потребления ПАВ: производство мыл и моющих средств для технических и санитарно-гигиенических нужд; текстильно-вспомогательных веществ, т. е. веществ, используемых для обработки тканей и подготовки сырья для них; лакокрасочной продукции.
ПАВ используют во многих технологических процессах химических, нефтехимических, химико-фармацевтических, пищевой промышленности. Их применяют:
Воздействие ПАВ на человека
Подавляющее количество ПАВ при использовании имеет непосредственный контакт с кожей, поэтому следует обращать внимание на их дерматологическое действие.
Известно, что мыла при длительном контакте вызывают раздражение кожи, причём этоя явление более характерно для натриевых солей С8 – С10 насыщенных жирных кислот в сравнении с их высшими гомологами.
Алкилсульфаты с длиной жирной цепи менее С12 и алкиларилсульфонаты раздражают кожу сильнее, чем мыла.
Сульфоэтерифицированные масла и сульфоэфиры, а также продукты конденсации высших жирных кислот и белков не вызывают заметного раздражения кожи, поэтому многие очищающие и моющие композиции включают соединения этих типов.
По убыли раздражающего действия на кожу человека ПАВы можно расположить в следующий ряд:
Катионные > анионные > неионные.
Влияние на слизистую оболочку глаз
Растворы многих ПАВ при попадании в глаза вызывают болезненное ощущение, а при большей концентрации могут повредить глазную ткань.
По силе раздражающего действия на глаза основные группы ПАВ располагаются в том же порядке, что и по их влиянию на кожу.
ПАВ и гемолиз эритроцитов.
Существенным недостатком синтетических ПАВ является то, что внутревенное введение их растворов сопровождается гемолизом (разрушением) эритроцитов.
При этом оболочка эритроцитов разрушается или становится проницаемой для гемоглобина, который выходит из них в окружающую среду.
Гемолитическое действие ряда гомологов жирных сульфатов и алкилдиметилбензиламмония хлорида проявляется при концентрациях, более низких по сравнению с критической концентрацией мицеллообразования.
Гемолиз, вызываемый ПАВ, задерживается в присутствии холестерина и фосфолипидов.
Введённые в ток крови ПАВы взаимодействуют не только с эритроцитами, но и с другими составными её частями.
Так, полиоксиэтиленовый эфир алкилфенола в очень высокой степени повышает фагоцитозное действие лейкоцитов, а сульфонаты лигнина действуют как антикоагулянты.
Все классы ПАВ проходят тщательную проверку на токсичность.
В таблице ниже приведены данные об иследованиях некоторых синтетических ПАВ на токсичность:
Наименование класса соединений ПАВ
Доза LD 50 г/кг
Способ введения ПАВ
Неполимерные четвертичные аммониевые соединения
Типичные анионоактивные вещества (сульфаты и сульфонаты)
Эфиры полиоксиэтилена и полиэтиленгликоля
Следует заметить, что величина LD50 в пределах данного класса ПАВ зависит от молекулярной структуры и от молекулярного веса.
Известно, что полиоксиэтилены с высоким молекулярным весом при приёме внутрь практически нетоксичны, тогда как их низшие гомологи, например диэтиленгликоль при введении с пищей белым крысам замедляли их рост, вызывали их дегенеративные изменения в печени и почках, появление в мочевом пузыре оксалатных камней и новообразований на слизистой оболочке.
Влияние ПАВ на окружающую среду.
В последние несколько десятилетий постоянно росло потребление синтетических моющих средств и соответственно происходило сокращение потребления мыла.
Дело в том, что многие синтетические моющие средства, в отличие от мыл, не подвержены естественному биохимическому разложению и не не задерживаются фильтрующими установками, и это приводит не только к загрязнению рек и других водоёмов, но и к проникновению ПАВ в источники питьевой воды, что непосредственно влияет на здоровье человека.
Биоразложение протекает очень медленно, конечными продуктами его являются вода и диоксид углерода.
Для массового производства и потребления моющих средств необходимо применять такие ПАВ и другие моющие вещества, которые были бы подвержены сравнительно быстрому их распаду.
В настоящее время приняты законы, разрешающие производство и применение ПАВ для моющих средств, биоразлагаемых не менее чем на 80%.
Биоразлагаемость некоторых ПАВов.
Биоразлагаемость алкилсульфонатов, полученных из нормальных парафинов, достигает 98%, олефинсульфонатов – 90-95%, у алкилсульфатов (С10-С18) – 97,9%.
Неиногенные ПАВ разлагаются легче, чем анионактивные, но их биоразлагаемость понижается с увеличением числа присоединённых групп этиленоксида и разветвлённости гидрофобной части молекулы.
Сульфаты неионогенных ПАВ, полученных на основе прямоцепочных жирных спиртов, легко разлагаются, и длина этиленоксидной цепи не влияет на степень и скорость разложения.
Разные подходы в защите окружающей среды
По данным ряда исследователей, для защиты окружающей среды при производстве и употреблении моющих средств наиболее рациональным путём является замена алкилбензолсульфонатов алкилсульфатами и алкилсульфонатами, а также применение натуральных жирных кислот и их производных, кукурузного крахмала и других, биоразлагаемость которых является стопроцентной.
Наличие моющих средств в сточных водах вызывает обильное пенообразование за счёт остаточных ПАВ, фосфатов и других компонентов моющих средств, что затрудняет биологическую очистку.
Но существует и другой подход, заключающийся в том, что введение в действие эффективных методов очистки сточных вод экономически целесообразнее, чем замена плохоразлагающихся компонентов моющих средств другими, менее эффективными в моющем действии.