Что такое диффузная способность легких
Исследование диффузионной способности легких с определеним ЖЕЛ
Если спирометрия и бодиплетизмография измеряют объемы легких и наличие/отсутствие сужения дыхательных путей, то исследование диффузионной способности легких проверяет, как кислород проходит через мембраны легких и попадает в мельчайшие сосуды легких (капилляры), откуда уже с током крови разносится по всему организму.
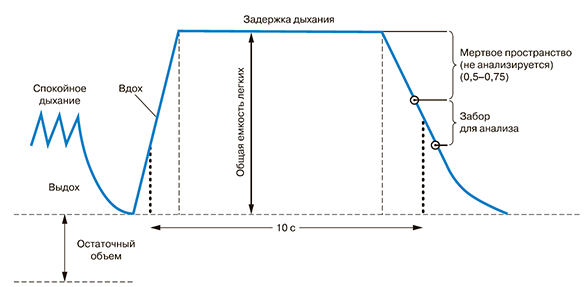
Маневр при выполнении оценки диффузионной способности чрезвычайно прост для пациента, нужно вначале сделать полный выдох, затем глубоко вдохнуть, задержать дыхание на 10 секунд и мощно выдохнуть. К этому исследованию практически нет противопоказаний.
Это очень важное исследование:
· Помогает определить причину одышки, уменьшения легочных объемов
· Помогает диагностировать эмфизему, и разграничить бронхиальную астму и ХОБЛ, что иногда бывает непросто
· Помогает диагностировать заболевания легочных сосудов
· Используется для отслеживания динамики при некоторых легочных заболеваниях (например, саркоидоз, легочный фиброз и многие другие)
Подготовка к исследованию:
· не курить в течение 4 ч до исследования, если это оказывается невозможным, то нужно обязательно сообщить врачу, когда Вы выкурили последнюю сигарету
· до проведения процедуры не использовать противоастматические лекарственные препараты, которые могут повлиять на результат измерения (продолжительность зависит от конкретного лекарственного препарата)
· за 15 минут до исследования следует приостановить терапию кислородом (если она проводится)
· избегать интенсивной физической нагрузки в течение 4 часов до исследования
Записаться по телефону: 8-495-395-63-93
Диффузионная способность легких при ХОБЛ: есть ли различия у пациентов разного пола
Актуальность
Хорошо известно прогностическое значение единичного измерения диффузионной способности легких для монооксида углерода у пациентов с хронической обструктивной болезнью легких (ХОБЛ). Вместе с тем данных об изменении диффузионной способности, как и о возможных отличиях в значениях этого показателя между мужчинами и женщинами крайне мало. В связи с чем целью обсуждающегося исследования стала оценка диффузионной способности легких за определенный промежуток времени у пациентов с ХОБЛ.
Методы
Участниками исследования были курящие пациенты. Всем пациентам на протяжении 5 лет проводилась оценка функции легких, в том числе определение диффузионной способности для монооксида углерода.
В исследование было включено 602 курящих пациента (33% – женщины). 506 (84%) пациентов имели ХОБЛ.
Среднегодовое снижение диффузионной способности легких составило 1.34±0.0015%. Такая динамика оказывалась более выраженной у пациентов с ХОБЛ, по сравнению с группой контроля (p=0.004).
Женщины имели худшие значения диффузионной способности легких на старте исследования, а также характеризовались более выраженной негативной динамикой этого показателя на протяжении всего периода исследования (p=0.039). При этом объем форсированного выдоха за первую секунду у них оказывался статистически значимо больше, чем у мужчин.
Заключение
Таким образом, пациенты с ХОБЛ характеризуются ускоренным снижением диффузионной способности легких. Причем женщины при лучшем объеме форсированного выдоха за первую секунду имеют как исходно худшие значения диффузионной способности легких, так и характеризуются более выраженным ее снижением на протяжении наблюдения.
Источник:
Casanova C, et al. Chest. 2021:S0012-3692(21)00696-6. doi: 10.1016/j.chest.2021.03.069.
Всероссийская Образовательная Интернет-Сессия
Информация и материалы, представленные на настоящем сайте, носят научный, справочно-информационный и аналитический характер, предназначены исключительно для специалистов здравоохранения, не направлены на продвижение товаров на рынке и не могут быть использованы в качестве советов или рекомендаций пациенту к применению лекарственных средств и методов лечения без консультации с лечащим врачом.
Лекарственные препараты, информация о которых содержится на настоящем сайте, имеют противопоказания, перед их применением необходимо ознакомиться с инструкцией и проконсультироваться со специалистом.
Мнение Администрации может не совпадать с мнением авторов и лекторов. Администрация не дает каких-либо гарантий в отношении cайта и его cодержимого, в том числе, без ограничения, в отношении научной ценности, актуальности, точности, полноты, достоверности научных данных представляемых лекторами или соответствия содержимого международным стандартам надлежащей клинической практики и/или медицины основанной на доказательствах. Сайт не несет никакой ответственности за любые рекомендации или мнения, которые могут содержаться, ни за применимость материалов сайта к конкретным клиническим ситуациям. Вся научная информация предоставляется в исходном виде, без гарантий полноты или своевременности. Администрация прикладывает все усилия, чтобы обеспечить пользователей точной и достоверной информацией, но в то же время не исключает возможности возникновения ошибок.
Диффузионный тест. Для чего проводится, какова методика, показания и результаты диффузионного теста
1. Для чего проводится диффузионный тест
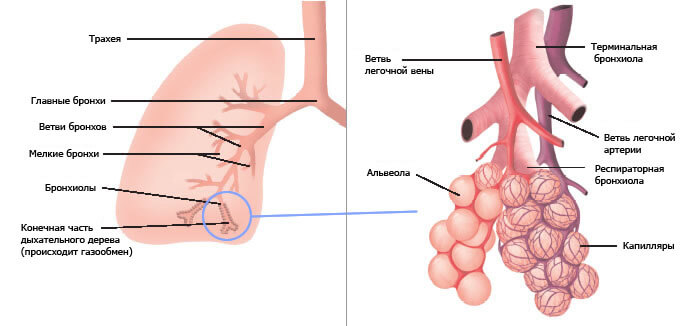
Процесс дыхания заключается не только в акте втягивания воздуха в дыхательную систему, но и в последующем переносе газов (кислорода и СО2), происходящем на альвеолярной поверхности лёгких. Важнейшая цель дыхания – газообмен. Именно этот процесс обеспечивается посредством циклов вдохов и выдохов: кровь насыщается кислородом и отдаёт в атмосферу углекислый газ. При нормальном функционировании лёгких, бронхов и диафрагмы, но нарушенной диффузии, наступает гипоксия, что неизбежно отражается на общем самочувствии и несёт риск тяжёлых расстройств.
В пульмонологии существенное значение отводится функции лёгочного газообмена. Многие заболевания требуют исследования не только органических структур дыхательной системы, но и изучения функции диффузии газов на поверхности лёгких. Одной из важнейших диагностических методик является диффузионный тест, позволяющий оценить эффективность лёгочного газообмена, которая зависит от скорости перехода газов через альвеолярно-капиллярный барьер.
Феномен диффузии кислорода в кровь и вывода CО2 в составе выдыхаемого воздуха отражается величиной, обратной сопротивлению диффузии, которая называется «диффузионная способность лёгких».
2. Какова методика проведения и показания для диффузионного теста
Измерение диффузионной способности лёгких может проводиться в рамках бодиплетизмографии или вне иных видов диагностики.
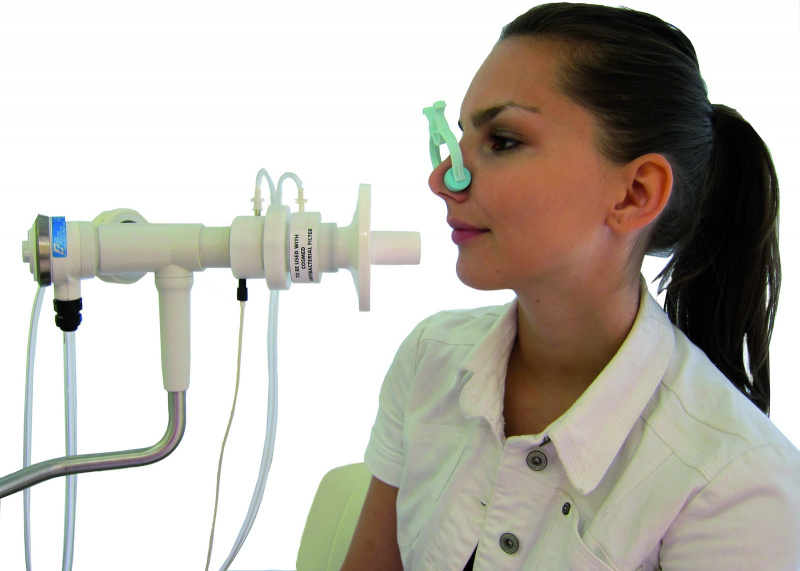
Нос пациента зажимается специальным зажимом. Для проведения исследования ему необходимо сделать глубокий вдох безопасной газовой смеси, содержащий инертный газ (гелий или метан). Она не имеет вкуса и запаха и воспринимается как обычный воздух. После этого необходимо ненадолго задержать дыхание, а затем произвести выдох в трубку прибора. Вдох должен длиться не более 4 секунд, а выдох – 3 секунды.
Результаты данной диагностики пациент получает сразу же. Методика не имеет противопоказаний, не доставляет больному дискомфорта и не требует специальной подготовки. Рекомендуется лишь отказаться от курения и плотного приёма пищи перед диагностикой. Также по согласованию с врачом при подготовке к диагностике отменяются некоторые лекарственные препараты и процедуры.
Исследование диффузионной способности дыхательной системы может быть назначено в следующих случаях:
3. Что отражают результаты исследования диффузионной способности лёгких
Диффузионная способность лёгких снижается при определённых заболеваниях. Диффузионный тест позволяет подтвардить, что причина недостаточности дыхательной функции заключается именно в нарушении газообмена. Данная патология может быть обусловлена капиллярным или мембранным компонентом. Увеличение толщины альвеолярно-капиллярной мембраны или снижение площади диффузионной поверхности обуславливают снижение показателей, получаемых в ходе исследования. Выявленное снижение диффузии по результатам проведения диффузионного теста может указывать на следующие нарушения:
Снижение способности к газообмену всегда сопровождает тяжёлые формы ХОБЛ, бронхиолит, эмфизему лёгких.
Повышенные показатель, полученные в ходе диффузионного теста, также могут указывать на наличие патологии. Такая клиническая картина может наблюдаться при:
Исследование диффузионной способности легких
В стандартной практике врачу пульмонологу чаще всего достаточно спирометрических тестов:
ФЖЕЛ (FVC) форсированной жизненной ёмкости легких
ЖЕЛ (VC) жизненной емкости легких
ОФВ1 (FEV1) объёма воздуха, выдохнутого в течение первой секунды форсированного выдоха.
Этих исследований чаще всего достаточно, чтобы отслеживать течение заболевания и корректировать эффективность проводимого лечения.
Показания для исследования диффузионной способности легких
Исследование диффузионной способности легких является вторым по значимости респираторным тестом, который зачастую выполняется совместно с бодиплетизмографией.
DLCO применяется для диагностики:
эмфиземы или легочного фиброза
заболевания легочных сосудов
разграничения бронхиальной астмы и ХОБЛ
отслеживания динамики заболеваний (саркоидоз и другие)
определить причину одышки, уменьшения легочных объемов
Важный критерием качества жизни для пациентов с обструктивными заболеваниями легких – это отдышка, способность пациентов жить обычной жизнью с бытовыми нагрузками, что часто не коррелирует с показателем объема форсированного выдоха за первую секунду (FEV1) и тут нам на помощь приходит исследование диффузионной способности легких.
История методики исследования диффузионной способности легких
Термин диффузионной способности легких по монооксиду углерода или иначе, трансфер фактор был впервые озвучен в 1909 году в трудах Августа и Мари Крог. Крог был первым, кто описал зависимость изменений в кровотоке мышц и других органов от потребностей организма через открытие и закрытие просвета артериол и капилляров, он также явился автором спирометра и еще нескольких известных сейчас приборов.
В 1957 году Огилви опубликовал “модифицированный метод Крога одиночного вдоха” исследования диффузионной способности легких по монооксиду углерода с использованием индикаторного газа для определения альвеолярного объема (VA).
В 2017 г. ATS и ERS были представлены новые стандарты проведения исследования дифузионной способности методом однократного вдоха СО с задержкой дыхания. Отличия в рекомендациях основаны на появлении современных датчиков, способных непрерывно анализировать газовую смесь, а не оценивать выдох по классическому способу в “мешке”.
На основе рекомендаций ATS и ERS Г. В. Неклюдова, д. м. н. и А. В. Черняк, к. м. н. составили национальный стандарт измерения диффузионной способности легких по монооксиду углерода методом одиночного вдоха.
Методика исследования трансфер-фактора
При поступлении кислорода в кровь его молекулы должны преодолеть альвеолярную стенку, капиллярную стенку, мембрану и плазму эритроцита и соединиться с гемоглобином.
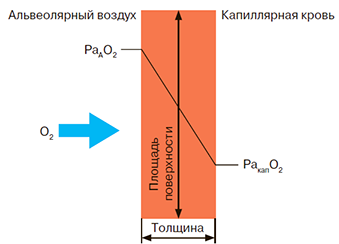
Теория процесса очевидна и проста, описывается первым законом диффузии Фика, согласно которому, скорость диффузионного потока через слой ткани прямо пропорциональна площади этого слоя, разности парциального давления по обе его стороны и обратно пропорциональна толщине слоя.
чем больше площадь альвеолярно-капиллярной мембраны, тем выше трансфер-фактор
чем больше толщина альвеолярно-капиллярной мембраны, тем меньше трансфер-фактор
Исследование основано на знаниях о разных диффузионных способностях газов в организме. Оценить транспорт кислорода технически сложно из-за большого содержания кислорода и углекислого газа в крови и как следствие инертности данного метода, поэтому мы используем оксид углерода (который практически не содержится в венозной крови) и аппроксимируем результат.
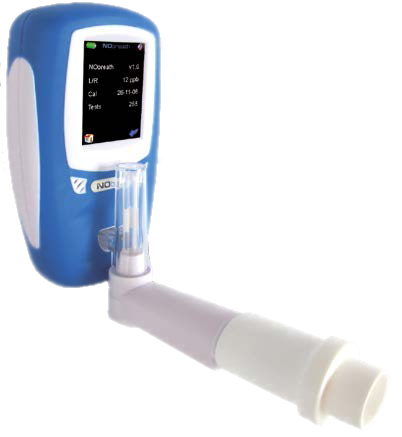
После нескольких спокойных вдохов и выдохов обычным воздухом пациент должен выдохнуть весь воздух, затем сделать максимально глубокий вдох газовой смеси, задержать дыхание на 8–10 с, после чего быстро выдохнуть газ.
Пациент вдыхает смесь из инертного газа, гелия He (до 10%) и оксида углерода CO (до 1%), уменьшение концентрации CO в выдыхаемом воздухе отражает его перенос в кровь.
Подготовка к исследованию диффузионной способности легких
Не заниматься интенсивной физической нагрузкой за 4 часа до исследования
Не использовать противоастматические лекарственные препараты, могут повлиять на результат измерения (продолжительность зависит от конкретного препарата)
Если проводится кислородная терапия – остановить за 15 минут до исследования
Исследование респираторной функции и функциональный диагноз в пульмонологии
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Кафедра госпитальной терапии РГМУ
НИИ пульмонологии Минздрава РФ, Москва
Хронические болезни легких диагностируют поздно, так как выраженные симптомы заболевания проявляются тогда, когда функция дыхания уже существенно нарушена, и, следовательно, назначаемая терапия уже не столь эффективна. Поэтому ранняя диагностика респираторных нарушений при заболеваниях легких – чрезвычайно актуальная проблема. Выявление и оценка выраженности тех или иных нарушений функции внешнего дыхания (ФВД) позволяет поднять диагностический процесс на качественно новый уровень и более адекватно оценить тяжесть заболевания.
Основные методы исследования ФВД
• исследование легочной диффузии;
• измерение растяжимости легких;
Если первые два метода могут считаться скрининговыми и обязательными для использования во всех лечебных учреждениях, осуществляющих наблюдение, лечение и реабилитацию легочных больных, то следующие три (бодиплетизмография, исследование диффузионной способности и растяжимости легких) являются более углубленными и дорогостоящими методами. Что же касается эргоспирометрии и непрямой калориметрии, то это довольно сложные методы, которые пока не применяются широко и которым еще только предстоит войти в повседневную клиническую практику.
Современные функциональные методы позволяют оценивать такие характеристики респираторной функции, как бронхиальная проводимость, воздухонаполненность, эластические свойства, диффузионная способность и респираторная мышечная функция. Хотя функциональных методов без учета клинической картины и других данных недостаточно для первичной постановки нозологического диагноза, они абсолютно необходимы легочным больным для оценки отдельных синдромов нарушения ФВД, наиболее распространенные из которых рассматриваются далее.
Нарушение бронхиальной проводимости
Критерии бронхиальной обструкции
Уменьшение просвета бронхиального дерева, проявляющееся ограничением воздушного потока – наиболее важное функциональное проявление легочных заболеваний. Общепринятые методы регистрации бронхиальной обструкции – спирометрия и пневмотахометрия с выполнением форсированного экспираторного маневра, когда после полного вдоха пациент делает максимально быстрый и полный выдох.
Основным критерием, позволяющим говорить о том, что у больного имеет место хроническое ограничение воздушного потока (бронхиальная обструкция), является снижение объема форсированного выдоха за 1-ю секунду (ОФВ1) до уровня, составляющего менее 70% от должных величин. Обладая высокой воспроизводимостью при правильном выполнении маневра, этот показатель позволяет документально зарегистрировать у пациента наличие обструкции и в дальнейшем мониторировать состояние бронхиальной проводимости и ее вариабельность. Бронхиальная обструкция считается хронической, если она регистрируется не менее 3 раз в течение 1 года, несмотря на проводимую терапию.
Очень важной проблемой является ранняя диагностика преимущественного поражения мелких бронхов диаметром менее 2–3 мм (Morrell N.W. et al, 1994), характерного для дебюта хронической обструктивной болезни легких (ХОБЛ). Оно очень долго не проявляется при спирометрии и при бодиплетизмографическом измерении сопротивления дыхательных путей. В этом случае более эффективным показало себя исследование парциальной кривой поток–объем [1]. Другой метод, который позволяет зарегистрировать поражение мелких бронхов, – определение внутригрудного компрессионного объема (Vcomp). Последний является той частью внутрилегочного объема воздуха, которая вследствие нарушения проводимости мелких бронхов во время форсированного экспираторного маневра подвергается компрессии. Vcomp определяется как разница между изменением легочного объема и интегрированным ротовым потоком.
Выявить нарушение бронхиальной проводимости, определить ее тяжесть и преимущественные уровни поражения – это начальный этап в программе постановки функционального диагноза при обструктивных заболеваниях. Следующим шагом является определение степени обратимости обструкции под действием бронхорасширяющих препаратов.
Для ответа на вопрос о том, является ли данная обструкция преимущественно обратимой или необратимой, обычно используют пробы с ингаляционными бронходилататорами и исследуют их влияние на показатели кривой поток–объем, главным образом на ОФВ1. Динамика форсированных экспираторных потоков на различных уровнях форсированной жизненной емкости легких (ФЖЕЛ) не может быть критерием обратимости, так как сама ФЖЕЛ, по отношению к которой рассчитываются эти потоки, изменяется при повторных тестах. В связи с этим другие показатели кривой поток–объем (за исключением ОФВ1), являющиеся в основном производными и расчетными от ФЖЕЛ, не рекомендуется использовать для оценки обратимости обструкции.
При обследовании конкретного пациента необходимо помнить, что обратимость обструкции – величина вариабельная и у одного и того же больного может быть разной в периоды обострения и ремиссии заболевания.
Бронходилатационный ответ на препарат зависит от его фармакологической группы, пути введения и техники ингаляции. Факторами, влияющими на бронходилатационный ответ, также являются назначаемая доза; время, прошедшее после ингаляции; бронхиальная лабильность во время исследования; состояние легочной функции; воспроизводимость сравниваемых показателей; погрешности исследования.
Хотя определение обратимости бронхиальной обструкции и считается рутинным исследованием для проведения дифференциального диагноза между бронхиальной астмой (БА) и ХОБЛ, тем не менее в нашей стране до сих пор отсутствуют общепринятые национальные стандарты по выполнению этой процедуры. В связи с этим в настоящее время приходится ориентироваться на документы и стандарты наиболее авторитетных и признанных в мире респираторных научных сообществ.
Поскольку БА в официальных документах функционально определяется как преимущественно обратимая обструкция, а ХОБЛ – как преимущественно необратимое или частично обратимое нарушение бронхиальной проводимости, то на первый план при определении и клиническом документировании обратимости обструкции выходят три фактора достоверности результатов проведения теста на обратимость:
1) выбор назначаемого препарата и дозы;
2) достижение критериев воспроизводимости как исходного, так и повторного теста;
3) способ расчета бронходилатационного ответа.
Выбор назначаемого препарата и дозы
Рабочая группа Ассоциации голландских специалистов по легочным заболеваниям в 1992 г. утвердила стандарты для проведения бронходилатационных тестов [2]. В соответствии с этим документом в качестве бронходилатационных агентов при проведении тестов у взрослых рекомендуется назначать:
• b2-агонисты короткого действия (сальбутамол – до 800 мкг, тербуталин – до 1000 мкг) с измерением бронходилатационного ответа через 15 мин;
• антихолинергические препараты (ипратропиума бромид до 80 мкг) с измерением бронходилатационного ответа через 30–45 мин.
Эксперты Британского торакального общества выработали рекомендации для проведения бронходилатационных тестов с использованием небулайзеров. При их осуществлении назначают более высокие дозы препаратов: повторные исследования следует проводить через 15 мин после ингаляции 2,5–5 мг сальбутамола или 5–10 мг тербуталина или же через 30 мин после ингаляции 500 мкг ипратропиума бромида.
Во избежание искажения результатов и для правильного выполнения бронходилатационного теста необходимо отменить проводимую терапию в соответствии с фармакокинетическими свойствами принимаемого препарата ( b2-агонисты короткого действия – за 6 ч до начала теста, длительно действующие b2-агонисты – за 12 ч, пролонгированные теофиллины – за 24 ч).
Достижение критериев воспроизводимости
Исследование считается воспроизводимым и завершенным, если пациенту удается выполнить три технически правильных попытки, при которых разница между максимальными и минимальными показателями ОФВ1 и ФЖЕЛ не превышает 5%.
Способ расчета бронходилатационного ответа
Способ расчета бронходилатационного ответа
Нет единого взгляда на интерпретацию результатов исследования обратимости бронхиальной обструкции из-за различия способов математического расчета [3].
Наиболее простой способ – измерение бронходилатационного ответа по абсолютному приросту ОФВ1 в мл [DОФВ1абс(мл) = ОФВ1дилат(мл) – ОФВ1исх(мл)]. Однако этот способ не позволяет судить о степени относительного улучшения бронхиальной проводимости, так как не учитываются величины ни исходного, ни достигнутого показателя по отношению к должному. Очень распространен метод измерения обратимости отношением абсолютного прироста показателя ОФВ1, выраженного в процентах к исходному [DОФВ1исх %]:
Но такая методика измерения может привести к тому, что незначительный абсолютный прирост будет в итоге давать высокий процент повышения в том случае, если у пациента исходно низкий показатель ОФВ1. Существуют также способ измерения степени бронходилатационного ответа в процентах по отношению к должному ОФВ1 [DОФВ1должн %]:
где ОФВ1исх – исходный параметр, ОФВ1дилат – показатель после бронходилатационной пробы, ОФВ1должн – должный параметр.
Выбор используемого индекса обратимости должен зависеть от клинической ситуации и конкретной причины, в связи с которой исследуется обратимость. Однако использование показателя обратимости, в меньшей степени зависящего от исходных параметров, позволяет осуществлять более корректный сравнительный анализ данных разных исследователей и лабораторий (Kerrebijn,1991; J. Van Noord и соавт., 1994). Несмотря на многообразие способов расчета бронходилатационного ответа, в большинстве случаев официальные рекомендации по этому вопросу предлагают способ расчета прироста по отношению к должным величинам ОФВ1.
Достоверный броходилатационный ответ по своему значению должен превышать спонтанную вариабельность, а также реакцию на бронхолитики, отмечаемую у здоровых лиц. Поэтому величина прироста ОФВ1, равная или превышающая 15% от должного, признана в качестве маркера положительного бронходилатационного ответа. При получении такого прироста бронхиальная обструкция документируется как обратимая.
Еще одной важной составляющей функционального диагноза и дифференциально-диагностическим критерием ХОБЛ и БА является степень нестабильности дыхательных путей, т.е. выраженность ответа на различные экзо- и эндогенные стимулы. Бронхиальная гиперреактивность, характерная для БА, хотя и определяется как неспецифическая, тем не менее, факторы, вызывающие ее, носят вполне конкретный специфический характер. Они условно могут быть разделены на три основные группы: 1) агенты, вызывающие бронхоспазм посредством прямого воздействия на гладкую мускулатуру (например, метахолин и гистамин); 2) факторы, оказывающие непрямое воздействие за счет высвобождения фармакологически активных веществ из секретирующих клеток, например, тучных (физические гипер- и гипоосмолярные стимулы) и немиелинизированных сенсорных нейронов (брадикинин, двуокись серы); 3) факторы, обладающие прямым и непрямым механизмом действия.
Для выявления бронхиальной гиперреактивности используется провокационный или бронхоконстрикторный тест (“challenge test”). В качестве бронхоконстрикторного агента при проведении тестов могут выступать фармакологические агенты (метахолин и гистамин), физические факторы (нагрузка, холодный воздух и др.) или сенситизирующие агенты (аллергены, профессиональные вредности). Выбор бронхоконстрикторного стимула определяется конкретной целью исследования. Для проведения клинических и эпидемиологических исследований фармакологические агенты (метахолин и гистамин) являются оптимальным выбором.
При выполнении методики во главу угла должны ставиться безопасность и надежность теста. Поэтому точную дозу или концентрацию провокационного агента необходимо знать не только для соблюдения методической точности, но и во избежание передозировки, способной вызвать тяжелый бронхоспазм. Стандартизация техники выполнения исследования позволяет не только получать воспроизводимые результаты внутри лаборатории, но и сравнивать данные различных лабораторий между собой при проведении многоцентровых исследований. Таким образом, проблема стандартизации и воспроизводимости этих методов – это проблема не только методическая, но и клиническая, так как от них в значительной степени зависит безопасность обследуемого пациента. При правильном проведении с учетом показаний и противопоказаний провокационные тесты достаточно безопасны для пациента.
Важным методом, позволяющим подтвердить диагноз ХОБЛ, является мониторирование ОФВ1 – многолетнее повторное спирометрическое измерение этого показателя. В зрелом возрасте в норме отмечается ежегодное падение ОФВ1 в пределах 30 мл в год. Проведенные в разных странах крупные эпидемиологические исследования позволили установить, что для больных ХОБЛ характерно ежегодное падение показателя ОФВ1 более 50 мл в год [4], в то время как для здоровых лиц и астматиков этот показатель не превышает 30 мл.
Изменение структуры статических объемов и эластических свойств легких
Бронхиальная проводимость характеризует лишь один, хотя и очень важный компонент респираторной функции. Бронхиальная обструкция в свою очередь может приводить к изменению воздухонаполненности (или структуры статических объемов) в сторону гипервоздушности легких. Основным проявлением гипервоздушности легких или увеличения их воздухонаполненности является увеличение общей емкости легких (ОЕЛ), полученной при бодиплетизмографическом исследовании или методом разведения газов.
Один из механизмов повышения общей емкости легких при ХОБЛ – снижение давления эластической отдачи по отношению к соответствующему легочному объему. В основе развития синдрома гипервоздушности легких лежит еще один весьма важный механизм. Повышение легочного объема способствует растяжению дыхательных путей и, следовательно, повышению их проводимости. Таким образом, возрастание функциональной остаточной емкости легких представляет собой своего рода компенсаторный механизм, направленный на растяжение и увеличение внутреннего просвета бронхов. Однако подобная компенсация идет в ущерб эффективности работы респираторных мышц вследствие неблагоприятного соотношения сила–длина. Гипервоздушность средней степени выраженности приводит к снижению общей работы дыхания, так как при незначительном повышении работы вдоха имеет место существенное снижение экспираторного вязкостного компонента [5].
Анатомически изменения паренхимы легких при эмфиземе (расширение воздушных пространств дистальнее терминальных респираторных бронхиол, деструкция альвеолярных стенок) функционально проявляются изменением эластических свойств легочной ткани – повышением статической растяжимости. Отмечается изменение формы и угла наклона петли давление–объем.
При рестриктивных легочных заболеваниях, напротив, происходит изменение структуры легочных объемов в сторону снижения общей емкости легких. Это происходит, главным образом, за счет уменьшения жизненной емкости легких. Эти изменения сопровождаются снижением растяжимости легочной ткани.
Нарушение диффузионной способности легких
Измерение диффузионной способности у больных легочными заболеваниями обычно выполняется на втором этапе оценки ФВД после выполнения форсированных спирометрии или пневмотахометрии и определения структуры статических объемов. Исследование диффузии применяется у больных рестриктивными и обструктивными заболеваниями, главным образом, для диагностики эмфиземы или фиброза легочной паренхимы [6, 7].
При эмфиземе показатели диффузионной способности легких – DLCO и ее отношения к альвеолярному объему DLCO/Va снижены, главным образом вследствие деструкции альвеолярно-капиллярной мембраны, уменьшающей эффективную площадь газообмена. Однако снижение диффузионной способности легких на единицу объема (DLCO/Va) (т.е. площади альвеолокапиллярной мембраны) может быть компенсировано возрастанием общей емкости легких (Standartization of lung function tests, 1993). Для диагностики эмфиземы исследование DLCO показало себя более информативным, чем определение легочной растяжимости [8], а по способности к регистрации начальных патологических изменений легочной паренхимы данный метод сопоставим по чувствительности с компьютерной томографией [9, 10].
У злостных курильщиков, составляющих основную массу больных ХОБЛ, и у пациентов, подвергающихся профессиональному воздействию окиси углерода на рабочем месте, отмечается остаточное напряжение СО в смешанной венозной крови, что может привести к ложно заниженным значениям DLCO и его компонентов [11].
Расправление легких при гипервоздушности приводит к растяжению альвеолярно-капиллярной мембраны, уплощению капилляров альвеол и возрастанию диаметра “угловых сосудов” между альвеолами. В результате общая диффузионная способность легких и диффузионная способность самой альвеолокапиллярной мембраны возрастают с объемом легких, но соотношение DLCO/Va и объем крови в капиллярах (Qc) уменьшаются. Подобный эффект легочного обьема на DLCO и DLCO/VA может приводить к неправильной интерпретации результатов исследования при эмфиземе.
При рестриктивных легочных заболеваниях характерно значительное снижение диффузионной способности легких (DLCO). Отношение DLCO/Va может быть снижено в меньшей степени из-за одновременного значительного уменьшения объема легких.
Нарушение физической работоспособности
В повседневной работе врач-клиницист сталкивается с проблемой, когда, несмотря на тщательно проведенные лабораторное и инструментальное исследование с оценкой функции внешнего дыхания в покое, бывает трудно определить общее функциональное состояние пациента, возможность его возвращения к привычному быту и прежним профессиональным обязанностям и назначить ему оптимальный реабилитационный режим [12]. Кроме того, не всегда есть возможность адекватно оценить эффективность проводимой терапии. Например, при проведении бронхолитической терапии иногда субъективная оценка не совпадает с объективно выявленным бронходилатационным эффектом, а также не во всех случаях удается выявить скрытое кардиотоксическое действие препарата, которое проявляется в чрезмерном увеличении ЧСС и электрокардиографических изменениях во время нагрузки.
Предложенные на сегодняшний день подходы к определению функционального класса легочных больных не учитывают таких важных факторов, как способность пациента к выполнению физической нагрузки и метаболический ответ на нее, исследование которых позволило бы во многих случаях более точно оценить функциональное состояние пациента и выявить тонкие механизмы ограничения физической работоспособности, скрытые от врача и исследователя при обычных исследованиях в состоянии покоя.
Вследствие того, что легочные заболевания сопровождаются снижением физической работоспособности и потребления кислорода [13, 14], роль нагрузочных тестов при проведении функциональных исследований все более возрастает. Кроме того, с каждым годом возрастает число больных легочной патологией с сопутствующими сердечно-сосудистыми заболеваниями. И в этих случаях требуется определить долевое участие респираторного и циркуляторного компонента в ограничении физической работоспособности, в соответствии с этим принимать индивидуальное решение о проводимой терапии и оценивать ее эффективность. Исследование во время физической нагрузки, моделируя стресс, может предоставить ценную информацию об адаптационных возможностях кардиореспираторной системы и тем самым позволить во многих случаях получить дополнительные данные об основном механизме возникновения одышки (диспноэ), происхождение которой иногда трудно установить при проведении исследований в состоянии покоя, характере изменений параметров вентиляции и конкретных метаболических условиях возникновения диспноэ у того или иного больного [15, 16].
Эргоспирометрическое иследование позволяет определить участие отдельных компонентов респираторной функции в ограничении физической активности. Однако для формирования более полного представления о функциональном состоянии пациента и формулирования развернутого и подробного функционального диагноза больного при легочной патологии необходимо ответить на следующие вопросы:
1) Проявляются ли во время нагрузки какие-либо нарушения респираторной функции, не выявляемые в покое?
2) Играют ли выявленные изменения какую-либо роль в ограничении физической активности?
3) Какой из компонентов респираторной функции играет первостепенную роль в ограничении физической активности?
Ответы на эти вопросы позволят выявить скрытые нарушения респираторной функции и определить, в какой мере эти нарушения могут влиять на качество жизни пациента.
Функциональная диагностика легочных заболеваний – это бурно развивающаяся область, быстро внедряющая самые последние технологические достижения. Общая тенденция современной медицины – тщательное протоколирование и максимально точный функциональный диагноз – приобретает при ведении больных обструктивными легочными заболеваниями все большее значение. У этой категории пациентов одной из основных целей проведения любых терапевтических и реабилитационных мероприятий является повышение функциональных возможностей больного к перенесению повседневных физических нагрузок, связанных с профессиональной деятельностью и бытом, улучшение качества жизни.
1. Garyard P., Orehek J., Grimaud C., Charpin C. Bronchoconstrictor effects of deep inspiration in patients with asthma. Am. Rev. Respir. Dis. 1975;111: 433–9.
2. Brand P., Quanjer P.H., Postma D.S. et al. and the Dutch Chronic Non-Specific Lung Disease (CNSLD) Study Group. Thorax 1992; 47: 429–36.
3. Van Noord J.A., Smeets J., Clement J. et al. Assessment of reversibility of airflow obstruction. Am. J. Respir. Crit. Care Med. 1994; 150 (2): 551–4.
4. Siafakas N.M., Vermeire P., Pride N.B. et al. Optimal assessment and management of chronic obstructive pulmonary disease (COPD). A consensus statement of the European Respiratory Society (ERS). Eur. Resp. J.1995; 8: 1398–420.
5. Wheatley J.R., West S., Cala S.J., Engel L.A. The effect of hyperinflation on respiratory muscle work in acute induced asthma. Eur. Respir.J. 1990, 3: 625–32.
6. Gelb A.F., Schein M., Kuei J., Tashkin D.P., Muller N.L., Hogg-J.C., Epstein J.D., Zamel N. Limited contribution of emphysema in advanced chronic obstructive pulmonary disease. Am.Rev.Respir. Dis. 1993; 147 (5): 1157–61.
7. Morrell N.W., Wignall B.K., Biggs T., Seed W.A. Collateral ventilation and gas exchange in emphysema. Am. J. Respir. Crit. Care Med. 1994; 150 (3): 635–41.
8. Morrison N.J., Abboud R.T., Ramadan F. et al. Comparison of single breath carbon monoxide diffusion capacity and pressure-volume curves in detecting emphysema. Am. Rev. Respir. Dis. 1989; 139: 1179–87.
9. Gould G.A., Redpath A.T., Ryan M. et al. Parenchymal emphysema measured by CT lung density correlates with lung function in patients with bullous disease. Eur. Respir. J. 1993; 6 (5): 698–704.
10. Stern E.J., Webb W.R., Gamsu G. Dynamic quantitative computed tomography. A predictor of pulmonary function in obstructive lung diseases. Invest. Radiol. 1994; 29 (5): 564–9.
11. Knudson R.J., Kaltenborn W.T., Burrows B. The effects of cigarette smoking and smoking cessation on the carbon monoxide diffusion capacity of the lung in asymptomatic subjects. Am. Rev. Respir. Dis. 1989; 140: 645–51.
12. Folgering H., Van-Herwaarden C. Pulmonary rehabilitation in asthma and COPD, physiological basics. Respir. Med. 1993; 87 (Suppl B): 41–4.
13. Carter R., Nicotra B., Blevins W., Holiday D. Altered exercise gas exchange and cardiac function in patients with mild chronic obstructive pulmonary disease. Chest. 1993; 103 (3): 745–50.
14. Wegner R.E., Jorres R.A., Kirsten D.K., Magnussen H. Factor analysis of exercise capacity, dyspnoea ratings and lung function in patients with severe COPD. Eur. Respir.J. 1994; 7 (4): 725–9.
15. Ross R. Interpreting Exercise Tests. Houston, CSI Software, 1989; 243.