Что такое болезнь пламмера
Что такое болезнь пламмера
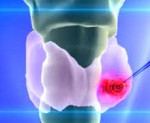
Болезнь провоцирует повышенная выработка тиреоидного гормона, вызывающая доброкачественную опухоль.
Причинами заболевания врачи считают такие факторы, как:
— Гиперсекреция тиропропина, которая вызывает увеличение размеров и кровенаполнения щитовидной железы.
— Расстройства регионарной симпатической иннервации, образующие трофический контур и нарушения работы сердца и нервной системы.
— Нарушение работы гипофиза, вызванное генетической мутацией.
— Воздействие токсических веществ на организм.
— Гормональный дисбаланс.
Чаще всего от токсической аденомы щитовидной железы страдают женщины в возрасте 40-60 лет. В особой группе риска находятся люди пожилого возраста, а также работники вредных производств. Болезнь также передается по наследству, поэтому людям, у которых от аденомы страдали родственники, следует быть внимательными к себе.
В Санкт-Петербурге, Гатчине, Луге, Выборге, Рощино и Светлогорске ведет прием кандидат медицинских наук, хирург-эндокринолог Виктор Алексеевич Макарьин. Вы можете обратиться к специалисту лично или назначить online-консультацию по скайпу. При необходимости пациенты могут записаться на УЗИ-исследования, биопсию щитовидной железы.
Желаем вам здоровья и, при необходимости, ждем на консультации!
Субкомпенсированная аденома
Болезнь проявляется незначительно, развивается медленно. Щитовидная железа функционирует нормально, поэтому пациент не придает значения токсической аденоме.
Декомпенсированная аденома
Признаки токсической аденомы щитовидной железы четко выражены, у каждого пациента болезнь проявляется индивидуально. Основным симптомом декомпенсированной болезни Пламмера является безболезненная маленькая опухоль круглой или овальной формы. Это неэстетичное образование смещается при глотании, чем создает больному дискомфорт.
Поставить диагноз «токсическая аденома щитовидной железы» может только врач-эндокринолог. Специалист назначает комплексное обследование, которое включает:
— Визуальный осмотр щитовидной железы;
— УЗИ щитовидной железы;
— Анализ крови на гормоны;
— Цитологический анализ клеток щитовидной железы (биопсия);
— Биохимический анализ крови;
— Сцинтиграфия (обследование щитовидной железы с помощью йода);
— Компьютерная томография щитовидной железы.
Ультразвуковое исследование может стать первым этапом лечения аденомы щитовидной железы. УЗИ на различных этапах болезни позволяет отличить опухоль от кисты. Как правило, врач назначает УЗИ в следующих случаях:
— При подозрениях на множественные новообразования;
— Для обследования беременных;
— Для дифференциальной диагностики кисты и аденомы;
— С целью контроля динамики заболевания;
— Для облегчения тонкоигольной аспирационной биопсии больших опухолей (ТАБ узла щитовидной железы, контролируемое УЗИ).
Сцинтиграфия щитовидки также помогает в лечении аденомы щитовидной железы, указывая на «холодные» и «горячие» образования в органе. После удаления опухолей обычно применяют магнитно резонансную томографию органа. Однако основным методом исследования остается тонкоигольная аспирационная биопсия узла щитовидной железы.
Лечение аденомы проводится хирургическим методом: проводится операция по удалению щитовидной железы. Возможно полное или частичное удаление органа. После операции пациенту назначают пожизненную заместительную гормональную терапию.
Перед операцией назначается медикаментозное лечение с целью подавления функции узловых образований. Как правило, пациентам прописывают такие лекарства, как:
При наличии серьезных противопоказаний к операции пациентам назначают консервативное лечение аденомы щитовидной железы:
— Лечение радиоактивным йодом;
— Введение этилового спирта в узел.
Послеоперационный период
Пациенту необходим психологический покой, полноценный сон. Важно соблюдать назначенную врачом диету.
Сразу после хирургического лечения аденомы щитовидной железы у пациентов могут наблюдаться такие неприятные симптомы, как:
— отеки и боли в горле;
— болевые ощущения в задней части шеи;
— опухание места шва.
Малоприятные симптомы указывают на нормальное проведение операции, они не должны пугать пациентов. Состояние улучшается через 15-20 дней, а на месте вмешательства остается только небольшой шрам.
Некоторые симптомы после операции должны насторожить пациента. Если после лечения аденомы щитовидной железы возникают такие проблемы, как нарушение голоса, хрипота, осиплость и общая слабость, обязательно стоит обратиться к лечащему врачу. В редких случаях операция провоцирует развитие ларингита.
Токсическая аденома
Токсическая аденома щитовидной железы
Причины
Точные причины формирования такого новообразования в тканях ЩЖ пока остаются неизвестными. Однако специалисты склонны полагать, что не последнюю роль в этом процессе играют:
Некоторые исследователи настаивают на том, что токсическая аденома ЩЖ также может стать следствием расстройств регионарной симпатической иннервации. У некоторых пациентов развитие данной болезни эндокринологи отметили после ранее диагностированного нетоксического узлового зоба.
Существует взаимосвязь между развитием токсической аденомы щитовидной железы и травмами шеи. Если у пациента имеются аутоиммунные заболевания, то его тоже включают в группу риска с высокой степенью вероятности возникновения такой опухоли.
Симптомы токсической аденомы
Болеют преимущественно женщины старше 40 лет. У мужчин данная патология встречается в несколько раз реже. Среди местных симптомов б-ни Пламмера – формирование одного или нескольких опухолевых узлов. Узлы округлые, плотные, не спаянные с окружающими тканями, диаметр их не превышает 3 см.
Диагностика токсической аденомы
В некоторых случаях увеличенные узлы в виде округлых образований можно обнаружить при пальпации (ощупывании) щитовидной железы. Среди инструментальных исследований – УЗИ и сканирование ЩЖ, в ходе которых обнаруживаются опухолевидные образования и «горячие» узлы, интенсивно поглощающие радиоактивный йод. Данные изменения служат показанием для аспирационной биопсии с последующим гистологическим исследованием содержимого узлов. Среди прочих диагностических методов – компьютерная и магнитно-резонансная томография.
При лабораторном исследовании обнаруживается избыток тироксина и трийодтиронина в крови. Иногда при декомпенсированном течении токсической аденомы повышение продукции тиреоидных гормонов ведет к торможению выработки передней долей гипофиза тиреотропного гормона.
Лечение токсической аденомы
Несмотря на то, что токсическая аденома протекает доброкачественно, существует опасность ее перерождения в рак щитовидной железы. Поэтому оптимальным способом лечения является оперативное вмешательство. Проводят резекцию ткани железы, содержащей патологический узел. В некоторых ситуациях альтернативой хирургическому вмешательству является лечение радиоактивным йодом. Этот йод интенсивно поглощается ЩЖ, и при этом разрушает аденоматозные клетки.
В качестве вспомогательной терапии применяются тиреостатики (средства, тормозящие продукцию тиреоидных гормонов), а также общеукрепляющие, белковые, иммуностимулирующие средства, витамины.
Болезнь Пламмера – это эндокринная патология, обусловленная развитием аденомы щитовидной железы, активно продуцирующей тиреоидные гормоны. Проявляется симптомами гипертиреоза: снижением массы тела, одышкой, слабостью, сонливостью, тахикардией, аритмией. В диагностический комплекс входит консультация и осмотр эндокринолога, УЗИ и сцинтиграфия щитовидной железы, анализ крови на тироксин, трийодтиронин и тиреотропный гормон. Лечение проводится хирургическими методами (реже медикаментозно), пациентам пожилого возраста показана терапия радиойодом, этаноловая склеродеструкция узлов щитовидной железы.
МКБ-10
Общие сведения
Болезнь Пламмера (тиреотоксическая аденома, токсический многоузловой зоб) получила свое название по фамилии американского физиолога, врача-эндокринолога Генри Стенли Пламмера. В 1913 году он опубликовал работу, в которой описал патологическое состояние, проявляющееся тиреотоксикозом, но лишенное некоторых классических признаков диффузного токсического зоба и отличное от него по механизмам происхождения. Заболеваемости больше подвержены женщины, гендерное соотношение составляет 4:1. Редкие случаи токсической аденомы регистрируются среди подростков и детей. Общие эпидемиологические показатели выше в эндемических по зобу областях.
Причины
Природа тиреотоксической аденомы полиэтиологична и не всегда может быть установлена достоверно. Считается, что основную роль в возникновении эндокринопатии играют соматические мутации клеток железы и внешние провоцирующие воздействия (интоксикации, ионизирующая радиация). Встречаемость изменений генов, ведущих к развитию синдрома, учащается в регионах с йодным дефицитом. Предположительно, мутации запускают активацию домена рТТГ в тироцитах независимо от силы естественных регулирующих сигналов гипофиза и аутоанатител к рецепторам ТТГ, определяемых при аутоиммунных триеопатиях. Мутации ТТГ-рецепторов, расположенных на эпителии щитовидной железы, приводят к гиперактивации отдельных секреторных клеток, которые начинают автономно и бесконтрольно продуцировать тиреоидные гормоны.
Патогенез
Болезнь Пламмера сопровождается тиреотоксикозом, который вызван избыточным производством йодированных гормонов клетками автономной аденомы. Ключевым звеном патогенеза являются мутации рецепторов тиреотропина, приводящие к их аутоактивации – способности усваивать большее количество йода и синтезировать тироксин (Т4), трийодтиронин (Т3) без регулирующего воздействия тиреотропного гормона. Развивается гиперплазия и гиперфункция отдельных эпителиальных клеток. В дальнейшем под воздействием факторов роста тироциты пролиферируют, формируя доброкачественную гормонально-активную эпителиальную опухоль – токсическую тиреоаденому. Еще один патогенетический механизм образования опухоли – изменения гена G-белка, повышающего функциональную активность отдельных фолликулов.
Тиреотоксикоз возникает преимущественно вследствие влияния трийодтиронина. Уровень ТТГ и тиролиберина остается нормальным либо снижается. При продолжительном течении заболевания подавляется выработка тиреотропина гипофизом – срабатывает закон обратной связи. На морфологическом уровне для болезни Пламмера характерно микрофолликулярное строение аденом. Если формируется многоузловое образование, параллельно с характерными микрофолликулярными опухолями могут возникать макрофолликулярные.
Симптомы болезни Пламмера
Отличительная особенность заболевания – преобладание в клинической картине нарушений сердечного ритма и миопатии. У пациентов определяется синусовая тахикардия и трепетание предсердий – кардиологические синдромы, которые субъективно переживаются как учащенное сердцебиение, дискомфорт, чувство тяжести или боль в области сердца. При тяжелом течении болезни появляется ощущение нехватки воздуха, одышка, слабость, головокружения, снижение работоспособности.
Тиреотоксическая миопатия проявляется мышечной слабостью, гипотрофией, дрожью, реже – миалгиями. Снижение тонуса диафрагмальной мышцы усиливает одышку. Привычная ранее физическая нагрузка становится непосильной. Офтальмологические расстройства представлены симптомом Грефе (отделение верхнего века от радужки при взгляде вверх) и симптомом Мебиуса (неспособность сфокусироваться на близко расположенных объектах).
Изменяется эмоциональное состояние больных: они становятся чрезмерно возбудимыми, эмоционально неуравновешенными, часто плачут, провоцируют конфликты, испытывают беспричинный страх и беспокойство. Снижается целенаправленность поведения, ускоряется речь и мыслительные процессы, но концентрация внимания ухудшается. Наблюдается суетливость, бессонница, тремор пальцев рук.
Увеличивается скорость метаболизма, поэтому больные испытывают приливы жара, часто потеют, плохо переносят жару и повышенную влажность воздуха, теряют вес, несмотря на то, что их аппетит усиливается, а калорийность рациона растет. Температура тела нормальная или повышенная до субфебрильных значений. Нарушаются половые функции: у мужчин снижается потенция, у женщин менструальный цикл становится нерегулярным, месячные кровотечения сопровождаются сильными болями, обмороками. У представителей обоих полов увеличивается риск бесплодия.
Осложнения
При разрастании аденомы и отсутствии лечения болезни Пламмера увеличивается риск перерождения доброкачественной опухолевой ткани в злокачественную. Фолликулы трансформируются в карциноматозные клоны, которые служат основой для развития рака щитовидной железы, особенно его агрессивных форм. По данным статистики, частота данного осложнения среди взрослых пациентов составляет от 2 до 5%. Другой проблемой являются побочные эффекты от лечения радиойодом. Патофизиологи предполагают, что такая терапия может служить провоцирующим фактором аутоиммунной тиреопатии, например, болезни Грейвса-Базедова, тиреоидита Хашимото. Сочетание этих заболеваний с болезнью Пламмера встречается в 2-4% случаев всех аутоиммунных патологий щитовидной железы.
Диагностика
Обследование пациентов проводит врач-эндокринолог. Основными диагностическими задачами являются определение тиреотоксикоза и дифференциация болезни Пламмера с клинически схожими аутоиммунными тиреопатиями – болезнью Грейвса, тиреоидитом Хашимото. Комплексное исследование включает следующие методы:
Лечение болезни Пламмера
Схема терапии всегда подбирается индивидуально. На сегодняшний день в клинической эндокринологии наиболее распространенными способами лечения аденомы являются консервативный, хирургический и радиоактивный. Целесообразность и безопасность того или иного вмешательства оценивается врачом индивидуально в зависимости от объемов опухоли, прогрессирования патологии, возраста пациента. Известны четыре тактических подхода:
Прогноз и профилактика
При своевременной диагностике и назначении адекватной терапии болезнь Пламмера не представляет опасности для здоровья и жизни пациента. Хирургическими и консервативными методами возможно полностью устранить опухоль и восстановить функции железистой ткани, а малигнизация аденом – достаточно редкое явление. Существует ряд мер, которые способны снизить вероятность развития данного заболевания. Рекомендуется придерживаться питания с достаточным поступлением йода, по назначению врача принимать йодсодержащие препараты, избегать ионизирующего облучения, поступления токсинов в организм.
Синдром Пламмера-Винсона — патологическое дисфагическое состояние, обусловленное сужением пищевода и атрофией эпителия верхних отделов ЖКТ на фоне железодефицитной анемии. Проявляется затруднениями глотания в сочетании с бледностью кожи и слизистых, головокружениями, болезненностью и покраснением языка, трещинами в углах рта, сухостью кожи, деформацией ногтевых пластин. Диагностируется с помощью общего анализа крови, определения уровней железа, ферритина, проведения эзофагоскопии, рентгенографии пищевода. Для лечения используют препараты, содержащие железо, В-витаминные комплексы. При стойкой обструкции выполняют баллонную дилатацию, бужирование пищевода.
МКБ-10
Общие сведения
Сидеропеническую дисфагию (болезнь Пламмера-Винсона, синдром Келли-Паттерсона) в 1911-1919 годах независимо друг от друга описали американские физиологи Г.С. Пламмер, П.П. Винсон и британские ларингологи Д.Р. Паттерсон, А. Браун-Келли. Заболеванию более подвержены белые женщины климактерического возраста, хотя известны случаи диагностики синдрома у подростков и даже детей. Патология выявляется крайне редко, самые высокие показатели заболеваемости отмечались в XX столетии на территории скандинавских стран. Уменьшение распространенности сидеропенической дисфагии связано с улучшением питания и эффективной медикаментозной коррекцией железодефицитных состояний. Актуальность своевременной диагностики расстройства обусловлена высоким риском развития сопряженного рака пищевода.
Причины синдрома Пламмера-Винсона
Хотя заболевание стойко ассоциировано с железодефицитной анемией и гипосидерозом, его этиология на сегодняшний день окончательно не установлена. С учетом характерных патоморфологических и клинических проявлений специалистами в сфере гастроэнтерологии, гематологии, иммунологии предложено несколько теорий происхождения сидеропенической дисфагии:
В качестве предпосылок к развитию расстройства рассматривается неполноценное питание, наследственная несостоятельность ферментов, участвующих в метаболизме железа, заболевания, сопровождающиеся хронической кровопотерей (метроррагии, геморрой, язвенная болезнь и др.), нарушение всасывания макроэлементов, витаминов при ахилии, энтеритах, другой патологии ЖКТ. У пожилых пациентов определенную роль могут играть инволюционные нарушения утилизации железа.
Патогенез
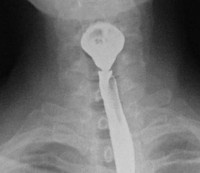
Механизм развития синдрома Пламмера-Винсона продолжает изучаться. Считается, что патогенез сидеропенической дисфагии основан на системных изменениях в тканях, связанных с железо-витаминной недостаточностью. В эпителиальной оболочке пищеварительных органов происходят гиперкератические и атрофические процессы, приводящие к сухости и истончению слизистых. Ситуация усугубляется повреждением железистой ткани с апоптозом секретирующих клеток, эпителиоцитов выводных протоков желез, выделением более густого секрета. В результате в верхнем отделе пищевода образуются небольшие липкие пленки (пищеводные мембраны), которые задерживают продвижение твердой части пищи и провоцируют спастическое сокращение мускулатуры. Атония дистальной части пищеводной трубки, вызванная низким содержания миоглобина в мышечных клетках, нарушает эзофагеальную перистальтику и препятствует нормальному прохождению пищевого комка.
Симптомы синдрома Пламмера-Винсона
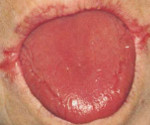
Клиническая картина заболевания развивается постепенно. Вначале возникают признаки анемического синдрома: бледность кожи, слизистых оболочек, быстрая утомляемость, головные боли и головокружение, нечеткость зрения, учащение пульса, снижение артериального давления. Типичные симптомы сидеропенической дисфагии — воспалительная атрофия слизистой оболочки языка, которая проявляется его покраснением, жжением, сглаженностью, сухостью, болезненностью при пережевывании пищи. Характерно выделение небольшого количества вязкой слюны, появление чувствительных трещин в углах губ (ангулярный хейлит). У многих пациентов выявляется кератоконъюнктивит, кожа становится сухой, ногти — ложкообразными, отмечаются признаки себореи. При прогрессировании заболевания обнаруживается дисфагия (нарушение глотания) вначале твердой, а затем и жидкой пищи. Возможны боли и тяжесть в левом подреберье, обусловленные увеличением селезенки. Типично сезонное обострение синдрома в весенний период.
Осложнения
При тяжелом течении симптомокомплекса Пламмера-Винсона у пациентов наблюдается стремительная потеря массы тела вплоть до кахексии, что вызвано невозможностью проглатывания пищи из-за значительного сужения пищевода. Длительное белково-энергетическое голодание ведет к дистрофическим изменениям в мышцах и внутренних органах. При выраженном снижении уровня гемоглобина может возникать анемическая кома, вызванная недостаточным поступлением кислорода в структуры головного мозга. При вовлечении в атрофический процесс слизистой желудка развивается гастрит с пониженной кислотностью, усугубляющий расстройства пищеварения. Наиболее опасное осложнение синдрома, выявляющееся у 3-15% больных, — плоскоклеточный рак пищевода, глотки, реже наблюдаются злокачественные неоплазии дыхательных путей.
Диагностика
Постановка диагноза может представлять затруднения вследствие неспецифичной клинической картины и низкой распространенности заболевания. О возможном наличии синдрома Пламмера-Винсона свидетельствует сочетание дисфагии с сидеропенической анемией и сужением пищевода. Наиболее информативными в диагностическом плане являются:
Для исключения других причин анемического синдрома может назначаться исследование клеточного состава костного мозга (миелограмма). Для обнаружения структурных изменений при выраженной спленомегалии производят УЗИ селезенки. Дифференциальную диагностику проводят с дивертикулами и злокачественными опухолями пищевода, кардиоспазмом, эзофагоспазмом, ахалазией пищевода, склеродермией, стриктурами органа после термических или химических ожогов, грыжей пищеводного отверстия диафрагмы, новообразованиями средостения, наследственными формами анемий, синдромом функциональной дисфагии, болезнью Меллера-Гунтера. Кроме осмотра гастроэнтеролога пациенту рекомендованы консультации онколога, хирурга, оториноларинголога, терапевта, гематолога, невролога, иммунолога, ревматолога.
Лечение синдрома Пламмера-Винсона
Тактика ведения пациента основана на вероятных причинах и механизмах развития заболевания. Обычно стойкого терапевтического эффекта удается достичь консервативными методами и изменением рациона с употреблением достаточного количества белка, продуктов, содержащих витамины группы В. Рекомендованная схема лечения включает следующие лекарственные средства:
При наличии сведений о патологических состояниях, осложнившихся анемией и сидеропенией, этиопатогенетическая терапия основного заболевания проводится по соответствующим протоколам лечения. Пациентам со стойкой дисфагией и выраженной эзофагеальной обструкцией для разрыва пленок, устранения спазма выполняется бужирование или баллонная дилатация пищевода.
Прогноз и профилактика
Исход заболевания зависит от выраженности структурных изменений пищевода и наличия функциональных расстройств других органов. Прогноз относительно благоприятный, после проведения комплексного лечения у большинства пациентов с расстройством Пламмера-Винсона наступает выздоровление. Меры профилактики заболевания неспецифичны, предусматривают соблюдение сбалансированной диеты, употребление продуктов с высоким содержанием железа и витамина С, посильные физические нагрузки, отказ от вредных привычек. Для предупреждения развития осложнений все больные, перенесшие синдром сидеропенической дисфагии, после выздоровления подлежат длительному диспансерному наблюдению.
Тиреотоксикоз с токсическим одноузловым зобом (E05.1)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Примечание. В большинстве литературных источников тиреотоксикоз с токсическим одноузловым зобом описывается под названием «тиреотоксическая аденома», поэтому именно этот термин будет использоваться при дальнейшем описании заболевания.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
Гистологически удаленная аденома состоит из скопления дифференцированных фолликулярных клеток, выстланных гиперплазированным эпителием (фолликулярная аденома).
Тиреотоксическая аденома, как правило, инкапсулирована и доброкачественна. Злокачественное перерождение автономно функционирующих узлов ЩЖ встречается редко. По некоторым данным, такая трансформация аденомы встречается у 2% взрослых (M.Smith и соавт., 1988) и у 11% детей (R.D.Croom и соавт., 1987).
Эпидемиология
Факторы и группы риска
Клиническая картина
Cимптомы, течение
Клиническая картина тиреотоксической аденомы характеризуется симптомами тиреотоксикоза, сходными по клинике с диффузным токсическим зобом:
— снижение массы тела при отсутствии изменения в питании;
— учащенное сердцебиение, сохраняющееся в покое и во сне;
— мышечная слабость;
— плохая переносимость жары;
— потливость;
— раздражительность.
При тиреотоксической аденоме данные симптомы менее выражены, а само заболевание имеет медленное развитие; долгое время больные наблюдаются у эндокринолога по поводу узлового зоба.
Развитие опухоли происходит медленно. Когда она достигает крупного размера, то может сдавливать органы шеи. Единственными жалобами у пожилых пациентов могут быть учащенное сердцебиение и одышка при физической нагрузке, слабость, сонливость или бессонница.
Диагностика
Диагноз тиреотоксической аденомы устанавливается на основании следующих результатов исследований:
1. Опрос и осмотр больного. При пальпации щитовидной железы выявляется увеличение одной из ее долей, наличие узла. Узловое образование имеет эластичную консистенцию, округлую форму с отчетливыми краями и гладкой поверхностью, различную плотность; смещается при глотании.
2. Исследование содержания в крови гормонов щитовидной железы:
— наблюдается значительное повышение количества Т3 при умеренно повышенном или нормальном уровне Т4;
— количество ТТГ может быть нормальным или сниженным;
— тиреоидстимулирующие антитела не определяются.
4. УЗИ щитовидной железы: обнаруживается узловое образование.
5. Биохимический анализ крови: выявляются признаки нарушения белкового, жирового и углеводного обмена.
Лабораторная диагностика
Дифференциальный диагноз
Тиреотоксическая аденома наиболее часто дифференцируется со следующими заболеваниями:
1. Диффузный токсический зоб. Отличия от тиреотоксичекой аденомы:
— развивается в более молодом возрасте (ранее 50 лет);
— более короткий анамнез;
— диффузное увеличение щитовидной железы;
— равномерное поглощение радиофармпрепарата;
— в 30-50% случаев наблюдается эндокринная офтальмопатия;
— в 70-80% случаев выявляется высокий титр антител к рецепторам ТТГ, кроме того, могут определяться антитела к пероксидазе тиреоцитов и тиреоглобулину;
— на УЗИ отмечаются диффузное снижение эхогенности ткани ЩЖ, отсутствие узловых образований.
2. Многоузловой токсический зоб: при сцинтиграфии выявляются как «горячие», так и «холодные» узлы.
3. Рак ЩЖ (высокодифференцированная аденокарцинома). Как правило, протекает в эутиреоидном состоянии. Различить цитопатологическую картину, наблюдаемую при токсической аденоме и раке ЩЖ, весьма трудно. Поэтому в данной ситуации тонкоигольная биопсия не помогает проведению дифференциальной диагностики.
В тех случаях, когда имеется «горячий» узел и происходит поглощение радиоизотопа в прилегающих областях при нормальной концентрации ТТГ в сыворотке крови, необходимо провести пробу с назначением Т3 (25 мкг 4 раза в день, в течение 10 дней). При повторном сканировании будет четко видно, что в окружающих «горячий» узел областях поглощения радиоизотопа отсутствуют в связи с ингибированием под влиянием экзогенного Т3 секреции ТТГ.
Осложнения
Лечение
2. Тиреостатики (мерказолил, тиразол, пропицил) назначают только в качестве подготовки к операции и терапии радиоактивным йодом.
3. Операция показана при тиреотоксической аденоме с объемом автономной ткани более 3 см в диаметре, узловом, многоузловом токсическом зобе.
4. В остальных случаях (у больных в возрасте старше 40 лет), а также при противопоказаниях к операции проводят терапию радиоактивным йодом (300-400 г).
5. Пациенту необходимо обеспечить психический покой, полноценный сон. Больным нельзя находиться на открытом солнце. Назначается диета с большим содержанием белка в пище, витаминов. Иногда назначаются бета-адреноблокаторы.