Что такое биопленка в стоматологии
Что такое биопленка в стоматологии
Важным аспектом каждодневной деятельности стоматолога-эндодонтиста является, на мой взгляд, четкое понимание биологии происходящих процессов. Долгие годы многие такие аспекты, как микробиология или иммунология, казались очень далекими от клинической работы. Накопленные сегодня знания подталкивают нас к изменению наших клинических решений. Одна из наиболее изучаемых и дискутируемых сегодня тем — это тема биопленки.
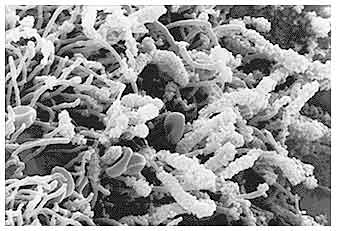
Биопленка — это конгломерат колоний микроорганизмов, которые погружены во внеклеточный матрикс и прикреплены к поверхности. Микроколонии занимают примерно 15% от общей массы биопленки.
Экстрацеллюлярный матрикс, состоящий из экзополисахаридов, выделяемый микробами и несущий важные функции в жизнедеятельности биопленки, занимает 85% массы биопленки. Несмотря на название биопленка не является однородной субстанцией, она гетерогенна в пространстве и во времени, сквозь биопленку проходят водные каналы, несущие питательные вещества и вымывающие продукты жизнедеятельности микроорганизмов.
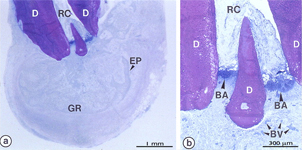
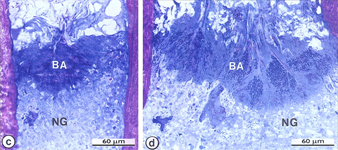
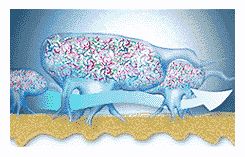
Экстрацеллюлярный матрикс является мощным биологическим клеем, с помощью которого биопленка прочно прикрепляется к поверхности. В области стоматологии речь идет о эмали зубов, если мы обсуждаем начальный кариес, и о поверхности корня, если говорим о патологии пародонта, в области эндодонтии мы говорим о биопленке, прикрепляющейся к поверхности дентина канала корня.
Кроме того, экстрацеллюлярный матрикс может являться и питательным субстратом для бактерий. Кстати, в эндодонтии биопленка была описана уже в 1987 году Nair P. как конгломерат микробов различной формы, погруженный в экстрацеллюлярный аморфный матрикс [1], однако термин «биофильм» в то время не звучал, и на это наблюдение не обратили внимание.
Сегодня медики уверены, что более чем в 80% случаев инфекционные поражения организма проходят в форме биопленочной инфекции. В такой ситуации предложение Nair P. «относиться к хроническому апикальному периодонтиту, как к инфекционному заболеванию, вызванному внутриканальной биопленкой» абсолютно логично [2].
Чем же так интересна эта структура? Внутри биопленки создаются уникальные условия с точки зрения взаимодействия между микроорганизмами: близкий контакт позволяет резко усилить обмен генетической информацией, соответственно, образование резистентных штаммов микроорганизмов происходит намного быстрее, чем у микроорганизмов, находящихся в форме планктона.
Между колониями микробов возникает свой язык общения по типу феромонов: сигнальные молекулы вызывают изменение в поведении микроколоний и влияют на скорость размножения микробов и проявления тех или иных фенотипических свойств [3]. И наконец, внутри биопленки возникают сложнейшие пищевые цепочки, где продукты жизнедеятельности одних микроорганизмов являются основой для существования других. Экстрацеллюлярный матрикс защищает микробов от воздействия внешних факторов, к которым относятся и наши попытки их уничтожения.
Как выяснилось, большинство международных микробиологических исследований изучало микробов в форме планктона, и поэтому часто исследователи не понимали, в чем такая большая разница результатов исследований in vitro и конечного эффекта in vivo. Характерным примером являются данные о возможной разнице резистентности микробов к амоксициллину в форме планктона и биопленки в 1000 раз [4].
Понимание взаимодействия микробов в биопленке помогает нам ответить на старый вопрос микробиологов: все ли микробы, что мы находим в инфицированном канале, нужны для возникновения апикального периодонтита или есть главные игроки, а часть микробов просто попала в канал и никакой роли в патогенезе не играет? Учитывая наши знания о биопленке, мы понимаем, что безобидные, на первый взгляд, микробы несут такие важные функции, как образование экстрацеллюлярного матрикса, и являются незаменимыми в пищевых цепочках [5]. Все эти данные рисуют непростую картину борьбы с инфекционными заболеваниями как в области общей медицины, так и в стоматологии. Наиболее логичным путем является механическое удаление биопленки с поверхности.
В терапевтической стоматологии мы часто совмещаем удаление биопленки с подлежащей поверхности. Пародонтологи уже много лет говорят о необходимости качественного удаления зубного камня и полировки корня как об основе любого пародонтологического лечения. Абсолютно естественно, что мы акцентируем наше внимание на инструментальной обработке канала как на основном этапе борьбы с биопленкой. Однако данные последних десятилетий неутешительны: даже при агрессивной обработке канала при использовании вращающихся никель-титановых инструментов 25—35% поверхности каналов остаются необработанными [6]. Мы не должны забывать, что основной целью инструментальной обработки канала является придание ему формы, а за очистку в основном ответственны ирригация и внутриканальная антисептическая обработка.
С вхождением в обиход термина «биопленка» многие исследователи начали поиски антидотов. Различают два основных направления: поиск новых методик и средств и проверка старых известных игроков на поле боя с инфекциями в новых лабораторных условиях. Одно из самых интересных направлений — фотоактивируемая дезинфекция (PTD, PAD). Эта процедура была разработана в области онкологии: нетоксичные маркеры, называемые фотосенситайзерами, наносились на злокачественные или предраковые ткани и затем активировались низкоэнергетическим лазером, вследствие чего образовывался активный кислород и свободные радикалы, приводящие к гибели раковой клетки [7].
В эндодонтии корневой канал прокрашивается, как правило, метиленовым синим или толуидиновым синим, и эти фотосенситайзеры прикрепляются к наружной поверхности микробов. После этого канал облучается низкоэнергетическим лазером (CO2) с длиной волны 665 нм. Данная процедура вызывает уничтожение бактерий. Естественно, что если бактерии находятся в форме планктона, такая система работает со 100%-ной эффективностью, но биопленка не позволяет красителям достичь внутренних слоев, и поэтому многие исследователи [8] показывают невозможность полного уничтожения микробной биопленки такими системами и как вывод пишут о создании мощной дополнительной антибактериальной системы, но не альтернативной [9].
Другие новые направления, такие как электрохимически активированная вода [10] или озоновые системы [11], к сожалению, показали свою несостоятельность в борьбе с биопленкой. Группы исследователей, изучающих взаимодействие между «старыми» ирригантами и биопленкой, пришли к однозначному выводу, что лучшим является раствор гипохлорита натрия [12, 13].
Огромное значение играет его способность растворять органический матрикс, в данной ситуации это растворение экстрацеллюлярного матрикса биопленки, и за счет этого — проникновение NaOCl в глубокие слои биопленки. Без ирригации NaOCl современная качественная эндодонтия невозможна. И естественно, что методики, повышающие эффективность ирригаций NaOCl, — в центре внимания исследователей. Рекомендую обратить ваше внимание на направление пассивной ультразвуковой ирригации. На базе научных данных о том, что Ca(OH)2 обладает свойством растворять органическую ткань [14], можно предположить, что его использование в случаях с зубами со сложным анатомическим строением и хроническими инфекционными состояниями тоже имеет смысл.
В будущем наиболее интересное решение — это поиск биологических методов борьбы с инфекцией, в основе которых будет лежать расшифровка языка микробов и управление биопленкой путем использования сигнальных молекул или воздействие на ключевые бактерии с точки зрения функционирования биопленки.
Итак, мы должны продолжать внимательно изучать новые данные о биопленке, следя за достижениями не только исследователей в области стоматологии, но также экстраполировать достижения микробиологов и общих врачей в нашу специальность. При анализе современных исследований, описывающих результаты антибактериального воздействия тех или иных препаратов, следует обращать внимание на то, проверялись ли эти материалы, методики на биопленке или нет.
Биопленка
Яркая реклама, огромное количество информации в интернете, рассказы друзей…
И, все таки: зачем нужна эта, на первый взгляд, простая процедура?
Мы привыкли слышать: зубные камни, налет…
Стоматолог – профессионал работает с понятием биопленка.
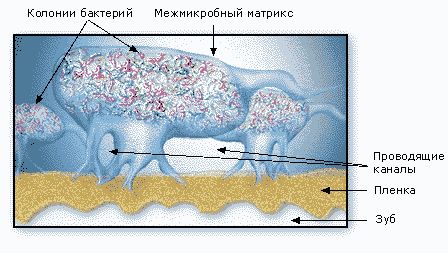
Биопленка — это хорошо организованное, взаимодействующее сообщество микроорганизмов. Микроорганизмы собраны в микроколонии, которые в свою очередь окружены защитным матриксом (барьером).
Матрикс пронизан каналами, по которым циркулируют питательные вещества, продукты жизнедеятельности, ферменты, метаболиты и кислород. Эти микроколонии имеют свои микросреды, отличающиеся уровнями рН, усваиваемостью питательных веществ, концентрациями кислорода. Бактерии в биопленке общаются между собой посредством химических раздражений (сигналов). Эти химические раздражители вызывают выработку бактериями потенциально вредных белков и ферментов.
Теперь становиться понятно, почему антимикробные средства как общего действия, так и применяемые местно, не всегда дают успешные результаты, даже тогда, когда они нацелены на конкретный вид микроорганизмов.
Барьер, защита, конгломерат – биопленка.
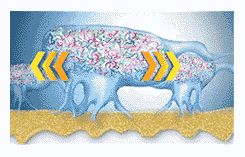
Это также помогает объяснить, почему механическое удаление бляшек и личная гигиена ротовой полости продолжают оставаться неотъемлемой составной частью лечения и профилактики заболеваний пародонта и болезней твердых тканей зуба.
Биопленка полости рта
Доминирующее положение среди обитающих в ротовой полости микроорганизмов занимают бактерии. А в результате их жизнедеятельности образуются кислоты, провоцирующие развитие кариеса и заболевания пародонта.
(!) Чтобы снизить риск развития кариеса, рекомендуется использовать средства ухода за полостью рта, содержащие Ксилит и Эритрол, – ополаскиватели, зубные пасты, жевательные резинки и т.д.
На сегодняшний день установлено, что более чем в 80% случаев инфекционные поражения организма проходят в форме биопленочной инфекции. В человеческом организме все взаимосвязано. Очаг инфекции в ротовой полости не только грозит разрушением зуба и поражением пародонта, но и наносит вред здоровью внутренних органов, поскольку болезнетворные бактерии могут распространяться по всему организму гематогенным путем (через кровь), а также запускать ряд патологических иммунологических реакций.
В форме биопленки образование резистентных штаммов микроорганизмов происходит намного быстрее, потому что на первый взгляд безобидные микробы образуют экстрацеллюлярный матрикс, который защищает их от внешних воздействий, в том числе лечебных манипуляций. Микроорганизмы в биопленке полости рта устойчивы к антибиотикам, антимикробным средствам и реакции организма хозяина.
Современные исследования подтверждают, что биопленка может приводить к:
Кроме того, именно она становится причиной развития отдаленных воспалительных осложнений имплантации (музозит, периимплантит). Комплекс «имплант-челюсть» обладает меньшими резервами, по сравнению с комплексом «зуб-челюсть». И на гистологическом уровне периимплантит характеризует более сильное воспаление, чем пародонтит.
В связи с этим Швейцарской Стоматологической Академией (SDA) рекомендовано механически удалять биопленку полости рта с помощью процедуры профессиональной гигиены. Для этого в 2018 году был разработан протокол Guided Biofilm Therapy (GBT). Он основан на принципах:
Guided Biofilm Therapy (GBT) предполагает регулярный контроль и удаление зубных отложений (налета и камня) методами индивидуальной и профессиональной гигиены ротовой полости. В стоматологическом отделении центра клинической постурологии профессора Бугровецкой для этих целей используется самый современный аппарат – Air Flow Prophylaxis Master.
Мы практикуем комплексный подход для эффективного лечения пациентов со стоматологическими, неврологическими, двигательными и другими проблемами.
Не откладывайте визит к врачу при появлении жалоб! –
Лечение в нашей клинике проходит максимально комфортно и быстро.
Биопленка: новый взгляд на бляшку
Памелла Р. Оверман
В течение последних 120 лет исследователи-стоматологи пытались понять микробную природу болезней ротовой полости. Их взгляды на зубную бляшку и составляющие ее микроорганизмы менялись от гипотез о специфичности бляшки к предположениям об ее неспецифичности и снова возвращались к теории о наличии специфических пародонтальных патогенов в бляшке. Изменения во взглядах на бляшку и образующие ее микроорганизмы влияют на стратегию профилактики заболеваний пародонта и контроля за ними. В последние годы некоторые исследователи-стоматологи стали рассматривать бляшку как биопленку. Такое изменение взгляда на бляшку является важной основой будущих усилий по профилактике и лечению. Данная статья освещает различные, менявшиеся с годами представления специалистов-стоматологов о бляшке, выдвигая на первый план современный взгляд на бляшку как на биопленку, и описывает разновидности терапии болезней пародонта.
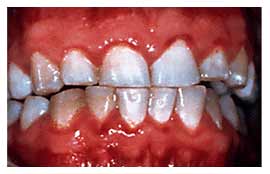
Несмотря на усилия специалистов-стоматологов, инфекции ротовой полости по-прежнему широко распространены. Среднестатистический взрослый американец имеет от 10 до 17 разрушенных, удаленных или запломбированных постоянных зубов. Большинство жителей США болели гингивитом, меньшая часть страдает умеренно выраженными или тяжелыми формами заболеваний пародонта (рис. 1).
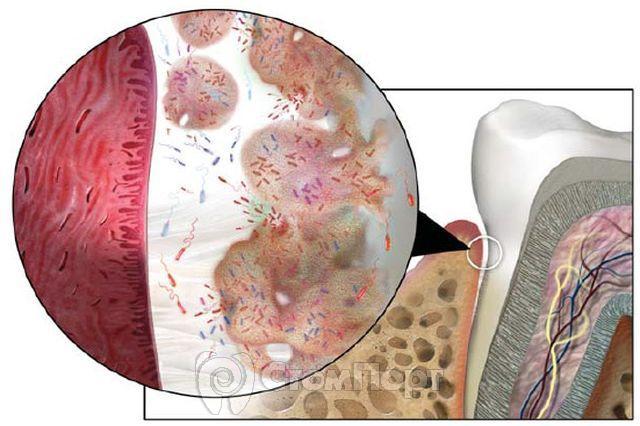
Общепризнанно, что микрофлора ротовой полости является многообразной и наличие специфических бактерий во внутриротовой бляшке рассматривается как необходимая, но недостаточная причина возникновения заболевания. До конца не ясно, как именно микроорганизмы бляшки (рис. 2) вызывают заболевания ротовой полости.
Компоненты зубной бляшки и входящие в нее микроорганизмы изучаются с помощью аналитического оборудования, и полученные результаты влияют на стратегию контроля и профилактику заболеваний зубов. За последние два десятилетия современные научные методы изменили взгляд на зубную бляшку, и сейчас многие ученые-стоматологи рассматривают ее как биопленку.
Биопленка
Биопленка — это хорошо организованное, взаимодействующее сообщество микроорганизмов. Классическим примером биопленки может служить тонкое наслоение на скалах, находящихся посреди течения. Подобные бляшки образуются и в ротовой полости. В природе биопленки распространены повсеместно. Они формируются в условиях текучести. Установлено, что свыше 95% существующих в природе бактерий находятся в биопленках. Иногда биопленки могут быть полезными, например, их применяют для обеззараживания отработанных и сточных вод.
Тонкое наслоение, формирующееся на зубах,— пример, знакомый большинству специалистов-стоматологов. Биопленки выстилают нефтепроводы, аквариумы, постоянные катетеры, внутренние имплантаты, контактные линзы и протезы (рис. 3).
Биопленки могут оказаться смертоносными. Болезнь легионеров, унесшая жизни 29 человек в Филадельфии в 1976 г., в конечном счете оказалась связанной с бактериями биопленки в системе кондиционирования воздуха. Миллионы долларов ежегодно расходуются на работы по контролю за этими биопленками.
Изменение взглядов на бляшку
Национальный институт стоматологических и черепнолицевых исследований недавно проводил международную конференцию по микробной экологии. Эта встреча сосредоточила внимание на новом взгляде на бляшку как на биопленку. Конференция подчеркнула важность изменения мнения о зубной бляшке и ее роли в развитии заболеваний ротовой полости. Такая смена взглядов стоматологов на бляшки происходит не впервые, за последние 120 лет эти воззрения претерпели различные изменения.
Период с 1880 по 1930 получил название золотого века микробиологии. За это время были дифференцированы возбудители многих важнейших системных инфекций. Исследователи также искали единственную специфическую причину заболеваний ротовой полости. Предполагая, что бляшка содержит специфический микроорганизм, вызывающий заболевания пародонта, ученые-стоматологи исследовали бляшки в поисках этого возбудителя. Используя доступные в то время методики (микроскопию влажных и окрашенных мазков), ученые идентифицировали различные группы потенциальных возбудителей заболеваний пародонта.
У пациентов с заболеваниями пародонта были выделены амебы, спирохеты, веретенообразные бактерии и стрептококки, считавшиеся, таким образом, потенциальными возбудителями. Лечение болезней пародонта в то время различалось в зависимости от предполагаемых причин заболевания и включало красители, систематическое применение мышьяксодержащих антимикробных препаратов, внутримышечные инъекции препаратов ртути, а также вакцины.
1930-е годы возвестили о новом взгляде на роль бляшки и ее микроорганизмов в этиологии заболеваний пародонта. Ученые-стоматологи предположили, что заболевания пародонта связаны с неким конституциональным дефектом индивидуума. Считалось, что механические раздражители, такие как камни и нависающие края реставраций, также играют важную роль в патогенезе заболеваний пародонта.
На смену уверенности в наличии единственного микробного возбудителя заболеваний пародонта пришли теории неспецифичности бляшек. Гипотеза о неспецифичности бляшки предполагала, что в деструкции пародонта играет роль скорее вся бактериальная флора бляшки, чем специфические бактерии одного вида. Вся бляшка рассматривалась как патогенная. Кроме того, наличие бляшки означает отягощенное течение заболевания. Контроль за бляшками считался необходимым для ограничения производства веществ, раздражающих десны и приводящих к воспалению и разрушению пародонта. Идентификация специфических микроорганизмов была не важна, важен был строгий контроль за бляшками, и это стало центральным моментом в терапии болезней пародонта.
1960-е отмечены возвращением к гипотезе о специфичности бляшки. Исследователи успешно показали возможность передачи заболеваний пародонта между хомяками. Электронная микроскопия подтвердила наличие спирохет в соединительной и эпителиальной тканях пациентов с острым язвенно-некротическим гингивитом в противоположность здоровым лицам контрольной группы. Допустив, что вызванные разными видами микробов бляшки отличаются друг от друга, ученые снова вернулись к поиску специфического микробного пародонтального возбудителя и лечения, нацеленного на причинный фактор.
Новейшие методы микробиологических исследований, такие как микроскопия в затемненном поле, трансмиссионная электронная микроскопия, сканирующая электронная микроскопия, исследования ДНК и иммунологический анализ помогли в исследованиях.
С тех пор ученые продолжают поиски специфического этиологического агента с переменным успехом. Haffajee и Socransky подробно описали причины, затрудняющие точное указание специфических патологических агентов. Некоторые из этих трудностей относятся к процессу отбора микробиологических проб и их культивированию. Эти проблемы включают: получение образца из пародонтального кармана, трудности культивирования некоторых микроорганизмов и большое количество пародонтальных патогенных микроорганизмов, которые могут быть обнаружены в пародонтальном кармане и затем выращены. Забор проб еще более усложняется тем фактом, что в пародонтальном кармане содержатся не только патогенные, но и сапрофитные виды микрофлоры.
Другая группа проблем в точном определении возбудителей болезней пародонта относится к самой природе этих заболеваний. Во-первых, патология пародонтита — не одно, а группа различных заболеваний. Во-вторых, эти заболевания имеют периоды активности и «затишья», и активность заболевания варьирует в пределах организма. И, наконец, трудность в идентификации специфических возбудителей пародонтита связана с колебаниями индивидуальной реакции организма хозяина.
Несмотря на эти трудности, нынешние исследователи по-прежнему согласны с тем, что заболевания пародонта являются инфекциями, вызванными специфическими патогенными микроорганизмами. Недавно было обращено внимание на Bacteroides forsythus, а также на P. gingivalis и A. actinomycetemcomitans как на первичных важнейших возбудителей большинства инфекций пародонта, явно связанных с другой подгруппой микроорганизмов (C. rectus, E. nodatum, F. nucleatum, P. intermedia/nigrescens, P. micros, S. intermedium и T. denticola) как с возможными болезнетворными микробами. Исследователи заняты разработкой и совершенствованием диагностических тестов для обнаружения возбудителя пародонтита и его лечения.
Были предложены антибиотики общего действия, такие как амоксициллин, метронидазол, тетрациклин, доксициклин и аугментин.Было также представлено местное применение антимикробных средств: тетрациклиновых волокон, гелей метронидазола и миноциклина, тонких пластинок хлоргексидина и полимера доксициклина. Хотя эти подходы увеличили наши возможности справиться с заболеваниями пародонта, они все же не смогли обеспечить стабильный успех. Рассмотрение бляшки как биопленки обещает помочь в попытках эффективно лечить пародонтит.
Бляшка как биопленка
Раньше изучались бактерии, выращенные в колониях на чашках Петри в лабораториях. Более усложненная микроскопия, такая как однофокусный сканирующий лазер, позволила исследовать биопленки в их естественных состояниях. Микроорганизмы в биопленке ведут себя не так, как бактерии в культурной среде.
Основные свойства биопленки:
Наблюдаемые в микроскоп бактерии в биопленке распределены неравномерно. Они сгруппированы в микроколонии, окруженные обволакивающим межмикробным матриксом (рис. 5).
Матрикс пронизан каналами, по которым циркулируют питательные вещества, продукты жизнедеятельности, ферменты, метаболиты и кислород. Эти микроколонии имеют свои микросреды, отличающиеся уровнями рН, усваиваемостью питательных веществ, концентрациями кислорода (рис. 6).
Бактерии в биопленке общаются между собой посредством химических раздражений (сигналов) (рис. 7). Эти химические раздражители вызывают выработку бактериями потенциально вредных белков и ферментов.
Наши предшествующие попытки предвидеть и контролировать заболевания пародонта были основаны на свойствах бактерий, выращенных в лабораторных условиях. С пониманием сути биопленки было показано, что существуют большие различия в поведении бактерий в лабораторной культуре и в их естественных экосистемах. К примеру, бактерия в биопленке вырабатывает такие вещества, которые она не продуцирует, будучи в культуре. Кроме того, матрикс, окружающий микроколонии, служит защитным барьером. Это помогает понять, почему антимикробные средства как общего действия, так и применяемые местно, не всегда дают успешные результаты, даже тогда, когда они нацелены на конкретный вид микроорганизмов. Это также помогает объяснить, почему механическое удаление бляшек и личная гигиена ротовой полости продолжают оставаться неотъемлемой составной частью лечения заболеваний пародонта. Биопленки могут быть удалены механическими средствами, однако они немедленно начинают восстанавливаться, поэтому поиск путей борьбы с биопленками продолжается.
Новые рубежи
Промышленные исследователи внедряют новые технологии борьбы с биопленками. Один из подходов предполагает вмешательство в обмен сигналами между бактериями таким образом, чтобы они не могли общаться между собой. Другой путь — подражание природной защите, выработанной обитателям океана, например, китами и дельфинами, не накапливающими бактериальные биопленки. Исследователи-стоматологи также продолжают следовать по пути новых стратегий для препятствия развития биопленок в ротовой полости.
Возможные стратегические направления для предотвращения развития биопленок в ротовой полости
Регулирование рН биопленки
Регулирование окислительно-восстановительного потенциала
Изменение концентрации кислорода, рН, усваиваемости питательных веществ в бляшке показало возможность моделирования микрофлоры биопленки и может оказаться полезным. Например, пародонтальным патогенным микроорганизмам для роста необходим низкий окислительно-восстановительный потенциал. Показано, что добавление окислителя, такого как метиленовый синий, в пародонтальные карманы подавляет рост P. gingivalis.
Поскольку увеличение циркуляции в зубодесневом желобке улучшает обеспечение питанием поддесневой биопленки, регулирование этой циркуляции может в будущем использоваться для контроля за поддесневой биопленкой. Использование противовоспалительных средств может не только помочь подавить разрушительные тенденции в организме хозяина, но и уменьшить поступление питательных веществ в биопленку в процессе циркуляции в зубодесневом желобке.