Что такое бдс при обследовании желудка
ФГС (фиброгастроскопия)
ФГДС – что это за процедура, подготовка, показания и противопоказания, осложнения после
ФГДС – что это за диагностическая процедура, подготовка к исследованию с важными врачебными рекомендациями, показания и противопоказания, возможные осложнения, последствия — опишем все это на сайте alter-zdrav.ru. Часто необходима такая подробная информация тем пациентам, которым впервые назначена фиброгастроскопия желудка и прилегающих органов.
В современной медицине применяются различные методы диагностики, позволяющие быстро и точно поставить диагноз. К ним относятся методы лучевой диагностики (флюорография, рентген, ангиография, компьютерная, магнитно-резонансная и ядерно-магнитная томография), методы прямой визуальной диагностики (фиброгастродуоденоскопия, эзофагогастродуоденоскопия, дуоденальное зондирование, копроскопия и др.).
Довольно часто любое визуальное обследование желудка, основанное на введении зонда через ротовую полость, называют гастроскопией – ФГС (фиброгастроскопия).
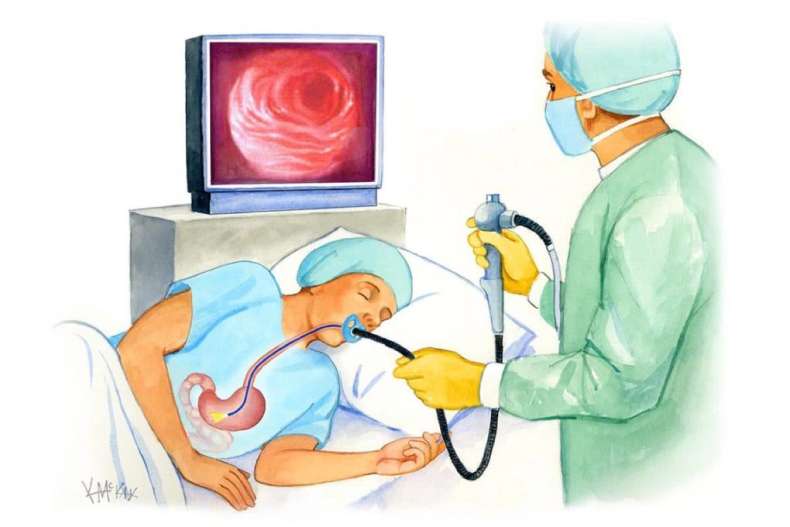
При гастроскопии исследуют слизистую желудка с помощью гибкой трубки (эндоскопа), вводимой в полость желудка через ротовую полость, и камеры на ее конце.
Другой вид визуального обследования – ЭФГДС (эзофагогастродуоденоскопия)предусматривает осмотр желудка, пищевода, 12-перстной кишки эндоскопом.
Методы визуального осмотра позволяют увидеть состояние глотки, пищевода, желудка, 12-перстной кишки, тонкого и толстого кишечника, желчного пузыря, взять желудочный сок, желчь, кусочки ткани на анализ, доставить лекарство точечно.
Один из методов визуального осмотра — метод ФГДС.
Что такое ФГДС
ФГДС (фиброгастродуоденоскопия) – метод обследования с помощью эндоскопа поверхностей пищевода, желудка и начала 12-перстной кишки. В гастроэнтерологии считается самым информативным методом для постановки и уточнения диагноза.
Обследование проводится тонким гибким зондом толщиной 8-11 мм, который вводится через рот и пищевод в желудок. Изображение проецируется на экран. Существует вид обследования, когда зонд вводится через нос.
Преимущества метода ФГДС:
Конструкция аппарата позволяет провести диагностику, взять образцы ткани на анализ, провести хирургические манипуляции в момент проведения процедуры.
Подготовка к ФГДС желудка — несколько важных рекомендаций
Процедура ФГДС требует определенной подготовки и пациенту желательно заблаговременно ознакомиться с требованиями, которые необходимо выполнить, чтобы процедура прошла успешно и с наибольшей информативностью.
Так как же правильно подготовиться к ФГДС, можно ли пить воду, что есть?
Требования к подготовке:
Правильная подготовка пациента, правильный настрой помогут пройти исследование без каких-либо сложностей.
Что взять с собой на исследование желудка
Показания к гастроскопии (ФГДС)
Не всегда анализы, рентгеновское исследование дают возможность поставить диагноз, а проведение ФГДС позволяет увидеть картину заболевания изнутри, уточнить или поставить окончательный диагноз. В основном обследование проводится для диагностики заболеваний желудочно-кишечного тракта, особенно его верхней части.
Когда проводится ФГДС:
ФГДС выявляет такие заболевания: гастрит, язва желудка и 12-перстной кишки, рак желудка и пищевода, воспалительные процессы в пищеводе, рефлюксную болезнь, полипы, дуоденит и другие заболевания.
Своевременно проведенное ФГДС желудка поможет диагностировать заболевание на ранней стадии, что дает возможность начать лечение вовремя.
При хронических заболеваниях ФГДС проводится один раз в год, в остальных случаях – по показаниям и направлению лечащего врача.
Противопоказания ФГДС
Хотя процедура ФГДС является информативной и без нее иногда сложно поставить диагноз, не всегда ее можно проводить. Существуют состояния, когда проводить исследование противопоказано:
Описание процедуры, что показывает ФГДС
ФГДС проводится в специальных диагностических кабинетах планово или экстренно, строго натощак.
До процедуры пациента знакомят с техникой проведения обследования, берется письменное разрешение на ее проведение.
Процедура ФГДС
Медсестра или врач орошает глотку спреем лидокаина, если на него нет аллергии (обязательно заранее выясняется данный вопрос).
Пациента укладывают на кушетку на левый бок. Поза должна быть удобной и комфортной для пациента, в противном случае он будет напряжен, а это мешает введению зонда.
В рот вставляется загубник для удобства введения эндоскопа (иногда прибор для ФГС называют гастроскопом) и чтобы не травмировать слизистую губ и рта.
Врач начинает вводить эндоскоп, пациент по команде врача выполняет глотательное движение. В момент введения может появиться рвотный рефлекс, но, если глубоко и спокойно дышать, это состояние проходит. После введения эндоскопа глотать нельзя, слюна собирается отсосом.
Когда зонд введен, в желудок подается воздух (для расправления складок), чтобы можно было лучше рассмотреть слизистую.
Длительность процедуры 5-10 минут и, при выполнении требований врача, не доставляет большого дискомфорта пациенту.
Если проводятся какие-то лечебные мероприятия, то время ее проведения доходит до 30 минут.
В некоторых случаях исследование проводится под общим наркозом (дети, возбужденное состояние пациента, полная непереносимость боли).
При ФГДС можно увидеть:
После процедуры врачом-эндоскопистом выдается заключение ФГДС — результат проведенного обследования, описание последовательно увиденной картины слизистых пищевода, желудка, привратника, луковицы ДПК (двенадцатиперстной кишки). Указывается наличие свободной проходимости, перистальтики, количества желудочного секрета/заброса желчи, варикозных вен, налета, сомкнутости/недостаточности кардиальной розетки, воспаления (гиперемия, отечность), складок, повреждений.
Довольно часто берется биопсия — микроскопический кусочек слизистой на наличие злокачественных клеток.
Осложнения после ФГДС
Правильно проведенная процедура ФГДС и выполнение пациентом рекомендаций врача осложнений практически не дает. Самое серьезное осложнение – нарушение слизистой пищевода или желудка, занос инфекции.
Чтобы избежать нежелательных реакций организма, каких-то осложнений, врач всегда спрашивает о наличии заболеваний, а пациенту обязательно нужно рассказать о своих индивидуальных особенностях, о своем состоянии перед обследованием (если ему что-то не нравится в своих ощущениях).
Осложнения после ФГДС:
При наличии любого нежелательного симптома обязательно следует проконсультироваться у врача.
После ФГДС – когда можно есть, ощущения
После ФГДС иногда наблюдается легкая тошнота, может быть сухость и першение в горле, но эти симптомы, обычно, быстро проходят.
Через 30 минут, если все хорошо, можно пить воду в небольших количествах, слабый чай (напитки с газом, спиртосодержащие напитки пить нельзя), а через час – принимать пищу. Пища должна быть легкой, не острой, чтобы лишний раз не травмировать слизистую желудка.
Если бралась биопсия, то легкой диеты рекомендуется придерживаться пару дней, нет горячей и раздражающей пище.
Эндоскопическая диагностика и лечение опухолей большого дуоденального сосочка
А. С. Балалыкин, Оноприев А. В., Муцуров Х. С., Катрич А. Н., Вербовский А. Н.
Москва, Краснодар
Актуальность
В настоящее время число воспалительных и опухолевых заболеваний поджелудочной железы, желчного протока и большого дуоденального сосочка (БДС), вызывающих непроходимость внепеченочных желчных протоков, продолжает увеличиваться и удельный вес рака БДС среди опухолей билиопанкреатодуоденальной зоны составляет 10,1–18,3 % (Русаков В. И. с соавт., 1986; Frosali D. et al., 1990).
Чрезвычайная злокачественность рака панкреато-биллиарной области и его поздняя диагностика приводят к тому, что хирургическое лечение больных сопровождается высоким операционным риском и невозможностью выполнения радикальных операций. Их частота составляет только 4–27 %, послеоперационная летальность достигает 8–22 %, а пятилетняя выживаемость — всего 4–6 % [М. В. Данилов соавт., 1995; А. А. Мовчун с соавт., 1994; В. А. Кубышкин с соавт., 2003].
Благодаря ранним клиническим проявлениям (механическая желтуха) опухоли БДС диагностируются на более ранней стадии, чем опухоли другой локализации. Существующие инструментальные методы исследования (эндоскопические, лучевые, лапароскопические) далеко не всегда позволяют сформулировать наиболее рациональную тактику и вид лечения, и главное, имеют существенные ограничения в оценке стадии болезни.
К 80-м годам прошлого столетия был разработан принципиально новый диагностический прибор — эхо-эндоскоп, соединивший в себе возможности гибковолоконной эндоскопии и ультразвукового исследования.
Отличительной особенностью и неоспоримым преимуществом метода перед другими является то, что ультразвуковой датчик под контролем зрения размещается в непосредственной близости от зоны исследования, что позволяет повысить разрешающую способность ультразвукового сканирования. Учитывая короткую дистанцию исследования, и доказанную корреляцию между получаемым ультразвуковым изображением и анатомическим строением стенки полых органов желудочно-кишечного тракта (ЖКТ), эндо-УЗИ позволяет произвести послойную структурную оценку БДС, окружающих его органов и тканей, сосудистых и протоковых образований в зоне исследования. Полученные данные позволяют установить диагноз и обосновать план лечения.
Материалы и методы исследования. Нами проанализированы результаты лечения 39 пациентов с подозрением на злокачественные новообразования диагностированные при обследовании 421 больных в 2004–2009 гг. в возрасте 35–77 лет.
Нами применен следующий инструментальный диагностический алгоритм: ТАУЗИ, фиброгастродуоденоскопия (ФГДС), эндо-УЗИ, эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ), фистулография, компьютерная томография (КТ) — по показаниям.
Несомненным преимуществом ТАУЗИ перед другими методами исследования является отсутствие противопоказаний и возможность использовать его в качестве экспресс-диагностического метода.
Перед ФГДС ставились следующие задачи: оценить проходимость верхнего отдела ЖКТ, выявить специфические изменения слизистой желудка и ДПК, характерные для сопутствующих заболеваний желудка и ДПК, определить доступность и состояние БДС и периампулярной области, оценить технические возможности проведения лечебных эндоскопических мероприятий на БДС.
Эндоскопическое ультразвуковое исследование.
Мы использовали видеоэндоскопический комплекс, EVIS EUS EXERA, «Olympus», Япония, включающий: видеоэндоскопический центр CV-160, осветитель CLV-160, ультразвуковой эндоскопический центр UM-60, радиальный ультразвуковой гастровидеоскоп GF-UM 160.
Подготовка больных к эндо-УЗИ панкреатобилиарной системы не отличается от таковой при обычной эндоскопии.
Проведению эндо-УЗИ обязательно должно предшествовать эндоскопическое или рентгенологическое исследование пищевода или желудка (для исключения стенозов, дивертикулов), поскольку введение эхоэндоскопа производится практически без визуального контроля.
Стандартные позиции проведения эндоскопического ультразвукового исследования различных органов были предложены M. Sivak (1982 г), и W. Strohm и M. Classen (1982) и утверждены Международной конференцией по эндоскопической эхографии (Стокгольм). В последствии методика была дополнена K. Inui et al. (2004).
Большой дуоденальный сосочек — осмотренный в поперечном сечении, представляется как дополнительное округлое (овальное) многослойное образование стенки нисходящего отдела ДПК. При идентификации структур БДС определяются поочередно мышечный слой ДПК (слой сниженной эхогенности), подслизистый слой ДПК (слой повышенной эхогенности), мышечный аппарат сфинктера (тонкий гипоэхогенный слой) и внутренний гиперэхогенный слой, соответствующий слизистому и подслизистому слою ампулы сосочка.
Для исследования БДС в продольном направлении необходимо смещение УЗ-датчика в проксимальном направлении, путем подтягивая эндоскопа. Основными ориентирами являются протоковые структуры; в этом случае ультразвуковая картина меняется индивидуально: соответственно анатомическим взаимоотношениям терминальных отделов желчного и панкреатического протоков, относительно друг друга и стенки ДПК.
Увеличение БДС в размерах более 1 см, выявление в просвете сосочка дополнительных образований, исходящих из его стенок, изменение эхографических характеристик многослойной структуры данного анатомического образования интерпретируется как патологическое изменение БДС.
Ультразвуковая семиотика заболеваний БДС. Эндоскопическими ультразвуковыми диагностическими критериями опухоли БДС являются: нарушение нормальной многослойной эхоструктуры БДС, солидное образование в проекции БДС, сниженная или смешанная эхо-генность образования, нечеткие контуры образования.
Опухоль может иметь экзофитную (в просвет ДПК) и эндофитную или инвертированную (в просвет дистальных отделов протоков) формы роста. На начальных стадиях роста и небольших размерах образования и при отсутствии инфильтративного роста надежных дифференциально-диагностических критериев карциномы и аденомы, не существует.
Эндоскопическими ультразвуковыми диагностическими критериями карциномы сосочка являются: распространение гипоэхогенных тканевых масс на мышечный слой стенки ДПК, в просвет холедоха и ГПП или на стенки протоков, в паренхиму поджелудочной железы, и/или обнаружение рядом с БДС лимфатических узлов подозрительных на их метастатическое поражение (Панцырев Ю. М. и соавт. 2002). Это- важные дифференциально-диагностические признаки, т. к. обнаружение хотя бы одного из них определяет тактику лечения и ставит под сомнение радикальность эндоскопической резекции опухоли. Недооценка указанных фактов приводит к неудовлетворительным результатам эндоскопических методов лечения.
Наиболее важными лимфатическими коллекторами, требующими детальной оценки для точного определения лимфогенного метастазирования опухоли БДС в процессе выполнения эндосонографии, являются лимфоузлы печеночно-двенадцатиперстной связки, задние поджелудочно-двенадцатиперстные лимфоузлы и верхнебрыжеечные лимфоузлы.
Так как опухоли БДС, которые инфильтрировали поджелудочную железу или периампулярную область, невозможно отличить от первичных панкреатических карцином, большинство авторов описывают их как «опухоли БДС» или «периампулярные раки». Так как оба типа в одинаковой степени склонны к метастазированию, нет необходимости в их дооперационной дифференцировке их локализации. Дооперационное определение стадии ампулярной карциномы базируется на основании Международной классификации по факторам TNM принятой европейской организацией «Union International Control Cancer».
Результаты
После комплексного применения диагностических методик у 36 из 421 обследованных пациента был установлен предварительный диагноз опухоли БДС, причем у 34 пациентов была заподозрена злокачественная природа процесса в стадии Т1 — у 7 (20,6 %), Т2 — у 16 (47 %), в стадии Т3 — у 11 (32,4 %) пациентов.
Нами была проанализирована диагностическая ценность инструментальных методов в диагностике опухолей БДС и установлено, что эндо-УЗИ имеет более высокую чувствительность, специфичность и диагностическую эффективность.
Показания к эндоскопическим методам лечения были выставлены у 7 пациентов. После применения комплекса диагностических методик, по макроскопической картине выявленные неоплазии были разделены на экзофитную и эндофитную (инвертированную) форму опухоли БДС. Размеры выявленных образований колебались в пределах от 8 до 32 мм. Морфологическая характеристика опухолей распределилась следующим образом: высокодифференцированная аденокарцинома, аденома с дисплазией III ст., аденома с дисплазией II ст.
Возможность выполнения эндоскопической эксцизии опухолей БДС (Балалыкин А. С. и соавт. 2008, Катрич А. Н. и соавт., 2008) обосновывалась данными эндо-УЗИ (тип роста образования, наличие измененных лимфатических узлов, состояние мышечного слоя стенки ДПК, терминальных отделов желчного и панкреатического протока). Всем пациентам был применен последовательный комплекс эндохирургических вмешательств, включавший атипичную «послойную» ЭПТ с помощью торцевого папиллотома, дополненная канюляционной ЭПТ у 6 больных, петельную электроэксцизию опухоли, электро — или аргоноплазменную деструкцию, а также вмешательства, направленные на обеспечение адекватного пассажа желчи и панкреатического сока (стент, НБД). Всем пациентам в послеоперационном периоде выполнялось желудочное и дуоденальное зондирование, проводился курс консервативной терапии. Контрольные обследования выполнялись в сроках от 3 до 6 месяцев.
Успех и безопасность эндоскопического вмешательства определяется правильным набрасыванием петли и рациональным сочетанием режимов резания и коагуляции, поэтому в зависимости от формы роста опухоли менялись технические аспекты выполнения данного этапа операции. В случае эндофитной формы роста опухоли после выполнения атипичной «послойной» ЭПТ, с помощью торцевого папиллотома выполнялись «полулунные» окаймляющие разрезы слизистой оболочки в пределах здоровых тканей, в 3 случаях дополненные введением с помощью инъектора, раствора в подслизистый слой, для создания «подушки» под тканью опухоли. С нашей точки зрения эти приемы обеспечивают:
1) адекватное набрасывание эндоскопической петли на опухоль;
2) снижают риск «сползания» петли;
3)резекцию «in block». С целью профилактики кровотечения и повышения абластичности операции выполнялась электро или аргоноплазменная деструкция зоны новообразования БДС. Обеспечение свободного пассажа желчи и панкреатического сока достигалось за счет выполнения билиопанкреатического стентирования.
Осложнениями оперативных вмешательств являлись: интраоперационное кровотечение, остановленное эндоскопически, микроперфорация ДПК, которая была излечена консервативно.
В одном случае, через 3 месяца после выполнения операции, при контрольном эндо-УЗИ, был выявлен продолжающийся рост опухоли. Пациенту была выполнена панкреатодуоденальная резекция.
Выводы
1. Методика эндоскопического ультразвукового исследования является наиболее эффективным методом диагностики заболеваний БДС, стадии злокачественного процесса и позволяет планировать объем и вид лечения больных. 2. Успех, радикальность и безопасность эндоскопической папиллэктомии определяется комплексностью эндоскопических методик и четким соблюдением этапности их выполнения. Включение в лечебный алгоритм стентирования протоков обеспечивает свободный пассаж желчи и панкреатического сока, и позволяет избежать послеоперационных осложнений.
Что такое бдс при обследовании желудка
Чтобы поставить точный диагноз при заболевании ЖКТ, когда клиническое обследование, анализы, УЗИ и рентгенография не дают полной картины, применяется гастроскопия (или эндоскопия) желудка.
У пациентов, которым впервые назначено данное обследование, может возникнуть вопрос: «Что это за процедура-эндоскопия желудка?»
Полный текст статьи:
Эзофагогастроскопия (от латино-греческого, где oesophagus-пищевод gaster-желудок, duodenum 12-перстная кишка, skopeo-смотреть) – вид эндоскопического узкоспециализированного исследования верхнего отдела желудочно-кишечного тракта (пищевод, желудок, 12п.кишка) с помощью гибкого эндоскопа. Эндоскопия проводится в диагностических и лечебных целях. Уникальные оптические возможности прибора позволяют не только рассмотреть все участки слизистой больного органа, рассмотреть ямочный и сосудистый рисунок, а также сделать его фото и видео.
Данная процедура позволяет за один прием осуществить изучить состояние органов верхнего отдела желудочно-кишечного тракта, а при необходимости даёт возможность провести дополнительные диагностические (проведение теста на «хеликобактер пилори», хромоскопию, определение кислотности, манометрию) и лечебные манипуляции (остановить кровотечение, выполнить забор кусочка ткани для гистологического изучения и удалить новообразования).
Как выполняется гастроскопия (эзофагогастродуоденоскопия)?
Чтобы провести обследование с наибольшей информативностью, важно знать, как подготовиться к процедуре эндоскопии желудка:
Как проходит процедура эндоскопии?
Во время эзофагогастродуоденоскопии тонкую гибкую трубку эндоскопа с оптической системой ( видеокамерой) на конце поэтапно ведут от устья пищевода до начальных отделов тонкой кишки. Эндоскопы, оснащенные волоконно – оптической системой и объективом, транслируют изображение на монитор онлайн, что позволяет доктору сразу диагностировать состояние обследуемого. Затем аккуратно извлекают аппарат.
Капсульная гастроскопия отличается тем, что вместо зонда пациент глотает пластиковую капсулу, в которой находится видеокамера (через 8 – 15 часов она выводится из организма естественным путем при акте дефекации).
Длительность процедуры определяется индивидуально. При местной анестезии время проведения манипуляций занимает 7-10 мин. При общем наркозе обследование длится около 30 мин.
ВАЖНО! После эндоскопии пищевода и желудка не рекомендуется 30 минут пить и принимать пищу. После наркоза\седации в этот день воздержаться от управления автомобилем.
Как готовиться к гастроскопии?
Перед тем как пройти гастроскопию, необходимо выполнить некоторые рекомендации. Желательно, прежде всего, пройти консультацию у специалиста (врача – гастроэнтэролога):
За два-три дня до манипуляции не следует принимать острую пищу, копчености и жареные блюда. А вот нежирное мясо, приготовленное на пару, легкие супы на овощных отварах и каши, наоборот приветствуются. Хлеб должен быть слегка подсушен.
В день проведения гастроскопии, если процедура назначена на первую часть дня, принимать пищу нельзя. А если на вторую половину дня, то можно позволить себе легкий завтрак (оптимально для этого хорошо проваренная каша или творог), но не позже, чем за 8-10 часов до исследования.
Особое внимание нужно уделить питьевому режиму! До обследования пить запрещено. А во время подготовки исключаются алкоголь, газировку и кофе.
Что ожидать во время гастроскопии?
Благодаря анестезии человек не кашляет и не испытывает позывов к рвоте. Дыхание не затруднено и приступы удушья исключены, так как эндоскоп не перекрывает дыхательные пути.
Главное, морально настроиться, тогда спокойное состояние не приведет к спазму мышц желудочно-кишечного тракта, и исследование будет легче как для пациента, так и для врача.
Что ожидать после гастроскопии?
Если гастроскопию проводят грамотно, то, как показали годы практики, после процедуры пациент не испытывает неприятных ощущений. Единственно, может ощущаться некоторый дискомфорт в горле и легкое першение. Но и эти симптомы исчезают в течение суток.
Каковы возможные осложнения гастроскопии?
Если Вам гастроскопию назначал Врач, то он проанализировал состояние Вашего здоровья и считает, что с Вашим состоянием здоровья риски осложнений минимальны (т.е. исключены инфаркт, инсульт, и прочее серьезные «общие» негативные проявления, которые могут быть спровоцированы за счет исследования)
Непосредственно у самой процедуры осложнения крайне редки, к возможным осложнениям при проведении эндоскопии желудка и двенадцатиперстной кишки можно отнести прободение (перфорацию) стенок органов и вызванные травмой кровотечения. Но такие побочные явления случаются крайне редко и если Вы правильно подоготовились, не срыгиваете, выполняете все требования и команды врача-эндоскописта, то риски минимальны.
Как правило, гастроскопию назначают при осмотре Врача-специалиста, если есть жалобы на ЖКТ т.е. «по требованию». некоторые вынуждены проходить «профилактическую гастроскопию» 2 раза в год в периоды обострения заболеваний и в рамках «диспансеризации» если этот пункт отмечен для Вашего возраста. Но если обнаружены патологии, то гастроэнтеролог или лечащий врач назначает данное обследование индивидуально, в зависимости от степени тяжести заболевания.
Если Вы заботитесь о сохранении своего здоровья, то рекомендуем проходить гастроскопию и колоноскопию раз в 4-5 лет, при отсутствии патологии. Спросите у Вашего эндоскописта, какой интервал рекомендует он именно Вам!
Опухоль большого дуоденального сосочка как причина рецидивирующего холедохолитиаза.
М.А. Евсеев, А.Л. Владыкин, Ю.А. Бирюкова, В.Е. Никитин. Представлено клиническое наблюдение рецидивного холедохолитиаза, связанного с развитием опухоли большого дуоденального сосочка на фоне суб- декомпенсированного рубцового стеноза пилоробульбарного сегмента; описаны этапы инструментальной диагностики и интраоперационная тактика в процессе лечения. Хирургическая практика. 2015, №1.
Рецидивный и резидуальный холедохолитиаз как много десятилетий назад, так и сегодня является по-прежнему трудным для диагностики и лечения осложнением желчнокаменной болезни (ЖКБ). По сводным данным литературы частота резидуальных и вновь сформированных камней желчных протоков с течением времени не уменьшается и может достигать 29%. Причины возникновения рецидивного и резидуального холедохолитиаза разнообразны. Тем не менее ведущим этиопатогенетическим фактором данной патологии по всеобщему мнению является недостаточный объем до- и интраоперационного обследований желчных путей и, как следствие, не диагностированные в предоперационном периоде и на операции холедохолитиаз, патология терминального отдела холедоха, большого дуоденального сосочка и головки поджелудочной железы. Последние три причины определяют возникновение, как правило, не резидуальных, а рецидивных конкрементов в желчевыводящих протоках. В качестве примера рецидивного холедохолитиаза, обусловленного развитием злокачественной опухоли большого дуоденального сосочка, приводим следующее клиническое наблюдение.
Из анамнеза известно, что в 2013 году пациентка находилась на лечении в ГКБ № 5х города Москвы по поводу хронического калькулезного холецистита, холедохолитиаза, субкомпенсированного рубцово-язвенного стеноза пилоро-бульбарной зоны. В период госпитализации после безуспешных попыток выполнения ретроградной холангиопанкреатографии (РХПГ), эндоскопической папиллосфинктеротомии (ЭПСТ) и литоэкстракции пациентка была оперирована. Произведены срединная лапаротомия, холецистэктомия, холедохолитотомия, дренирование холедоха по Керу, пилоропластика по Гейнеке — Микуличу. Послеоперационный период протекал гладко, пациентка была выписана в обычные сроки, дренаж Кера удален через три недели.
Повторное возникновение желтухи с эпизодами гипертермии пациентка отметила в последней декаде декабря 2014 года, по поводу чего в срочном порядке 31. 12. 14 была госпитализирована в ГКБ № 1х города Москвы, где диагноз механической желтухи был верифицирован, но активных хирургических действий не предпринималось.
Пациентка покинула ГКБ № 1х и самостоятельно обратилась в хирургическое отделение ГКБ № 52. На момент госпитализации в ГКБ № 52 06. 01. 15 факт механической желтухи и холангита был подтвержден клинически, данными УЗИ (билиарная гипертензия, холедохолитиаз), лабораторно (прямой билирубин 432 мкмоль/л, общий билирубин 464 мкмоль/л), гектической лихорадкой, лейкоцитозом (до 14, 6 х 109/л) ; кроме того пациентка периодически отмечала возникновение чувства переполнения в эпигастрии при приеме твердой пищи, редко — рвоту съеденной пищей.
Пациентке выполнена фиброэзофагогастроскопия, при которой выявлен суб- декомпенсированный стеноз пилоробульбарного сегмента (аппарат 9 мм через зону стеноза провести не удалось, просвет двенадцатиперстной кишки не визуализирован), органической патологии со стороны пищевода и желудка выявлено не было. При экспертном УЗИ гепатобилиопанкреатической зоны наряду с дилатацией холедоха и множественным холедохолитиазом в области головки поджелудочной железы, но не в ее ткани, нечетко лоцировалось мягкотканное образование 2 х 2 см.
В экстренном порядке 06. 01. 15 пациентке под УЗ-контролем произведена чрезкожная чреспеченочная холангиостомия (ЧЧХС), дренаж 12 Fr через левый долевой проток установлен в гепатикохоледох, получена темная желчь с хлопьями фибрина. Пациентке проводилась комплексная дезинтоксикационная, антибактериальная терапия, дозированная билиарная декомпрессия, сбалансированная энтральная и парентеральная нутритивная поддержка. Через 7 суток на фоне снижения гипербилирубинемии до 62 мколь/л пациентке проведена чрездренажная холангиография, при которой выявлены множественные крупные конкременты общего желчного протока, дислоцированные от супрадуоденального до терминального его отделов, блок поступления контраста в двенадцатиперстную кишку; оценить состояние стенок интрапанкреатического и интрадуоденального отделов холедоха не представлялось возможным. В удовлетворительном состоянии без явлений интоксикации с функционирующим наружным желчным свищом (дебит желчи 600 мл/сут) пациентка была выписана для проведения амбулаторной реабилитации с рекомендацией последующей госпитализации через 14 суток для проведения радикального хирургического лечения.
25. 01. 15 пациентка вновь самостоятельно обратилась в ГКБ № 52 и была госпитализирована в хирургическое отделение. На момент повторной госпитализации состояние пациентки клинически и по данным лабораторных исследований было расценено как удовлетворительное, явления желтухи и холангита клинически регрессировали полностью. Дополнительно в плане обследования больной выполнена рентгеноскопия желудка с контрастом, при которой контраст задерживался в желудке более 6 часов, опрдлялись признаки суб- декомпенсированного стеноза пилоробульбарной зоны, вследствие чего добиться тугого заполнения контрастом просвета двенадцатиперстной кишки и оценить состояние ее слизистой не удалось.
При проведении компьютерной томографии органов брюшной полости и забрюшинного пространства визуализирован умеренно дилатированный холедох с равномерно утолщенными стенками и множественными крупными конкрементами в просвете, расширение вирсунгова протока на всем протяжении до 0, 9 см, мягкотканное образование стенки двенадцатиперстной кишки в области интактной головки поджелудочной железы 2, 5 х 2, 5 см с тенденцией к накоплению контраста в артериальную фазу.
Таким образом на основании комплексного обследования у пациентки диагностированы рецидивный холедохолитиаз, суб-декомпенсированный рубцовый стеноз пилоро-бульбарного сегмента, состояние после наружного дренирования желчных протоков, полный наружный желчный свищ, опухоль большого дуоденального сосочка (?). Учитывая установленный клинический диагноз, включающий как рецидивный холедохолитиаз, так и стеноз пилоробульбарного сегмента при невозможности консервативного разрешения данных патологических состояний, а также невозможность неинвазивной оценки состояния терминального отдела холедоха и исключения опухолевого процесса в данной зоне, принято решение о необходимости проведения оперативного вмешательства. Предполагаемый объем вмешательства: дистальная резекция 2/3 желудка по Ру с холедохолитотомией и билиодигестивным анастомозом — минимальный, гастропанкреатодуоденальная резекция (ГПДР) — максимальный.
После подписания информированного согласия пациентка была оперирована в плановом порядке. При выполнении верхне-срединной лапаротомии, проведения адгезиолизиса, ревизии органов брюшной полости и выполнении диагностической дуоденотомии установлен следующий интраоперационный диагноз: Рак большого дуоденального сосочка oT3N1M0 (IIB стадия), регионарная лимфаденопатия ретропанкреатических узлов; рецидивный холедохолитиаз, состояние после холецистэктомии, дренирования холедоха от 2013 года, состояние после ЧЧХС от 06. 01. 15; суб- декомпенсированный рубцовый стеноз пилоро-бульбарного сегмента, состояние после пилоропластики по Гейнеке-Микуличу от 2013г.
Учитывая интраоперационный диагноз принято решение о выполнении вмешательства в объеме ГПДР. Произведена гастропанкреатодуоденальная резекция с регионарной лимфаденэктомией. Реконструкция производилась с формированием панкреатико-гастроанастомоза, гепатико-энтероанастомоза на выключенной по Ру петле и поперечного функционального полуклапанного гастро-энтероанастомоза.
Ведение пациентки в послеоперационном периоде проводилось по программе ERAS (Enhansed Rehabilitation After Surgery) с ранним (на 2-е сутки) началом энтерального питания и активизацией больной. Ранний послеоперационный период у пациентки протекал гладко. На 7-е сутки послеоперационного периода пациентка после проведения контрастного исследования пищеварительного тракта и удаления холангиостомического дренажа выписана на амбулаторную послеоперационную реабилитацию с полным восстановлением пищеварительной функции. Рекомендовано проведение адъювантной полихимиотерапии под наблюдением врача-онколога, а также опроеделение возможности проведения таргетной биотерапии после иммуногистохимического анализа на р53 и KRAS.
Таким образом, причиной возникновения рецидивного холедохолитиаза у пациентки Р. послужило длительное и прогрессирующее нарушение пассажа желчи в терминальном отделе холедоха вследствие развития опухоли большого дуоденального сосочка. Интересность данного клинического наблюдения, на наш взгляд, обусловлена редким сочетанием трех патологических процессов — опухоли большого дуоденального сосочка, рецидивирующим холедохолитиазом и рубцовым стенозом пилоро-бульбарного сегмента. Последний сделал очевидно невозможной дооперационную верификацию опухолевого процесса и определения первопричины рецидива патологии билиарного тракта.
Проведенное в объеме гастропанкреатодуоденальной резекции оперативное вмешательство явилось радикальным методом лечения как с точки зрения имеющегося онкологического процесса, так и с точки зрения обеспечения максимально адекватного функционирования желудка, билиарного тракта и поджелудочной железы (рис. 7). Последний момент особенно интересен, поскольку формирование именно панкреатико-гастроанастомоза имеет целый ряд позитивных особенностей, среди которых наиболее важными являются: возможность сохранения большей части желудка (выполняется антрумрезекция) без опасности развития его острого эрозивно-язвенного поражения вследствие защитного ощелачивающего действия бикарбонатов панкреатического сока; отсутствие активации панкреатических ферментов в кислой среде желудка при отсутствии энтерокиназы; пространственное разделение билио- и панкреатикодигестивного анастомозов, что принципиально уменьшает риск несостоятельности последнего. Мы полагаем, что именно такой вариант реконструкции позволяет добиться максимально быстрой и эффективной реабилитации пациента в послеоперационном период, в том числе после вмешательств большого объема, что и продемонстрировало приведенное клиническое наблюдение.
Касаткин В. Ф. Пути улучшения непосредственных результатов панкреатодуоденальной резекции при периампулярном раке. Хирургия. 2008; 10; 10–15.
Bang BW, Lee TH, … Jeong S. Twenty-Second versus Sixty-Second Dilation Duration in Endoscopic Papillary Balloon Dilation for the Treatment of Small Common Bile Duct Stones: A Prospective Randomized Controlled Multicenter Trial. Clin Endosc 2015; 48 (1): 59-65
Parra-Membrives P, Díaz-Gómez D, Vilegas-Portero R, et al. Appropriate management of common bile duct stones: a RAND Corporation/UCLA Appropriateness Method statistical analysis. Surg Endosc 2010 May; 24 (5): 1187-94.
Статья добавлена 13 января 2016 г.