Что можно после анестезии
Питание в послеоперационный период
Изменения в метаболизме после операций или травмы являются фактором риска послеоперационных осложнений.
Показатели обмена веществ у пациента влияют на скорость, с какой он восстановится после операции или травмы. Если ответ организма на вмешательство мощный, то человек истощается, слабеет иммунитет, может легко присоединиться инфекция. Это осложняет процесс восстановления. Почему так происходит?
Как организм реагирует на операцию или травму
При операции и травме в кровь пациента поступают гормоны стресса и цитокины. Цитокины – вещества, которые регулируют воспалительные процессы в организме. Воспаление – реакция организма на различные повреждения. Эта реакция активизирует защитные силы организма – потому что через любую рану может попасть инфекция. Выброс в кровь цитокинов и гормонов стресса изменяет обмен веществ. Что это за изменения? Запускается процесс расщепления гликогена – тратится энергетический запас организма. В качестве дополнительных источников энергии перерабатываются жиры из жировой ткани и белки из мышц. Расход белка на энергетические потребности не позволяет использовать его на первоочередные нужды: создание новых клеток и тканей, т.е. заживление раны. Это мешает восстановлению пациента после хирургического вмешательства:
Чтобы улучшить прогноз для больного, нужно снабжать его организм дополнительными питательными веществами, которые дают легкоусвояемую энергию и белок. Профилактика общего истощения положительно влияет на иммунитет, повышая защитные силы всего организма. Даже минимальное питание оказывает лечебное действие на клетки слизистой кишечника, сохраняя барьерную функцию желудочно-кишечного тракта по отношению к микробам.
Одна из составляющих поддержки больного на пути к его выздоровлению – нутритивная терапия. Это питание для пациента, которое направлено на профилактику или лечение истощения. В нутритивную терапию входит питание через рот – обычная или лечебная диета, энтеральное и парентеральное питание.
Какому хирургическому пациенту нужна нутритивная терапия?
— больному без признаков истощения, если ожидается, что он не сможет есть больше 5 дней, или у него будут проблемы с приемом достаточного количества пищи через рот (меньше 60% больше 7 дней)
— больному, у которого возможен риск послеоперационных осложнений, связанных с питанием. Скрининг риска проводится, когда у пациента
Своевременная профилактика недостаточного питания заметно влияет на исход заболевания. Как это выглядит в цифрах – читайте статистику ниже.
Немного статистики исследований «прогностическое влияние состояния питания на осложнения и летальность»
Раннее начало питания после операций может показаться особенно сомнительным в случае хирургических вмешательств на желудочно-кишечном тракте. Но даже здесь – при соблюдении правил проведения нутритивной поддержки – снижается процент осложнений и время, проведенное в больнице. Это показано в Кокрейновском обзоре 2 о влиянии раннего энтерального питания на частоту осложнений после операций на желудочно-кишечном тракте. Кокрейн – это некоммерческая организация, которая анализирует опубликованные медицинские исследования и проверяет их на соответствие принципам доказательной медицины.
Авторы обзора отобрали 14 исследований, включавших 1224 пациента. По этим работам они заключили, что начало нутритивной поддержки в течение 24 часов после операции сокращает пребывание в больнице на 1 день и уменьшает частоту некоторых осложнений:
В качестве нутритивной терапии подходят сбалансированные по питательным веществам, витаминам и микроэлементам специальные смеси.
Продукты Nutrien Stadard и Nutrien Energy для восстановления организма после операции
К таким смесям относятся Nutrien Standard и Nutrien Energy. Это универсальные лечебные продукты, которые подходят для перорального приема и энтерального питания через зонд после операций и травм.
Обе смеси содержат:
молочный белок, который легко усваивается,
полиненасыщенные жирные кислоты (омега-3), которые способствуют противовоспалительному и иммуномодулирующему действию,
жиры, которые не перегружают поджелудочную железу, легко усваиваются и дают быстро и много энергии,
Nutrien Energy отличается большей концентрацией белка и энергии, витаминов и минералов, и лучше подходит для более поздней, длительной реабилитации, когда желудочно-кишечный тракт восстановился после операционного стресса. Какая из этих смесей лучше подойдет? Для точного ответа получите рекомендации от лечащего врача.
Нутритивная терапия статистически улучшает прогноз хирургического пациента, но нюансы поддержки с помощью питания могут отличаться у разных больных. Чтобы получить только пользу от лечебных смесей, важно не только понимать, как организовать свое питание после операции, но и действовать согласованно с лечащим врачом или диетологом.
Что родителям нужно знать о наркозе?
В СМИ иногда рассказывают о том, как ребенок пострадал во время наркоза. После этого родителям страшно приводить ребенка в клинику для операции или другой манипуляции, при которой нужна анестезия. Но на самом деле плановая операция под наркозом безопаснее полета на самолете. Рассказываем чем опасен наркоз на самом деле и как можно снизить риски.
Что это такое
Наркоз или общая анестезия — это искусственный сон. Он отличается от обычного тем, что из-за препаратов мозг не реагирует на болевые сигналы и другие раздражители. Это способ защитить ребенка не только от операционного, но и от психологического стресса. Поэтому часто маленьким детям даже небольшие вмешательства проводят под наркозом.
Главная задача анестезиологического пособия во время операции обеспечить отсутствие боли, сознания и двигательную активность. Для этого анестезиолог вводит препараты:
Препараты и вид анестезии зависит от процедуры. Если нужно, чтобы ребенок спокойно перенес МРТ и не двигался, то чаще всего используются только анестетики для кратковременного сна. В этом случае не понадобятся релаксанты и обезболивающие.
Для некоторых поверхностных вмешательств достаточно газовых анестетиков. Они расслабляют и обезболивают. В таком случае можно обойтись без введения дополнительных препаратов.
Во время любой процедуры под наркозом, анестезиолог следит за состоянием ребенка с помощью монитора и капнографа. По ним можно видеть частоту сердцебиения и дыхания, измерить давление и уровень выдыхаемого углекислого газа. Это нужно чтобы вовремя заметить изменения в состоянии ребенка и ввести лекарство или поменять параметры на дыхательном аппарате.
Анестезия бывает местная, регионарная и общая.
Местная используется для обезболивания небольшого участка. Она применяется в стоматологии и для небольших хирургических вмешательств. Например, для вскрытия фурункула или лечения панариция. Но у нее есть важное противопоказание — ребенок должен спокойно переносить уколы и медицинские манипуляции. Поэтому без седации местная анестезия редко используется у маленьких детей.
Регионарная анестезия используется для блокирования болевых импульсов от крупного участка тела. Для операций на верхних конечностях используют проводниковую анестезию, когда анестезиолог обезболивает крупное нервное сплетение для снижения чувствительности кисти или всей руки. Часто проводится под контролем УЗИ. У детей используется редко или как часть общей анестезии.
Для операций на нижних конечностях чаще пользуются спинальной или эпидуральной блокадой. Она хороша тем, что выключает поток болевых импульсов от места операции к головному мозгу. Это приводит к меньшему операционному стрессу, более быстрому восстановлению ребенка и меньшему количеству осложнений. Также уменьшает количество наркотических анальгетиков и миорелаксантов, если применяется как часть общей анестезии.
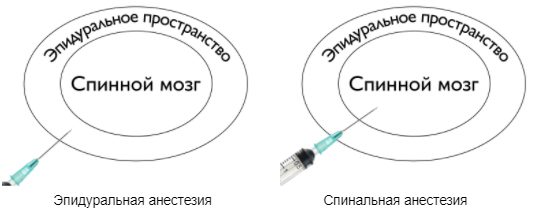
При спинальной анестезии анестетик вводится на уровне конского хвоста, которым заканчивается спинной мозг. Повредить его таким образом сложно. Анестетик вводится однократно и перестает действовать через определенное время, поэтому продолжительность операции при спинальной анестезии ограничена.
При эпидуральной анестезии препарат вводится в пространство вокруг спинного мозга. Это удлиняет начало эффекта от анестезии, но безопасно для пациента. Для этого анестезиолог пользуется пробами, которые помогают понять, когда игла попала в эпидуральное пространство. После этого врач обычно устанавливает катетер для постоянного введения анестетика.
У детей эпидуральная анестезия применяется для длительных и сложных вмешательств, после которых нужно продолжительное обезболивание и наблюдение за состоянием. Такой вид анестезии уменьшает потребность в наркотических анальгетиках. А прерывание болевых импульсов от места операции снижает операционный стресс, помогает быстрее восстановиться и уменьшает скорость заживления тканей.
Перед операцией анестезиолог составляет план наркоза. Он выбирает подходящий вариант, исходя из тяжести операции и особенностей ребенка. Например, маленьким детям сначала подают газ через маску. Когда малыш уснет, тогда уже ставят внутривенный катетер и вводят в него необходимые препараты. И добавляют другие виды анестезии, если есть необходимость. Это менее травматично для детской психики.
В чем опасность
Общая анестезия крайне редко вызывает осложнения. Особенно, если анестезиолог опытный и внимательно относится к подготовке. Но иногда случаются реакции, которые сложно предсказать.
Аллергическая реакция. Ее нельзя предусмотреть заранее, но если ребенок склонен к аллергии, то анестезиолог может ввести лекарства от аллергии перед началом манипуляции, чтобы уменьшить риски. В операционной должны быть необходимые препараты для лечения этого осложнения.
Злокачественная гипертермия. Это крайне редкое наследственное состояние, 1 случай на 3–15 тысяч наркозов. При ней нельзя использовать некоторые миорелаксанты и газовые анестетики. Чтобы уменьшить риск этого осложнения, анестезиолог должен знать, если у ребенка или его родственников была какая-то реакция на предыдущие наркозы.
Нарушения сердечного ритма редко встречаются у детей. Они могут быть связаны с реакцией на препараты для наркоза. Чтобы снизить вероятность, до плановой операции ребенку нужно обязательно записать ЭКГ. Возможно потребуется консультация кардиолога, если на ЭКГ будет что-то не так. Во время операции анестезиолог следит за сердечной деятельностью с помощью монитора, на котором, в том числе, записывается ЭКГ.
Проблемы с дыханием возможны если используются препараты, угнетающие дыхание или у ребенка есть хронические заболевания легочной системы. В таком случае анестезиолог может принять решение о вентиляции легких во время операции, чтобы снизить риски.
Иногда родители опасаются, что наркоз может повлиять на развитие ребенка. Этот миф появился давно, тогда использовались токсичные препараты, которые могли повлиять на нервную систему. Но современные средства не обладают такой токсичностью при редком применении.
По словам Владимира Алиева, анестезиолог должен вовремя распознать и решить сложившуюся ситуацию. Если все прошло без осложнений, то наркоз не влияет на головной мозг и развитие ребенка. Об этом нет никаких достоверных данных, ведь каждый день в мире проводятся сотни тысяч операций у детей.
После окончания наркоза препараты быстро выводятся легкими, почками или инактивируются в печени. Поэтому не оказывают влияния на дальнейшую жизнь ребенка.
«Чтобы уменьшить возможные риски, — объясняет Владимир Алиев, — перед операцией анестезиолог подробно расспрашивает родителей. Он должен знать были ли раньше операции, наркозы и как ребенок их перенес. Также важно узнать о хронических заболеваниях, есть ли у него аллергия и на что именно. Анестезиолог беседует с родителями, объясняя все моменты операции и хода анестезии так, чтобы это было понятно».
Как подготовиться
Когда ребенку назначают плановую операцию, то сначала отправляют сдавать анализы. Это нужно, чтобы уменьшить риски от наркоза и операции.
Перед большими вмешательствами, которые предполагают длительный наркоз или возможное кровотечение, нужна более серьезная подготовка. Кроме основных анализов, ребенку нужно сдать кровь на инфекции: ВИЧ, сифилис, гепатиты В и С, а также сделать рентгенограмму, чтобы исключить туберкулез.
«Нужен общий анализ мочи и биохимия крови, чтобы убедиться в нормальной работе печени и почек, — продолжает Рузанна Аванесян, — обязательно проверить свертываемость, чтобы исключить риск кровотечений. Также нужна кардиограмма, чтобы вовремя заметить нарушения ритма, которые могут во время наркоза проявиться аритмией или другими осложнениями».
Если во время подготовки обнаружились отклонения от нормы в анализах или исследованиях, плановую операцию придется отложить. Нужно разобраться в причинах отклонений, чтобы обезопасить ребенка во время оперативного вмешательства.
«Если есть какой-то воспалительный процесс, то нужно найти причину и устранить его, — советует Рузанна Аванесян, — при нарушениях ритма возможно проведение операции после консультации кардиолога. Но анестезиолог должен быть в курсе, чтобы подготовиться к возможным осложнениям».
Детям с хроническими заболеваниями нужны не только общие анализы, но и консультации специалистов по заболеванию. Например, ребенку с эпилепсией нельзя вводить определенные препараты и его лечащий врач должен об этом написать в заключении. А ребенку с гемофилией потребуется дополнительное введение лекарств, чтобы снизить риск кровотечения.
Перед операцией анестезиолог обязательно должен поговорить с представителем ребенка. Он может задать много вопросов:
«На еду всегда строгий запрет на еду и питье, — предупреждает Владимир Алиев, — когда ребенок в бессознательном состоянии под влиянием анестезиологических препаратов, то защитные рефлексы перестают работать. Все мышцы расслабляются, в том числе мышцы желудка и пищевода. Поэтому при рвоте содержимое желудка может попасть в ротовую полость и оттуда в дыхательные пути. Кроме этого, рвота может быть реакцией на вдыхание анестетического газа».
В желудке агрессивная кислая среда. Если она попадет в дыхательные пути, то вызовет ожог слизистой, тяжелую воспалительную реакцию и пневмонию.
Продолжительность голодной паузы зависит от возраста ребенка и определяется анестезиологом. Маленьким детям обычно можно воду, грудное молоко или смесь за четыре часа до операции.
Перед операцией родителям нужно психологически подготовить ребенка. В спокойных понятных по возрасту выражениях объяснить, что будет происходить. Не стоит показывать ребенку свое беспокойство, чтобы не нервировать малыша.
«Я считаю, что родители должны говорить с ребенком так как есть, — говорит Владимир Алиев, — рассказать, что ребенок придет в операционную, там ему дадут специальную масочку, которую надо будет плотно прижать к лицу и глубоко дышать. Дома можно потренироваться с маской от небулайзера, например. Чтобы ребенку это было привычно и он не боялся маски. Также мы всегда пускаем родителей в операционную, чтобы сделать время до начала операции комфортным. Просмотр мультиков в начале анестезии на операционном столе тоже может снизить стресс и улучшить настроение ребёнка».
По словам Владимира Алиева, есть еще медикаментозные методы уменьшения стресса. Незадолго до операции ребенку делается внутримышечный укол или дается небольшое количество жидкости со специальным лекарством. После этого ребенка приносят в операционную в состоянии «полусна» без стресса. Важно всегда помнить, что польза для ребенка важнее.
Также перед операцией важно снять все украшения: цепочки, крестики и сережки. Если на ногтях был лак, нужно его убрать. Накрашенные ногти хуже пропускают информацию с датчиков. Кроме этого, цвет ногтей — один из показателей состояния ребенка и нужно, чтобы анестезиолог их видел.
Что делать после наркоза
Когда ребенок начинает просыпаться, он может быть растерянным и сонным или возбужденным. Это зависит от средств для наркоза, которые использовались и от скорости их выведения из организма.
«После окончания операции ребенка отдают родителям в тот момент когда он еще спит или уже почти проснулся, — предупреждает Владимир Алиев, — в это время необходимо наблюдать за ним. Я рекомендую положить ребенка на бок, если это возможно после операции. Если вдруг случиться рвота, положение на боку будет наиболее безопасным. Анестезиолог не отдаст ребенка, пока не будет уверен в восстановлении необходимых защитных рефлексов и определенного уровня сознания».
Из побочных эффектов чаще встречаются тошнота или рвота, озноб или дрожь. А также может быть боль в горле, если для наркоза использовали интубационную трубку. Когда ребенок окончательно проснулся и просит пить, можно намочить губы и дать небольшой глоток воды. Если это не вызвало тошноту, то через 15–20 минут можно дать еще несколько глотков.
«Главное после любой операции, чтобы ребенок нормально дышал, был в ясном сознании и вел себя как обычно, — говорит Владимир Алиев, — после операции анестезиолог рассказывает родителям обо всех особенностях прошедшего наркоза. И также рассказывает на что нужно обратить внимание в раннем послеоперационном периоде. Если затем с ребенком что-то будет не так, то родители заметят это быстрее и смогут забить тревогу».
Когда кормить ребенка, зависит от оперативного вмешательства. Это можно спросить у лечащего врача.
Реабилитация после операции. Выбор правильного питания
Полноценное, сбалансированное, легко усваиваемое питание обязательно включается в программу послеоперационной реабилитации.
Хирургическое вмешательство является для организма большим стрессом, как психологическим, так и физиологическим. Ответ организма на травматическое воздействие, которым по факту является операция, нейроэндокринная мобилизация защитных сил как реакция на угрожающую ситуацию, а также адаптация к изменившимся условиям функционирования прооперированных органов, – все это требует значительных энергетических затрат. В послеоперационном периоде усиливается распад белков, из которых строится новая соединительная ткань, усиленно расходуются углеводы, витамины и микро- и макроэлементы. В связи с ухудшением состояния желудочно-кишечного тракта после хирургического вмешательства, а в частности, с замедлением нормального всасывания, имеется большой риск возникновения белково-энергетической недостаточности.
Именно поэтому полноценное, сбалансированное, и что немаловажно – легко усваиваемое питание обязательно включается в программу послеоперационной реабилитации. К сожалению, часто специалисты, борясь с непосредственной угрозой для организма, забывают о создании условий для обеспечения процессов регенерации и восстановления полноценного функционирования.
Тяжесть заболевания и объем хирургического вмешательства — не единственные факторы влияния на продолжительность реабилитации и прогноз восстановления. Индивидуальные особенности каждого человека, его пол, возраст, вредные привычки, набор хронических заболеваний, общее физическое и психологическое состояние должны непременно учитываться не только для разработки программы восстановительного лечения, но и для подбора оптимального рациона. Только питание обеспечивает доступ энергии для нормального метаболизма и строительного материала для новых тканей.
Оптимальная диета после перенесенных хирургических вмешательств должна:
Специализированные смеси от Nestle были созданы с учетом особенностей патофизиологии пост-хирургических процессов и питательных нужд ослабленных пациентов:
Impact®Oral
Иммунопитание Impact®Oral показано для взрослых и детей от 7 лет перед и/или после операций на желудочно-кишечном тракте, в области головы, шеи и на других органах и системах.
Обогащенный аргинином молочный белок служит прекрасным материалом для регенерации тканей.
Иммуностимулирующий эффект питания, доказанный в рандомозированных исследованиях с участием более 2 000 пациентов в «большой» абдоминальной хирургии, обусловлен наличием в продукте аргинина, омега-3 жирных кислот и нуклеотидов в определенном соотношении.
Impact®Oral содержит среднецепочечные триглицериды (22% от общего жирового компонента) в качестве быстрого источника энергии для восстановления и пищевые волокна, которые улучшают работу пищеварительной системы, и подстегивают «кишечный» иммунитет.
Прием смеси в течение 5-7 дней в качестве дополнительного или единственного источника питания позволяет нормализовать метаболизм, иммунитет, скорректировать общие клинические показатели. После операции Impact®Oral применяют также в течение 5-7 дней в качестве дополнительного питания по 2-3 пакетика в день, в качестве единственного источника пищи 5 пакетиков в день. Смесь помогает быстрее восстановить силы, физическую форму и вернуться к нормальной жизни.
Resource®Diabet Plus
Продукт предназначен для пациентов с сахарным диабетом или нарушением толерантности к глюкозе, в частности, перенесшим хирургическую операцию.
Готовая смесь, содержащаяся в бутылочке объемом 200 мл, достаточно калорийна (320 ккал), чтобы побороть чувство голода и обеспечить организм энергией, но в то же время имеет низкий гликемический индекс и благотворно влияет на гликемический и жировой профиль. Углеводный компонент на 90% состоит из «медленных» углеводов и изомальтулозы. Высокая концентрация белка (смесь белков молочной сыворотки и казеина) – 18 г на одну бутылочку – полностью покрывает нужды восстанавливающегося организма в аминокислотах, расходном материале для создания клеточных структур. Пищевые волокна Prebio1+ и PHGG (частично гидролизованная гуаровая камедь) нормализуют работу пищеварительного тракта и благотворно влияют на гликемический профиль.
Смесь предназначена для перорального приема маленькими глоточками или через соломинку. Одна бутылочка по составу питательных веществ заменяет полноценный прием пищи. Resource®Diabet Plus можно использовать в качестве дополнения к пищевому рациону или в качестве единственного источника питания. Можно использовать для питания через зонд или стому.
Peptamen®
Пациентам, перенесшим большие операции, у которых в послеоперационном периоде наблюдается выраженное истощение, необходимо более интенсивное питание с гарантией усвоения питательных веществ. В таких случаях рекомендуется продукт Peptamen®. Даже при значительно сниженной способности кишечника к всасыванию и при поврежденной кишечной стенке, компоненты смеси Пептамен хорошо усваиваются организмом, снабжая организм необходимым количеством белков, жиров, углеводов, витаминов и микроэлементов.
Гидролизованный белок молочной сыворотки покрывает 12% энергетических затрат, снижает риск рефлюкса и диареи. Среднецепочечные триглицериды, составляющие 70% жирового профиля Пептамена, являются легкодоступным источником энергии, снижают риск жировой мальабсорбции. Цистеин, Омега-3 жирные кислоты и сбалансированное соотношение ARA (арахидоновой кислоты) и DHA (докозагексаеновой кислоты) способствуют контролю воспалительных реакций, ускоряют процессы регенерации.
Peptamen®Junior
Лечебное питание Peptamen®Junior рекомендовано для использования в педиатрии. Полноценное полуэлементарое питание на основе гидролизоанного белка молочной сыворотки подходит для детей от года до 10 лет. Продукт подходит маленьким пациентам с нарушением работы пищеварительной системы и с непереносимостью стандартных смесей, в частности, на основе казеина.
Помимо гидролизованого белка молочной сыворотки, Пептамен Юниор также как Пептамен для взрослых содержит среднецепочечные триглицериды (СЦТ) — 55% жирового профиля, витамины и минеральные вещества, которые с успехом обеспечивают организм энергией для быстрого восстановления. Поскольку Peptamen®Junior – сухая смесь для приготовления напитка, можно адаптировать ее концентрацию индивидуально под нужды малыша и использовать в качестве дополнительного или единственного источника питания.
Лечебное питание в послеоперационном периоде
Важнейшим фактором послеоперационной реабилитации больных, перенесших операции на органах пищеварения, является лечебное питание.
Диетотерапия направлена на удовлетворение пластических и энергетических потребностей организма больного. Правильное питание способствует снижению частоты осложнений и приводит к скорейшему выздоровлению. Важнейшей задачей диетотерапии как в условиях стационарного, так и амбулаторного этапов реабилитации считают преодоление белкового, витаминного, минерального и энергетического дефицитов, которые развиваются у большинства больных в связи с операционной травмой, лихорадкой и недостаточным питанием после операции.
Оперативное вмешательство, независимо от вида хирургического воздействия и сопровождающей его анестезии, вызывает мощные метаболические сдвиги в организме. На организм пациента влияют как специфические факторы хирургической травмы (крово- и плазмопотеря, гипоксия, токсемия, нарушения функций поврежденных органов), так неспецифические факторы, такие как болевые импульсы, возбуждение адренергической и гипофизарно-надпочечниковой систем.
Хирургический стресс характеризуется резким усилением процессов катаболизма, выраженными нарушениями метаболизма, особенно белкового и энергетического. Основными причинами этих нарушений являются катаболическое действие адренокортикотропного гормона и глюкокортикоидов, адреналина и вазопрессина, повышенный протеолиз в тканях, потери белка с отделяемым из операционной раны и увеличение энерготрат с утилизацией собственных белков. При этом не только усиливается катаболизм, но и угнетается синтез белков. Разрушение гликогена в печени и мышцах (легкодоступный, но небольшой по объему источник энергии), триглицеридов в жировой ткани считается частью раннего нейроэндокринного ответа на хирургическую травму. Резервы углеводов в организме ограничены, и поэтому в энергетический обмен активно вовлекаются тканевые белки, в первую очередь белки скелетных мышц.
Длительность и выраженность катаболической фазы стресса при тяжелых и обширных хирургических вмешательствах (резекция и пластика пищевода, желудка, гастрэктомия) препятствуют в ранний послеоперационный период реализации фазы долговременной адаптации.
У больных, перенесших оперативные вмешательства, в ближайшем послеоперационном периоде резко повышен энергетический обмен, в основном за счет неадекватного увеличения фактического основного обмена. При этом нередко энергетический дефицит достигает таких величин, что даже при потреблении обычного пищевого рациона (2500–3000 ккал/сут) больные все равно оказываются в условиях выраженной белково-энергетической недостаточности. При этом происходит переход на полное или частичное эндогенное питание, что приводит к быстрому (иногда катастрофическому) истощению резервов углеводов и жиров, а также значительной потере белков. Эти явления значительно ухудшают течение процессов регенерации, затягивают течение послеоперационного раневого процесса. Возникают предпосылки развития послеоперационных осложнений, в том числе пострезекционной дистрофии, спаечной болезни, эрозивно-язвенных осложнений, метаболических расстройств, вплоть до развития сепсиса.
Осложнения, наблюдаемые после операций на пищеварительном тракте (представленно по: J. C. Melchior, 2003):
Осложнения, связанные с поздним началом энтерального питания, приводящие к гастростазу, вздутиям живота, недостаточностью швов анастомозов.
Инфекционные осложнения, вызванные снижением иммунной и неспецифической защиты, обусловленные отсутствием питания, такие как нагноения послеоперационной раны, застойная пневмония, перитонит и сепсис.
Лечебное питание после операций на пищеводе
Диетотерапия – важная часть всего комплекса послеоперационной реабилитации больных, перенесших операции на пищеводе.
В ранние сроки после проведения оперативного лечения больному проводят восстановительное лечение в хирургическом стационаре, а затем в гастроэнтерологическом отделении, куда больной переходит на долечивание. На амбулаторное лечение больного переводят, как правило, через 1,5-2 месяца после операции.
Диетическое питание в первые месяцы после операции на пищеводе осуществляется по принципам проведения парентерального и энтерального искусственного питания.
Лечебное питание после операций на желудке и двеннадцатиперстной кишке
Больным, перенесшим оперативные вмешательства на желудке, в течение всей жизни рекомендуется соблюдать дробное питание (4–5 раз в день), ограничивать продукты и блюда, наиболее часто вызывающие демпинг-синдром (сладкие напитки, сладкие молочные каши, очень горячие и очень холодные блюда), принимать пищу не спеша, тщательно пережевывая ее.
Лечебное питание при постгастрорезекционных синдромах
Среди неблагоприятных последствий операций на желудке выделяют следующие патологические состояния:
Синдром приводящей петли.
Пептическая язва анастомоза.
Гастрит культи желудка.
Питание при демпинг-синдроме
Демпинг-синдром – это наиболее частое осложнение, возникающее в различные сроки после резекции желудка по поводу язвенной болезни.
Основными признаками этого заболевания являются: чувство жара, сердцебиение, одышка, потливость, слабость, головокружение, сухость во рту, тошнота, рвота, «дурнота», боли в животе, вздутие его, понос, сонливость, усталость, непреодолимое желание лечь, обморочное состояние. Все эти явления появляются чаще всего после еды, особенно после приема сладкой, горячей, молочной пищи. В лежачем положении эти явления ослабевают.
Возникновение демпинг-синдрома связано с быстрым переходом (сбросом) недостаточно переваренной пищи из культи желудка непосредственно в тонкую кишку, минуя двенадцатиперстную кишку, удаленную в процессе операции. Стремительный пассаж химуса по тонкой кишке провоцирует нарушения гуморальной регуляции за счет изменения внутрисекреторной функции поджелудочной железы. В результате возникают патологические проявления демпинг-синдрома.
Выделяют три степени тяжести демпинг-синдрома.
Легкая степень тяжести. Характеризуется тем, что приступы возникают только после обильного приема пищи или пищи, богатой простыми углеводами. Приступ сопровождается легкими вазомоторными и кишечными симптомами, которые быстро проходят в положении больного лежа. Трудоспособность у этих больных сохраняется.
Средняя степень тяжести демпинг-синдрома. Проявляется выраженными вазомоторными нарушениями и кишечными симптомами, возникающими ежедневно. Больной вынужден принимать горизонтальное положение, которое улучшает его самочувствие. Общая работоспособность больного снижена.
Тяжелая форма демпинг-синдрома. Проявляется ярко выраженными приступами почти после каждого приема пищи, иногда с обморочным состоянием, что приковывает больного к постели на 1–2 часа. Трудоспособность больных резко снижается или полностью утрачена.
Ведущим методом лечения демпинг-синдрома является правильно построенный диетический режим.
Общие рекомендации по питанию при демпинг-синдроме
Частое дробное питание небольшими порциями (5-7 раз в день). Принимать пищу следует медленно. Пища должна быть медленно и тщательно пережевана.
Ограничение продуктов и блюд, наиболее часто вызывающих демпинг-синдром: сладостей (сахар, мед, варенье), очень горячих или очень холодных блюд, жидких сладких молочных каш и др.
Прием жидкости производить отдельно от остальных блюд, т.е. чай, молоко, 3-е блюдо в обед и кефир вечером следует употреблять через 20-30 минут после основного приема пищи. Количество жидкости за один прием не должно быть обильным (не более 1 стакан).
Пища и напитки должны быть теплыми.
После еды пациент должен принять лежачее положение на 20–30 мин., особенно после обеда.
Пища должна содержать достаточное количество пектина (овощи и фрукты).
Этапность диетотерапии при демпинг-синдроме
При этом в питании резко ограничивают продукты и блюда, содержащие простые (быстро всасывающиеся) углеводы – сладкие жидкие молочные каши, особенно манную, рисовую, сладкое молоко, сладкий чай. Больным противопоказаны холодные и очень горячие блюда. Рекомендуется раздельный прием жидкой и плотной части пищевого рациона, причем жидкость следует употреблять через 30 мин после приема твердой пищи, а во время обеда сначала надо съедать второе блюдо, а затем первое.
При осложнении демпинг-синдрома панкреатитом или при подозрении на пептическую язву культи желудка, анастомоза или тощей кишки рекомендуется диета № 1 с добавлением в 17 часов белкового блюда. При отсутствии осложнений и при хорошем самочувствии больного диету можно постепенно расширять, соблюдая основные ее принципы, и постепенно переходить на обычный пищевой рацион.
Питание при синдроме приводящей петли
В основе патогенеза синдрома приводящей петли лежит нарушение эвакуации содержимого из приводящей петли вследствие ее перегибов, образования спаек, нарушения моторной функции из-за изменения нормальных анатомических взаимоотношений.
Синдром приводящей петли обычно развивается в течение первого года после операции. Он проявляется сильными болями в эпигастрии и правом подреберье, рвотой желчью после еды. В промежутках между приемами пищи больные испытывают чувство тяжести в верхней части живота в результате заброса кишечного содержимого обратно в желудок, накоплением жидкости и пищи в приводящей петле и в культе желудка.
Тактика восстановительного лечения и диетического питания при синдроме приводящей петли такая же, как и при демпинг-синдроме.
Питание при астеническом синдроме
Астенический синдром является поздним послеоперационным осложнением резекции желудка.
Частота его появления находится в прямой зависимости от уровня резекции желудка. Большое значение в патогенезе этого состояния имеет нарушение секреторной и моторной функций культи резецированного желудка, изменение секреции желчи и панкреатического сока. В патогенезе определенное значение имеет быстрый пассаж по тощей кишке, нарушение всасывания железа и витаминов.
Для больных характерны быстрая утомляемость, общее недомогание, похудание, признаки гиповитаминоза, склонность к гипотонии и обморочным состояниям, нервно-психические нарушения. Общая слабость усиливается чаще всего после еды, особенно богатой углеводами. Наблюдаются различные диспептические явления: пониженный аппетит, отрыжка, срыгивание горькой жидкостью, ощущение тяжести в подложечной области. Характерным симптомом является расстройство кишечной деятельности, выражающееся в появлении (особенно после молочной и жирной пищи) громких кишечных шумов и поноса.
Питание при пептических язвах анастомоза и гастрите культи желудка
В механизмах развития пептических язв анастомоза и гастрита культи желудка первостепенное значение придается агрессивному действию желудочного сока и развитию хеликобактерной инфекции. Кроме того, имеет значение забрасывание дуоденального и кишечного содержимого в желудок, слабая перистальтическая функция культи желудка и быстрое опорожнение ее после еды.
Клиника пептической язвы анастомоза сходна с проявлениями язвенной болезни, но симптомы заболевания обычно более интенсивны, периоды обострения более длительны, чем при язве, по поводу которой была произведена операция. Характерны снижение аппетита, потеря массы тела.
Лечебное питание после операций на кишечнике
Правильная диетотерапия после операций на кишечнике способствует снижению частоты осложнений и более быстрому выздоровлению больного.
Традиционные подходы к лечебному питанию больных, перенесших операции на тонкой и толстой кишке, основанные только на принципах сбалансированного питания не приводят к восстановлению всего объема физиологических функций. Целесообразно подходить к реабилитации больных после резекции кишечника, с позиций теории адекватного питания, сформулированной академиком А. М. Уголевым. Необходимо обеспечивать не только элементное восстановление содержания нутриентов в организме, но и максимально восстановить полостное и мембранное пищеварение, всасывание в кишечнике, а также восстановить нормальный микробиоценез. Только при соблюдении этих условий возможна нормализация работы всего пищеварительного тракта.
Принципы питания больных, перенесших операции на кишечнике
Лечебное питание должно обеспечить щажение кишечника, а также других отделов желудочно-кишечного тракта.
Лечебное питание должно способствовать нормализации обмена веществ и восстановлению организма.
Лечебное питание должно повысить сопротивляемость организма при явлениях воспаления и интоксикации.
Лечебное питание должно способствовать заживлению операционной раны.
При отсутствии осложнений желателен более ранний перевод больных на физиологически полноценное питание с широким продуктовым набором.
Этапность диетотерапии после операций на кишечнике
В непосредственно послеоперационном периоде необходимо наладить парентеральное питание больного. В первую очередь это касается введения энергетических субстратов. Объем и состав парентерального питания определяют индивидуально в зависимости от потребности больного.
Стабилизация состояния больного и контролируемая диарея служат показаниями к переходу на питание с использованием желудочно-кишечного тракта. Обычно это происходит через 3–4 дня после операции. В то же время при обширных резекциях тонкой кишки некоторые специалисты рекомендуют начинать энтеральное питание через 2–4 недели после операции. В большинстве клинических случаев назначают стандартные смеси для энтерального питания, однако при резекциях тонкой кишки целесообразно применение деполимеризированных нутриентов (полуэлементных диет). Комбинированное парентерально-энтеральное питание в комплексной реабилитации больных после оперативных вмешательств на кишечнике позволяет сократить сроки и повысить эффективность восстановительного лечения, значительно снизить частоту осложнений и неблагоприятных исходов послеоперационного процесса.
При положительной динамике состояния больного рекомендован переход на естественное питание. Однако, следует помнить, что необоснованно ранний перевод больных на естественное питание после операций на кишечнике существенно ухудшает течение восстановительного периода, стимулирует развитие синдрома энтеральной недостаточности, нарушает естественные механизмы полостного и мембранного пищеварения.
Через 3–4 недели после выписки больного из стационара требуется постепенный переход на непротертый вариант диеты № 1. Постепенность перехода с одного варианта диеты на другой предполагает каждодневное сокращение количества протертых блюд. Хорошая переносимость вводимых блюд является свидетельством нормализации секреторной и моторно-эвакуаторной функций системы пищеварения и позволяет продолжить расширение диеты.
При плохой переносимости молока больными после операций на кишечнике следует надолго (иногда навсегда) исключить потребление молока. Лактозные перегрузки при наличии ферментатной недостаточности способны усугубить секреторные расстройства кишечника. Таким образом, при развитии послеоперационной лактозной недостаточности в диете больных следует максимально и надолго ограничить цельное молоко. К потреблению молочнокислых продуктов это относится в меньшей степени. Замена молочных продуктов может быть с успехом проведена за счет соевых продуктов. Соевые белки являются очень важным источником дополнительного обеспечения организма высокопластичным белком.
Питание при синдроме короткой кишки
Состояние, которое развивается после резекции тонкой кишки и характеризуется диареей, стеатореей, мальабсорбцией нутриентов, принято называть синдромом короткой (или укороченной) кишки.
При удалении менее 50% тонкой кишки синдроме короткой кишки протекает субклинически, но больший объем резекции приводит к нарастающей диарее, стеаторее, дефициту железа и фолиевой кислоты.
У больных с благоприятным течением послеоперационного периода при достаточно быстром восстановлении функций кишечника следует осуществлять постепенный, но обоснованно быстрый переход на полное естественное питание. Однако, то после осуществления обширных резекций кишечника переход от полного парентерального к естественному питанию должен проходить достаточно длительный этап частичного парентерального питания, растянутый подчас на несколько месяцев. Длительность переходного периода определяется сугубо индивидуально. В ряде случаев при обширных резекциях тонкой кишки пациент должен пожизненно получать полное или частичное парентеральное питание.
Введение новых продуктов в рационы лечебного питания должно строго зависеть от индивидуальной переносимости больных. Белково-энергетический дефицит рассматриваемых диет по отношению к физиологическим потребностям организма должен покрываться парентеральными средствами питания. Последовательность применения стандартных диет приведены выше.
После перехода на полное естественное питание больным с короткой кишкой рекомендуется диета с повышенным содержанием белка, углеводов и умеренным количеством жира. Диета должна быть дополнена триглицеридами со средней длиной углеродной цепи, поливитаминами в жидких формах, витамином В12 (внутримышечно 1 мг каждые 2–4 нед), фолиевой кислоты (внутримышечно по 15 мг в неделю), витамином К (внутримышечно по 10 мг в неделю), препаратами железа (парентерально, а затем и перорально).
Необходим динамический лабораторный контроль уровня оксалатов в моче. При появлении первых признаков гипероксалурии необходимо ограничить прием продуктов, содержащих повышенное количество оксалатов (щавель, шпинат, петрушка, картофель, шоколад).
Через 1-2 года после операции могут наблюдаться различные клинические варианты течения заболевания. В зависимости от состояния пациента и назначается лечебное питание.
Возможны следующие индивидуальные сценарии диетотерапии больных:
Естественное нормальное или близкое к нормальному питание.
Естественное питание с использованием индивидуально подобранных специализированных продуктов, содержащих деполимеризированные (короткоуепочечные) нутриенты (белки, жиры и углеводы).
Естественное питание с частичной парентеральной поддержкой.
Полное парентеральное питание.
Лечебное питание после операций на печени
В непосредственно послеоперационном периоде необходимо наладить парентеральное питание больного. В первую очередь это касается введения энергетических субстратов. Объем и состав парентерального питания определяют индивидуально в зависимости от потребности больного. Рекомендуемая в настоящее время продолжительность полного сбалансированного (по белкам, жирам, углеводам) парентерального питания зависит от объема и сложности проведенной операции на печени и составляет в среднем 3–5 дней.
Переход к естественному питанию должен проходить этап комбинированного (парентерально-энтерального) питания продолжительностью не менее 4–5 дней. Это связано с тем, что в результате операционной травмы печени происходит значительное угнетение функции тонкой кишки, восстановление которой занимает не менее 7–10 дней после операции. Зондовое введение элементных питательных смесей в пищеварительную систему в постепенно возрастающих количествах обеспечит у больных после операций на печени адаптацию желудочно-кишечного тракта к усиливающимся пищевым нагрузкам. Сочетание энтерального питания с парентеральным направлено на предотвращение метаболического голода.
Лечебное питание после операций на желчевыводящих путях
Общие правила питания для больных после операций на желчевыводящих путях
Частое, дробное питание. Прием пищи каждые 3,5–4 ч.
Ограничение продуктов, богатых холестерином.
Равномерное распределение жиров на все приемы пищи и перемешивание их с пищей, что способствует лучшему усвоению жиров, профилактике боли и диспепсических явлений.
После операций на желчных путях ухудшается переносимость очень многих продуктов, что требует минимизации их употребления. Особенно плохо больные переносят овощи, богатых эфирными маслами (редьку, редис, зеленый лук), острые блюда (перец, маринады, майонез, консервы). Также больные, перенесшие операцию на желчных путях, часто плохо воспринимают молоко, мороженое, шоколад, какао.
Лечебное питание больных, перенесших холецистэктомию
Через 24 часа после операции – минеральная вода без газа или отвар шиповника без сахара (маленькими глотками, не более 1 литра в сутки).
Через 36–48 часов – минеральная вода без газа, несладкий кисель из сухофруктов, несладкий некрепкий чай, нежирный кефир в объеме 1–1,5 л в течение суток (по 100–150 мл на один прием через каждые три часа).
В дальнейшем осуществляется переход на непротертый вариант диеты № 5а. Соблюдать эту диету рекомендовано в течение 1,5–2 месяцев после холецистэктомии и других видов хирургического лечения заболеваний билиарной системы.
Однако не все больные хорошо переносят диету № 5а: возникают транзиторные поносы, вздутие живота, метеоризм и появление связанных с этим болей в пилородуоденальной зоне и правом подреберье. Для этих случаев разработана диета № 5щ (щадящая), эта диета также назначается на 1–1,5 месяца после операции на желчных путях. Однако диета № 5щ (щадящая) не показана больным с пониженной массой тела из-за низкой ее энергоемкости, к тому же полное исключение растительного масла на фоне резкого ограничения жиров может способствовать формированию холестатического синдрома.
Несоблюдение принципа химического и механического щажения пищеварительной системы в 1,5–2 месяца восстановительного лечения после холецистэктомии способно привести к формированию хронического течения энтеральной недостаточности как одной из форм постхолецистэктомического синдрома.
Лечебное питание при постхолецистэктомическом синдроме
У 20–40% больных после проведения холецистэктомии развивается постхолецистэктомический синдромом. Данный синдром может быть обусловлен самыми разнообразными заболеваниями: камнями в желчных протоках, спазмом или стриктурой сфинктера Одди, гастритом, дуоденитом, язвенной болезнью, панкреатитом, дисбактериозом кишечника. Необходимо уточнить причину постхолецистэктомического синдрома, после чего назначать медикаментозное и диетическое лечение.
При постхолецистэктомическом синдроме используются следующие диеты:
При возникновении после холецитэктомии застоя желчи, гипомоторной дискинезии используют диету № 5 л/ж (липотропно-жировую).
Лечебное питание после операций на поджелудочной железе
Лечебное питание больных, перенесших операции на поджелудочной железе, независимо от характера заболевания, должно складываться из двух этапов: искусственное питание (парентеральное, зондовое, смешанное) и естественное питание.
На исход оперативного вмешательства положительно влияют длительность искусственного питания больного, адекватный компонентный состав и энергетическая ценность нутриционного обеспечения.
Этапность диетотерапии после операций на поджелудочной железе
Первый этап – полное парентеральное питание. Продолжительность полного парентерального питания больных, перенесших тяжелые хирургические вмешательства на поджелудочной железе, должна быть не менее 10–12 дней при условии полной белково-энергетической обеспеченности рациона нутриционной поддержки. Это позволяет свести до минимума послеоперационные осложнения. При менее тяжелых оперативных вмешательствах переход от парентерального к естественному питанию может состояться не ранее 5–7-го дня.
Второй этап – частичное парентеральное питание. Применяется в период перехода к естественному питанию. Сочетание постепенно нарастающего объема естественного питания с постепенно редуцирующимся парентеральным питанием – основное требование к лечебному питанию в условиях послеоперационной реабилитации. Это позволяет сохранить на должном физиологическом уровне белково-энергетическое обеспечение организма в данный период реабилитации и одновременно осуществлять плавно возрастающую пищевую нагрузку за счет механически, химически и термически щадящей гипокалорийной диеты.
Третий этап – естественное питание. Необходимо максимально медленно увеличивать пищевую нагрузку больным после операций на поджелудочной железе. Решение вопросов о расширении пищевого рациона, перехода с одной диеты на другую, требует тщательной оценки показателей состояния организма и особенностей течения заболевания.
Вначале больным после операций на поджелудочной железе назначается диета № 0а на срок 5–7 дней, а не на 2–3 дня, как при операциях на других органах.
На смену диеты № 0а назначают диету № 1а на срок 5–7 дней, также восполняя белково-энергетический дефицит средствами парентерального питания.
В дальнейшем рекомендуется переход на диету № 1б на срок 5–7 дней.
Статья добавлена 27 января 2016 г.